Cell子刊 | 北京大学邓宏魁团队揭示人多能干细胞衍生的β细胞成熟过程中的脂质代谢重塑
Highlights
1. 单细胞多组学分析确定脂质代谢在β细胞成熟中起重要作用
2. 神经酰胺稳态在hPSC-β细胞成熟过程中被重塑
3. TH34通过减少细胞内神经酰胺积累改善hPSC-β细胞的功能成熟
近日,Cell Stem Cell(IF:19.8)上发表题为“Remodeling ceramide homeostasis promotes functional maturation of human pluripotent stem cell-derived β cells”的论文,探讨了人多能干细胞(hPSC)衍生的β细胞(hPSC-β细胞)成熟过程中,鞘氨醇代谢重塑对β细胞功能成熟的重要性。

研究背景介绍
hPSC具有分化成各种类型细胞的潜力,包括胰岛分泌的β细胞,这为糖尿病等代谢性疾病的治疗提供了新策略。目前,hPSC-β细胞在功能上(如基因表达谱、转录组熵、细胞内Ca2+振荡、线粒体呼吸以及胰岛素分泌等)常表现出不成熟表型,限制了其在临床中的应用。
尽管在发育生物学的指导下,hPSC分化研究已取得一定进展,但揭示hPSC-β细胞成熟过程的分子机制,特别是在体内成熟过程中的功能获得,仍是当前研究的重点和挑战。
研究思路分析
01hPSCs-β细胞的体内成熟过程
①将hPSC-胰岛移植到免疫缺陷小鼠肾囊下,8周后观察到小鼠血浆中人C肽表达逐渐升高,提示hPSC-β细胞在体内逐渐成熟。
②在hPSC-β细胞成熟过程中,超过80%的差异表达基因下调,且染色质可及性降低。
③hPSC-β细胞成熟过程中观察到4种不同的基因表达模式,涉及代谢适应、细胞功能负向调控因子去除以及转录组和表观遗传组的建立。
02调控hPSCs-β细胞成熟的调控因子识别
①通过分析染色质调控域(DORCs)和预测染色质(GPCs)基因,鉴定调控hPSC-β细胞成熟的“主导因子”,包括正向和负向调节转录因子。
②脂质代谢重塑,尤其是鞘脂代谢中的神经酰胺代谢活性下调,对hPSC-β细胞成熟至关重要。
03促进 hPSCs-β 细胞成熟的小分子化合物筛选
①研究人员通过小分子化合物富集分析和筛选,找到一种HDAC抑制剂TH34,可以有效降低细胞内鞘氨醇的含量,从而提高hPSC-β细胞的功能成熟度。
②TH34处理后,hPSC-β细胞在胰岛素分泌、钙瞬变、线粒体功能和逆转糖尿病等方面获得显著性改善。
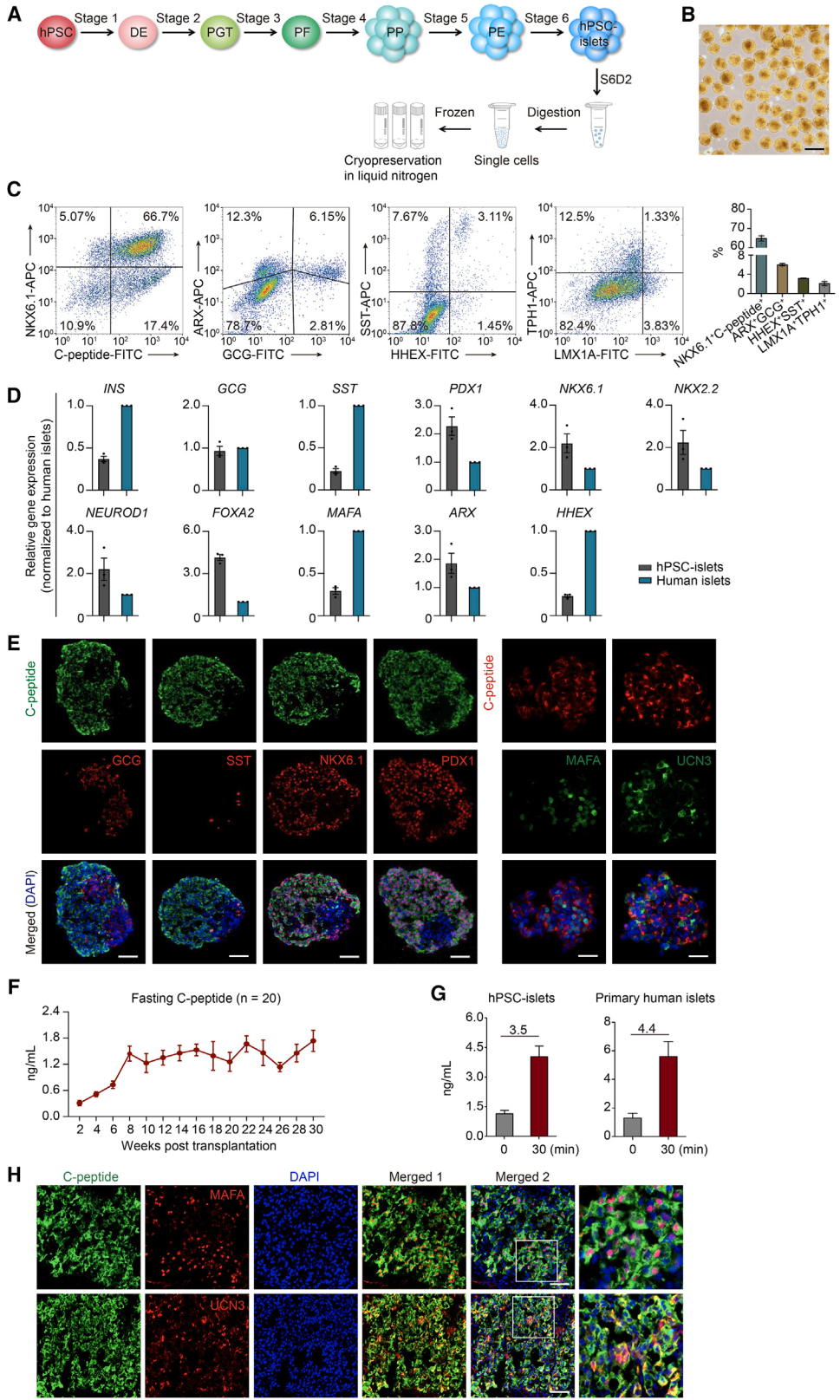
图1.移植前后hPSC-胰岛的特征
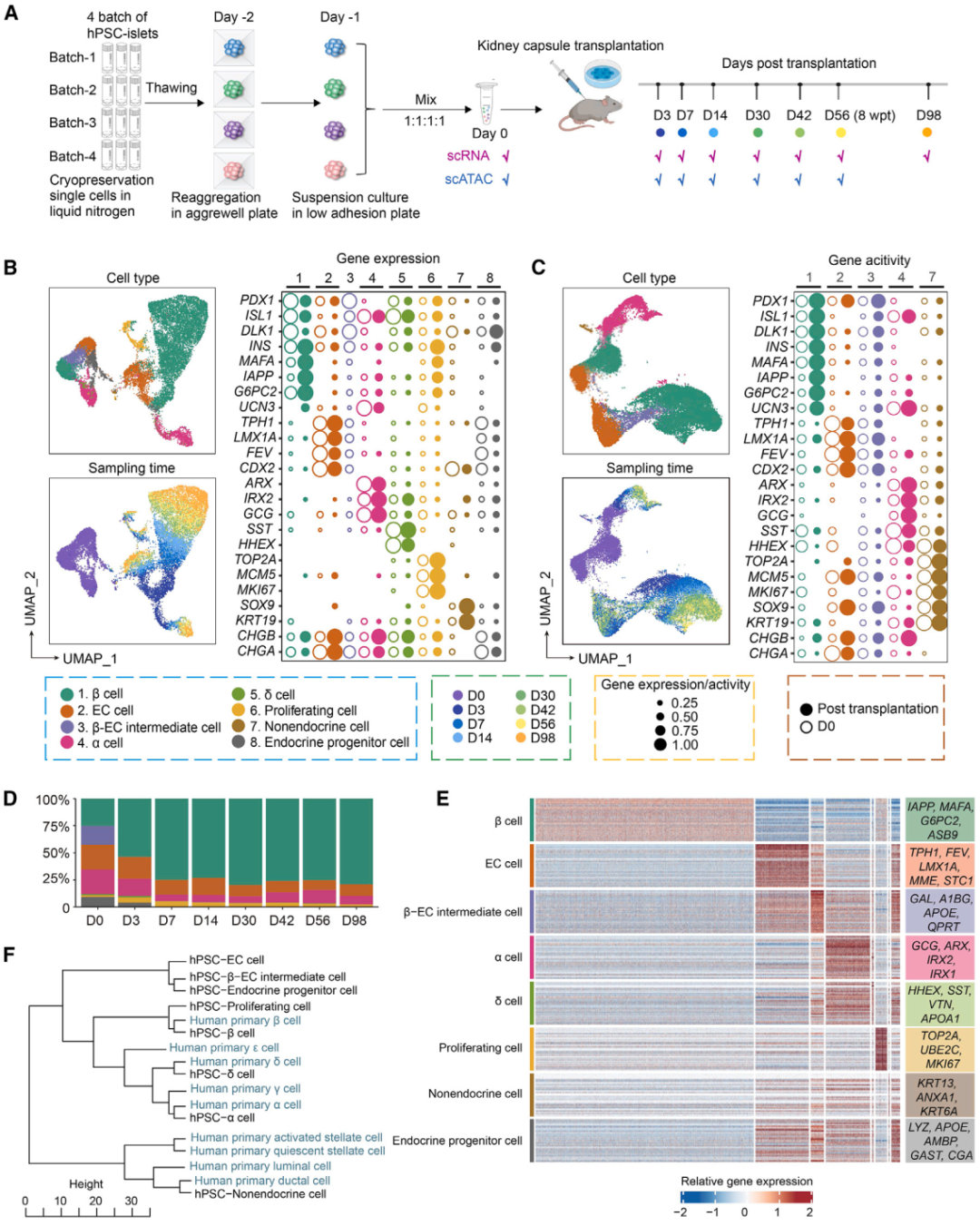
图2.移植后hpsc-胰岛的单细胞基因表达及染色质可及性分析
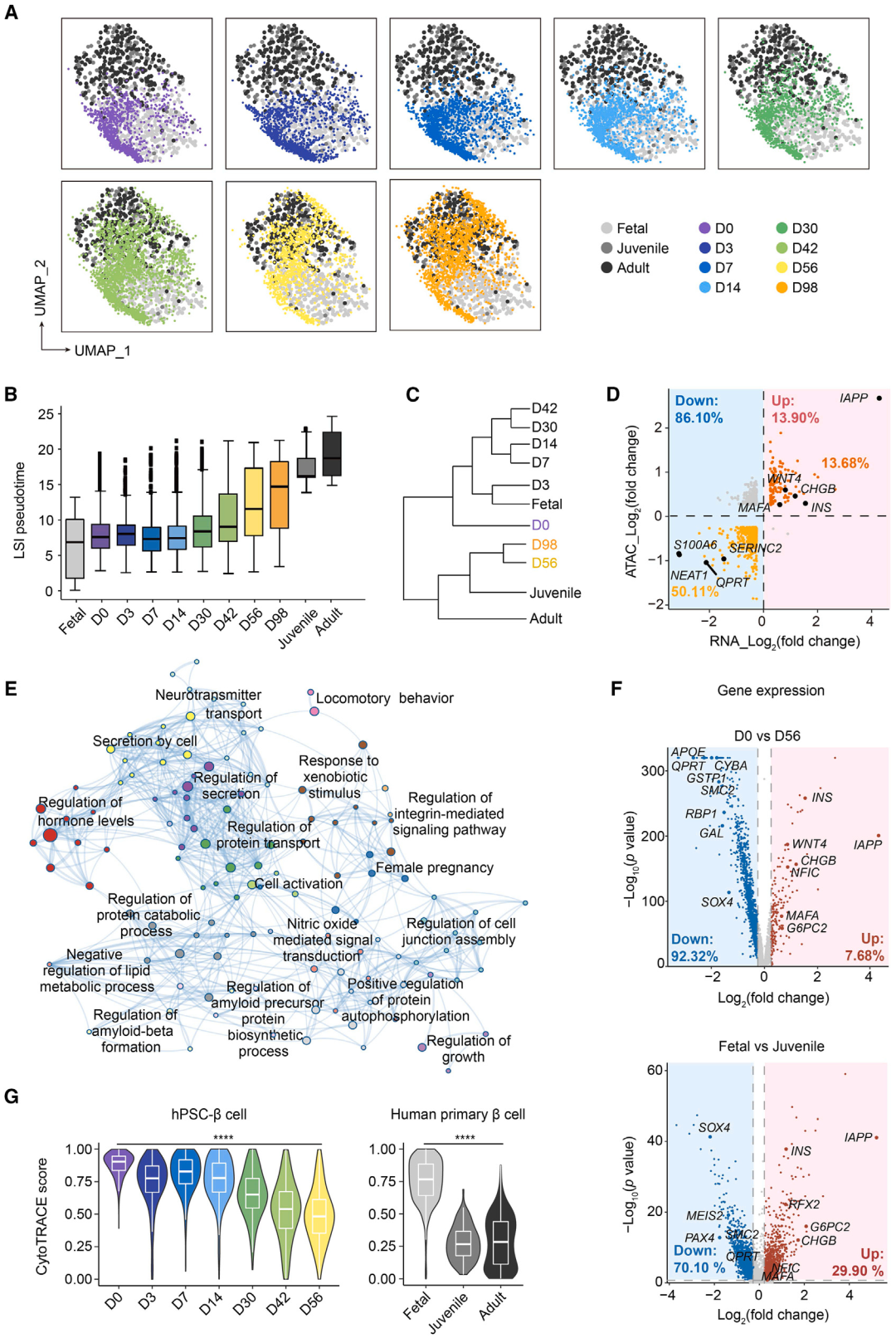
图3. scRNA-seq和scATAC-seq分析显示hPSC-β细胞在移植后逐渐成熟
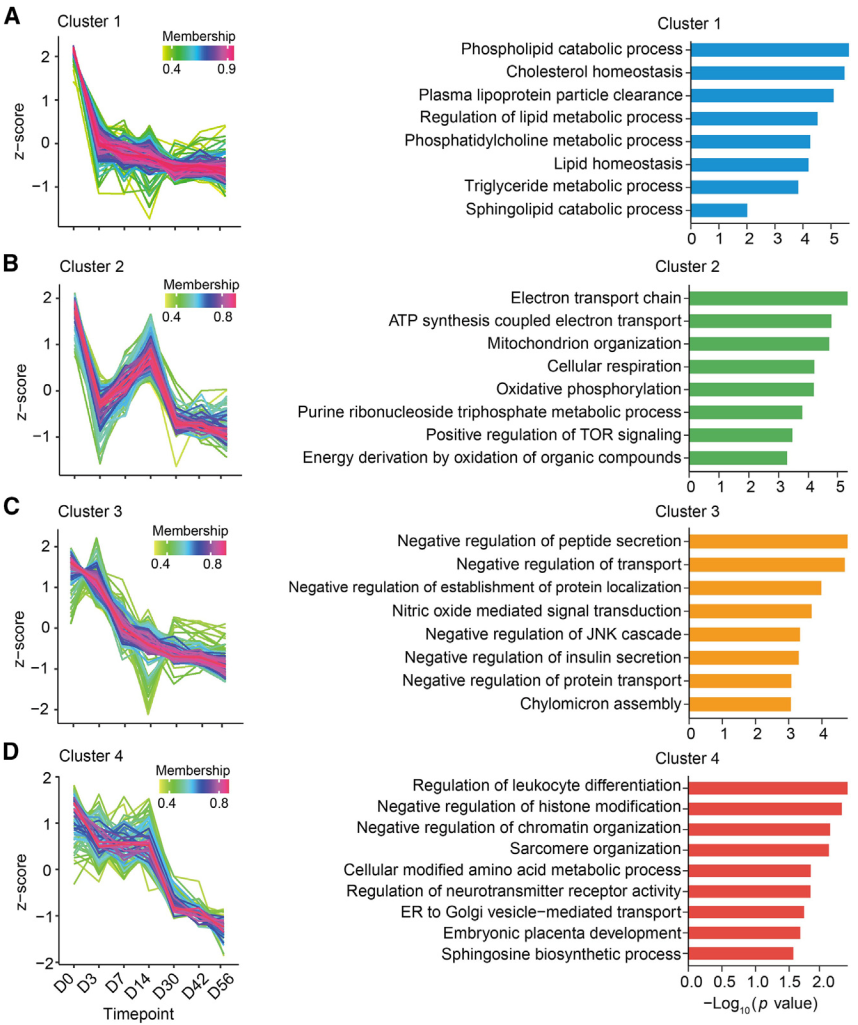
图4.在hPSC-β细胞成熟过程中,染色质可及性降低且表达下调的四种不同的基因表达模式
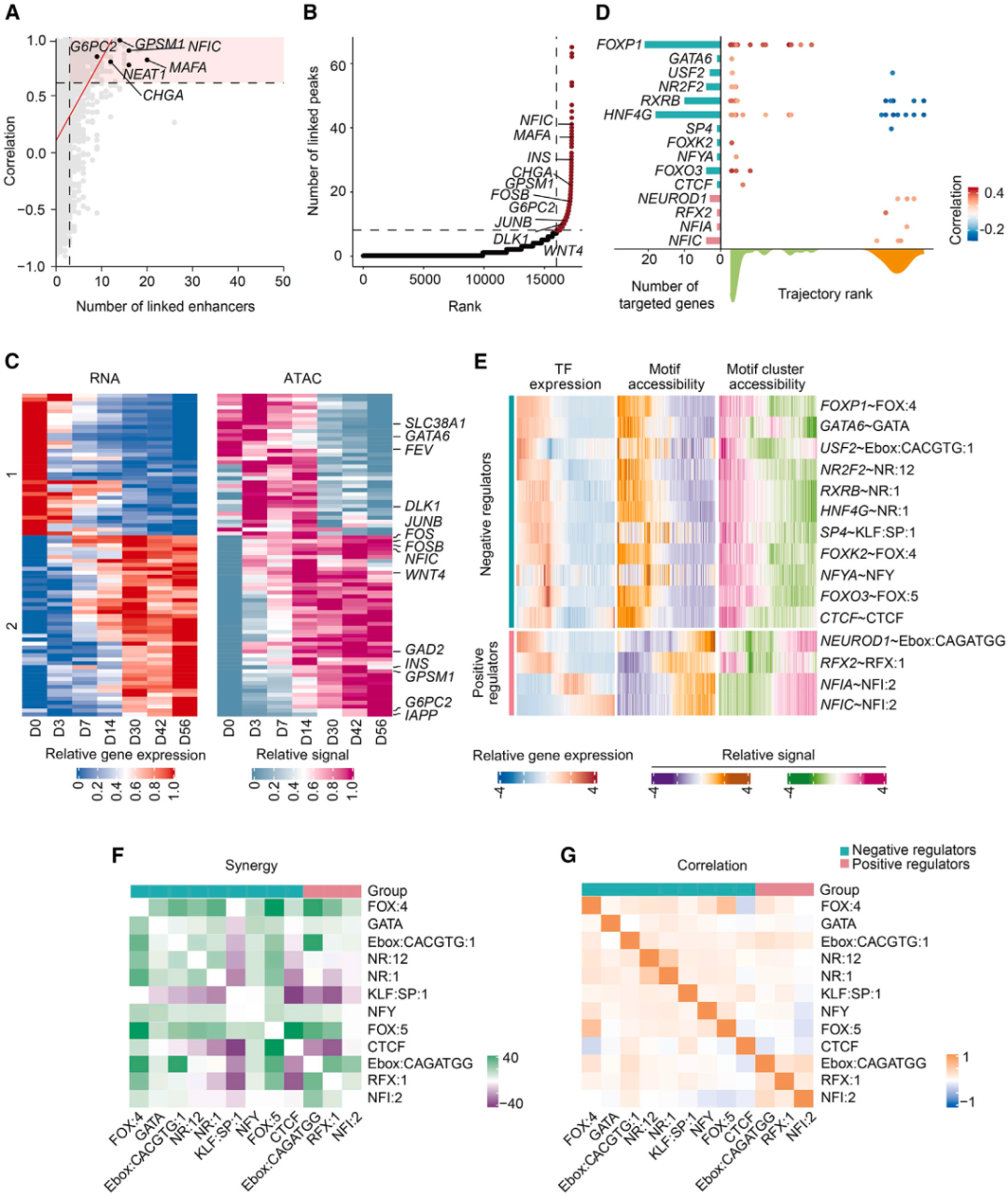
图5.调控hPSC-β细胞成熟的关键调控通路
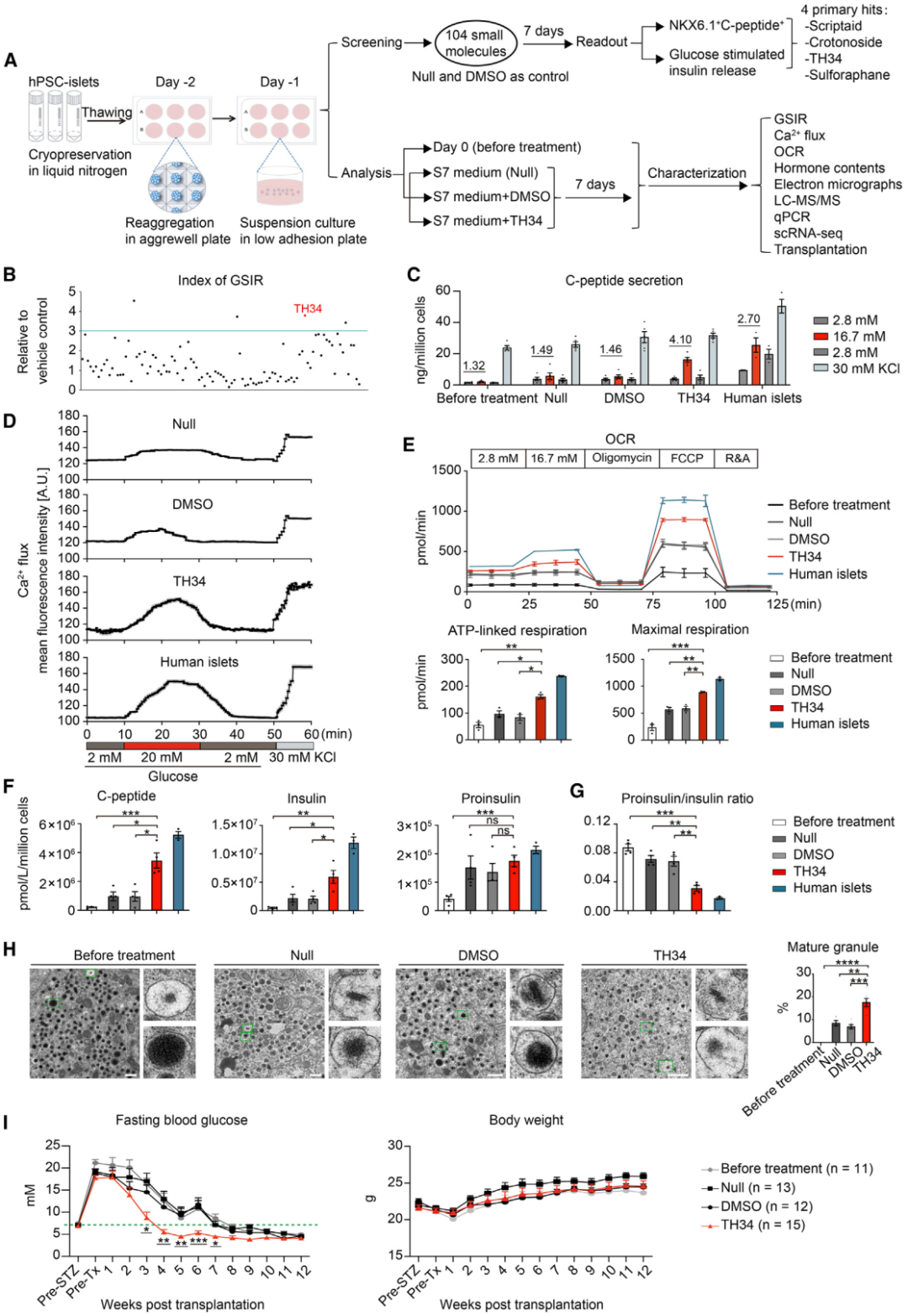
图6. TH34可促进体外hPSC-β细胞的功能成熟
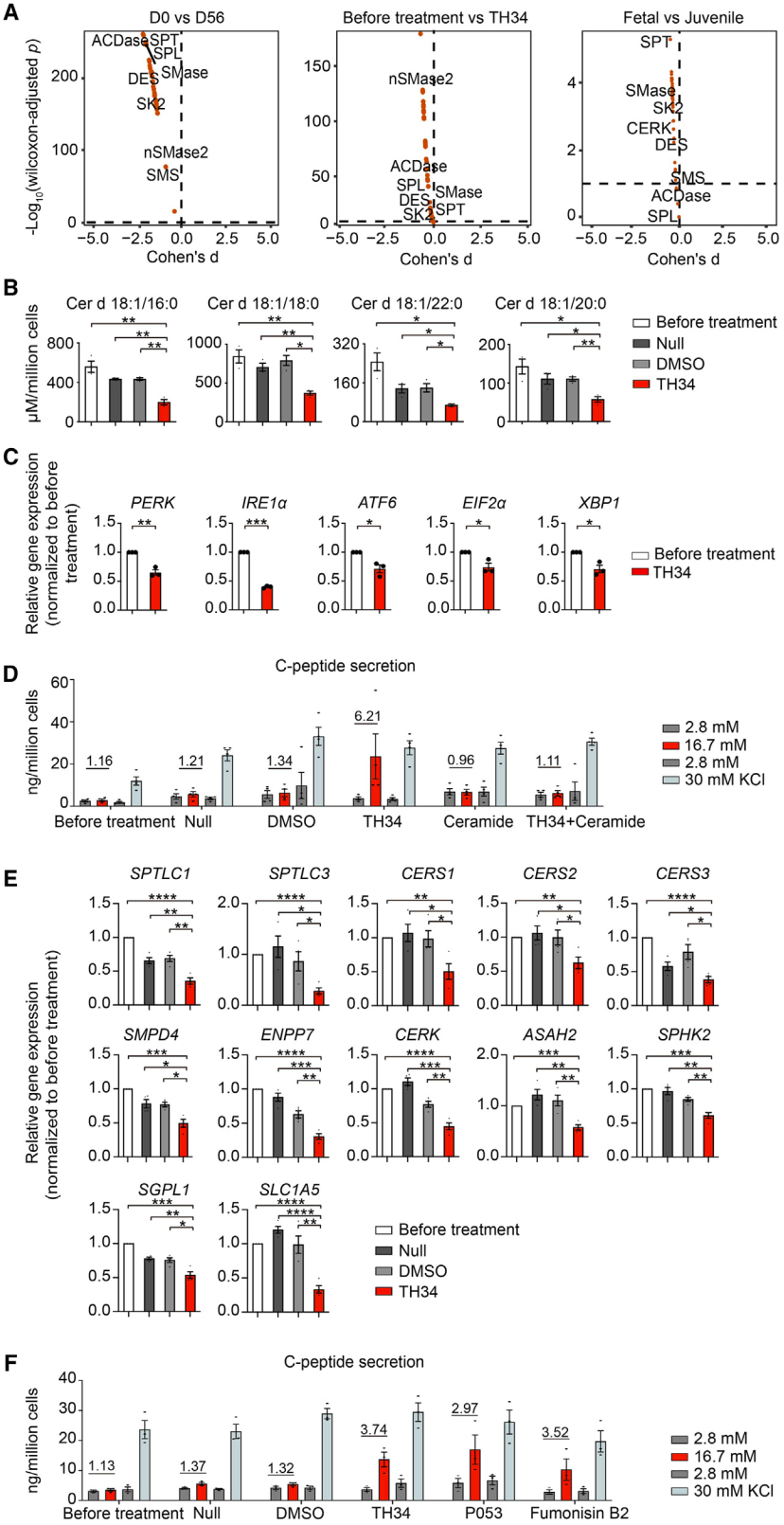
图7. TH34治疗可重塑hpsc-胰岛的神经酰胺代谢
结论与讨论
本研究利用单细胞多组学技术分析,证实hPSC-β细胞的成熟是一个有序的多步骤过程,涉及代谢适应、细胞功能负向调控因子去除以及更专业的转录组和表观遗传基因组的建立。此外,脂质代谢,特别是鞘氨醇代谢的重塑,对β细胞成熟至关重要。小分子化合物TH34可有效降低细胞内鞘氨醇的积累,从而改善hPSC-β细胞的功能并促进其成熟,为糖尿病等代谢疾病的治疗提供了新的策略。
未来,仍需深入研究TH34及其他小分子化合物对不同hPSC系和不同分化阶段的作用,并探索hPSC-β细胞成熟过程中其他代谢途径的变化及其对细胞功能的影响。此外,仍需开发新的方法和策略来进一步提高hPSC-β细胞的成熟度和功能。
















 {{item.name}}会员
{{item.name}}会员
