上海大学最新35.5分SCI:抑制Hmbox1激活Gck促进心肌细胞存活和糖代谢,为治疗心脏缺血/再灌注损伤提供新策略
Highlights
1. 在I/R损伤中,抑制Hmbox1能够保护心脏的功能,减少了心肌细胞的凋亡。
2. Hmbox1通过直接靶向并抑制Gck的表达来调控心肌细胞的代谢和存活
3. ETS1能够负向调控Hmbox1的表达
近日,“Circulation”(IF=35.5)上发表了一篇题为“Inhibition of Hmbox1 Promotes Cardiomyocyte Survival and Glucose Metabolism Through Gck Activation in Ischemia/Reperfusion Injury”的文章。这篇文章主要研究了Hmbox1在心脏缺血/再灌注损伤中的作用,以及其对心肌细胞存活和葡萄糖代谢的影响。

研究背景介绍
Hmbox1是一种含有同源结构域的转录因子。它在多种细胞过程中发挥作用,包括细胞分化、增殖、凋亡和自噬。
葡萄糖激酶(Gck)是一种在糖酵解途径中催化葡萄糖磷酸化的酶。
ETS1是一种转录因子,属于ETS家族成员,参与多种生物学过程,包括细胞增殖、分化和迁移。
缺血/再灌注(I/R)损伤发生在血流恢复至缺血组织时,可能引起额外的细胞损伤。在心脏中,I/R损伤常见于心肌梗死后的再灌注治疗,是心脏疾病研究的重要领域。
研究思路分析
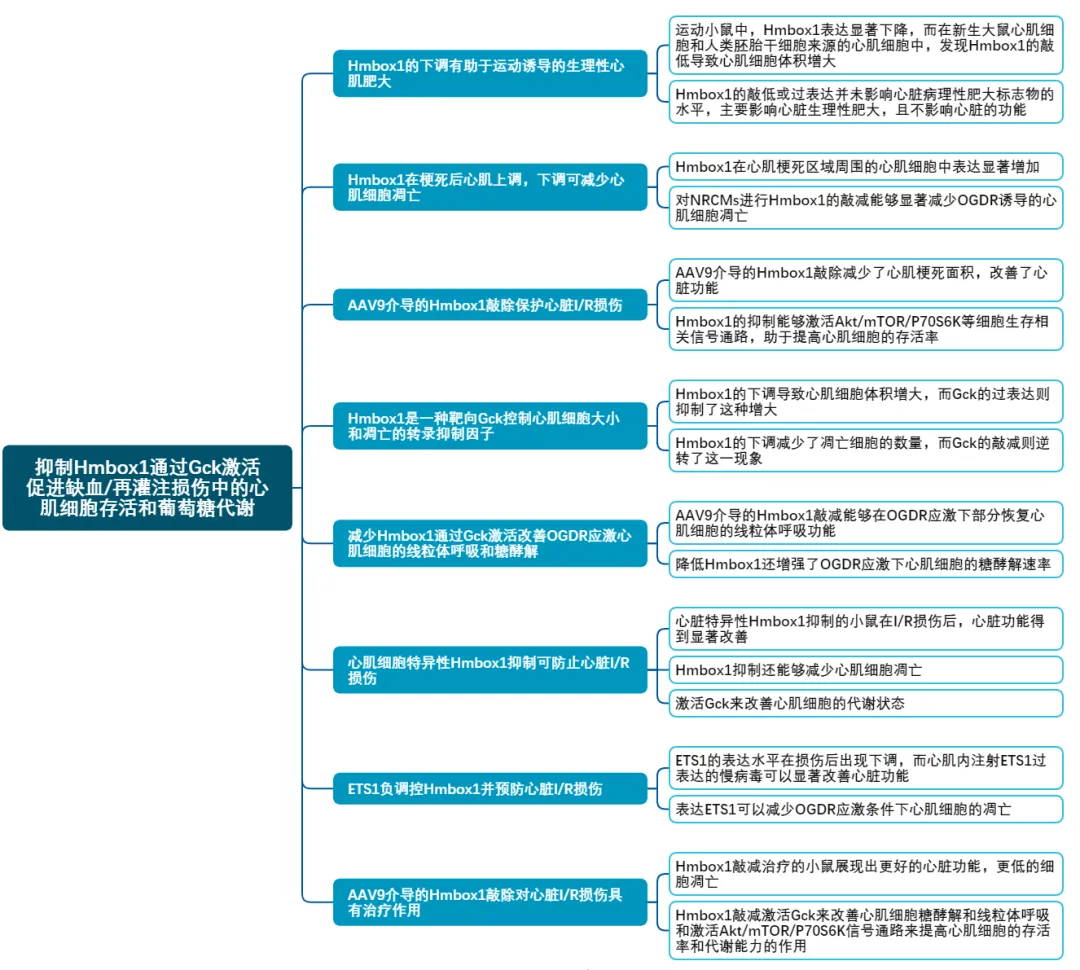
研究技术路线图
01Hmbox1在生理性心脏生长中的作用
①在进行为期四周游泳训练的小鼠心脏组织中,Hmbox1的表达水平显著下降。且实验显示,Hmbox1的表达不影响心肌细胞的增殖能力。
②研究显示,Hmbox1的敲低或过表达并未影响心脏病理性肥大标志物的水平,主要影响心脏生理性肥大,且不影响心脏的功能。此外,Hmbox1在心肌细胞中的表达水平高于心脏成纤维细胞。
③研究发现,在心肌梗死患者的心脏组织和模拟心脏I/R损伤的小鼠模型中,Hmbox1的表达水平显著上调。
④通过在体外模拟心脏I/R损伤的OGDR(氧气和葡萄糖剥夺及再灌注)模型中,对NRCMs进行Hmbox1的敲减能够显著减少OGDR诱导的心肌细胞凋亡,而过表达Hmbox1则加剧了凋亡。在人类胚胎干细胞来源的心肌细胞中也有此发现。
02Hmbox1在心脏I/R损伤中的保护作用
①通过结扎和释放小鼠冠状动脉的方法建立心脏I/R损伤模型,并利用AAV9病毒载体,携带Hmbox1 shRNA尾静脉注射到小鼠体内以降低心肌细胞中的Hmbox1表达。实验结果显示,与对照组相比,该模型的心肌梗死面积显著减少,且心脏收缩和舒张功能得到显著改善,心脏恢复更好。长期观察发现,该模型小鼠心脏纤维化程度降低,心脏结构和功能得到更好的保护。
②分子机制研究表明,Hmbox1的抑制能够激活Akt/mTOR/P70S6K等细胞生存相关信号通路,这些信号通路的激活有助于提高心肌细胞的存活率。
③通过RNA-seq分析发现,I/R损伤模型中,Hmbox1的下调与Gck基因表达的上调有关。研究显示Hmbox1的下调导致心肌细胞体积增大,而Gck的过表达则抑制了这种增大。而在OGDR诱导的心肌细胞凋亡模型中,Hmbox1的下调减少了凋亡细胞的数量,而Gck的敲减则逆转了这一现象。表明,Hmbox1的抑制不仅通过Gck促进心肌细胞的生理性肥大,还通过改善能量代谢和减少凋亡来保护心脏免受I/R损伤。
④在OGDR模型中,心肌细胞会经历氧气和葡萄糖的剥夺后进行灌注,该过程会导致线粒体受损和能量代谢障碍。而AAV9介导的Hmbox1敲减能够在OGDR应激下部分恢复心肌细胞的线粒体呼吸功能。具体表现为提高氧气消耗率、基础呼吸率、最大呼吸率和备用呼吸能力。同时降低Hmbox1还增强了OGDR应激下心肌细胞的糖酵解速率。
03Hmbox1的特异性抑制与治疗潜力
①通过基因敲除技术,在心肌细胞中特异性地敲除Hmbox1基因的小鼠模型显示,在I/R损伤后,心脏的收缩和舒张功能得到了显著改善,心脏结构更加完整,心肌细胞凋亡减少,Bax/Bcl2比例和caspase3活性降低。此外,除凋亡途径外,还通过激活Gck来改善心肌细胞的代谢状态。且Hmbox1抑制能够激活Akt/mTOR/P70S6K等细胞生存和代谢相关的信号通路,来提高心肌细胞的存活率和代谢能力。
②在心脏I/R损伤的动物模型中,ETS1的表达水平在损伤后出现下调,而通过心肌内注射ETS1过表达的慢病毒,可以显著改善心脏的收缩功能和减少心脏重塑。此外,ETS1的过表达也降低了Hmbox1的表达,改善了心肌细胞的代谢状态和减少心肌细胞凋亡。
③在AAV9介导的Hmbox1敲减的I/R损伤模型中,Hmbox1敲减治疗的小鼠同样展现出更好的心脏功能,更低的细胞凋亡,激活Gck来改善心肌细胞糖酵解和线粒体呼吸和激活Akt/mTOR/P70S6K信号通路来提高心肌细胞的存活率和代谢能力的作用。
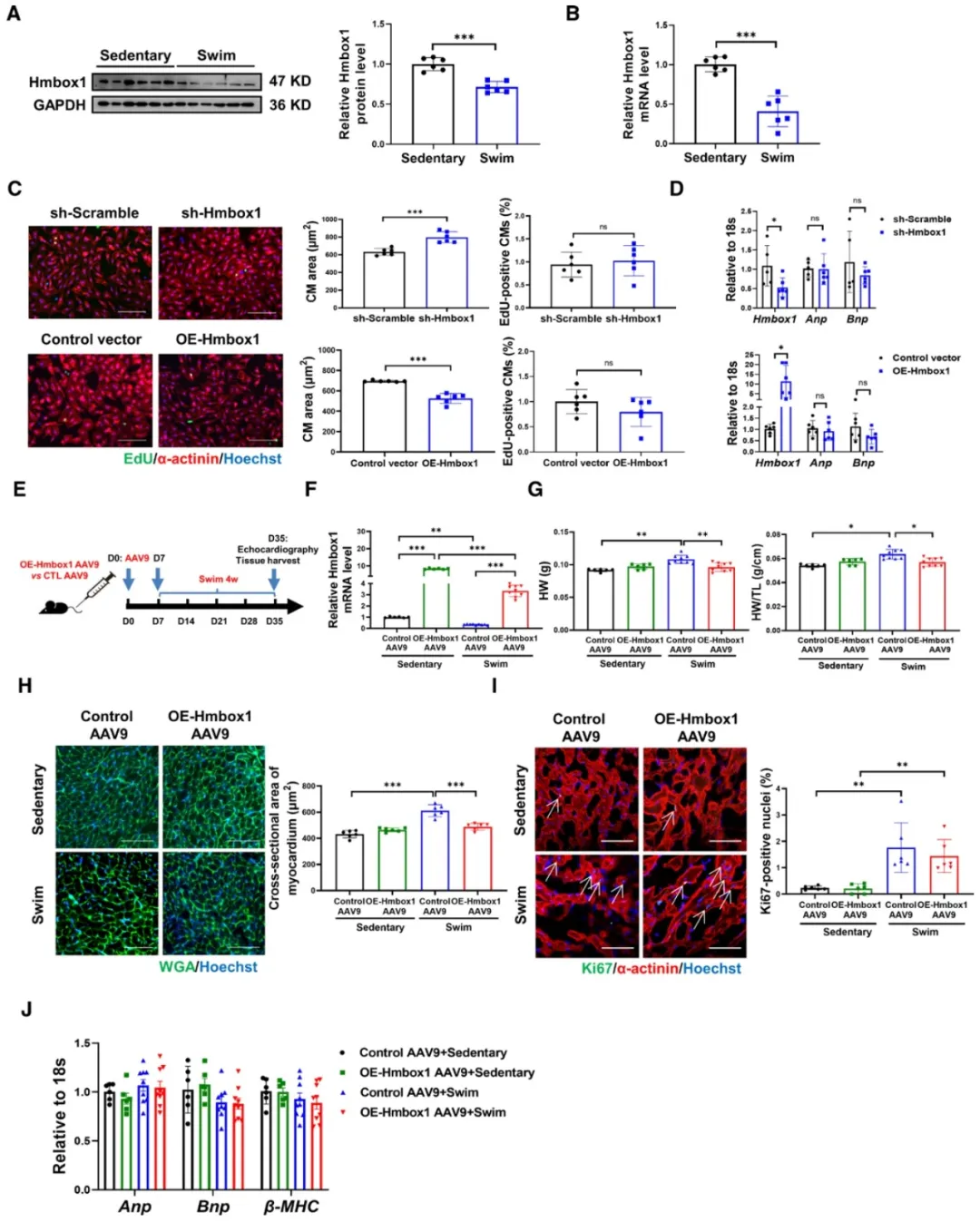
图1. Hmbox1下调是运动诱导的生理性心脏肥大所必需的
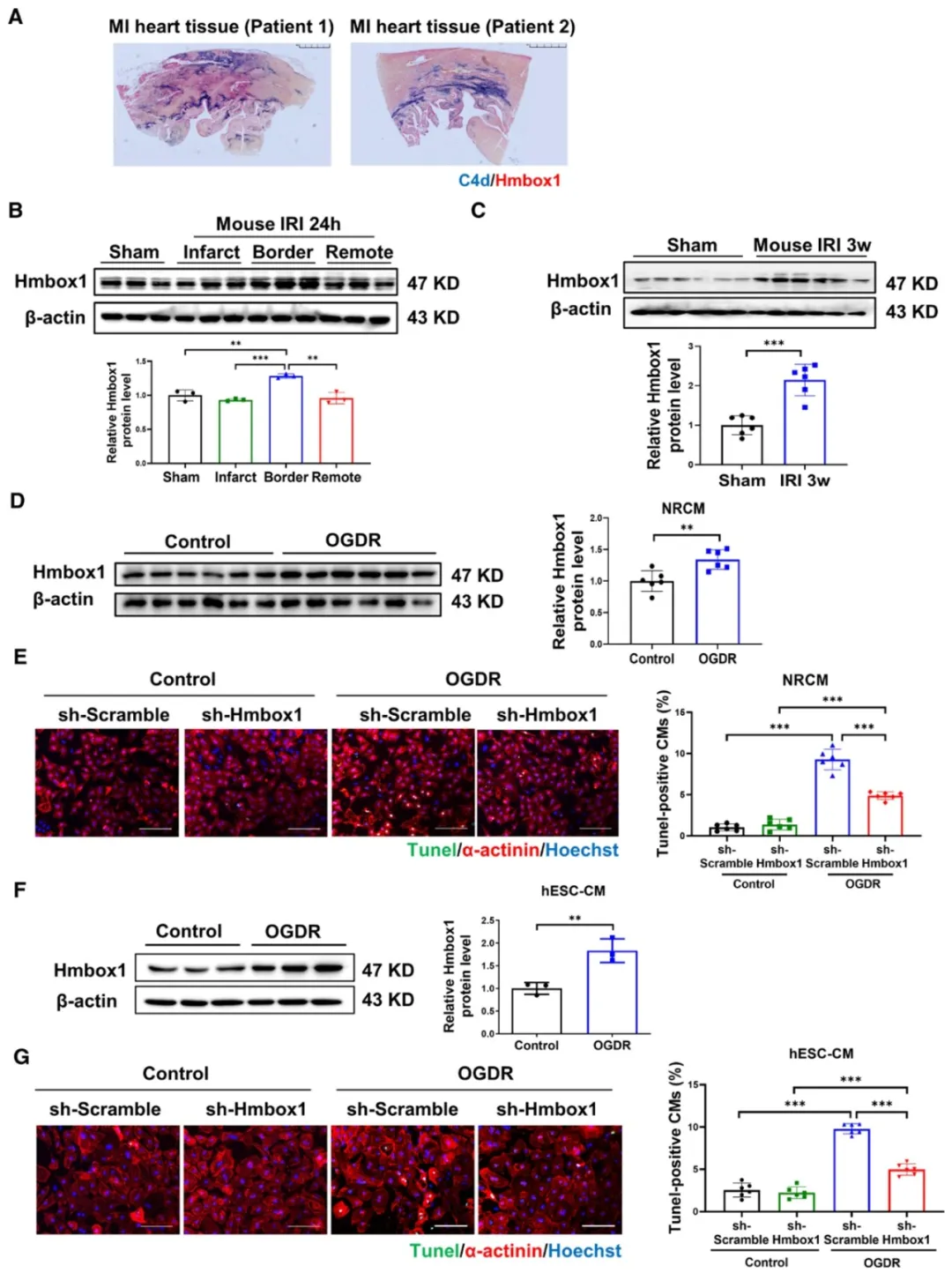
图2. Hmbox1在心肌梗死后心肌中上调,且Hmbox1的下调抑制心肌细胞凋亡
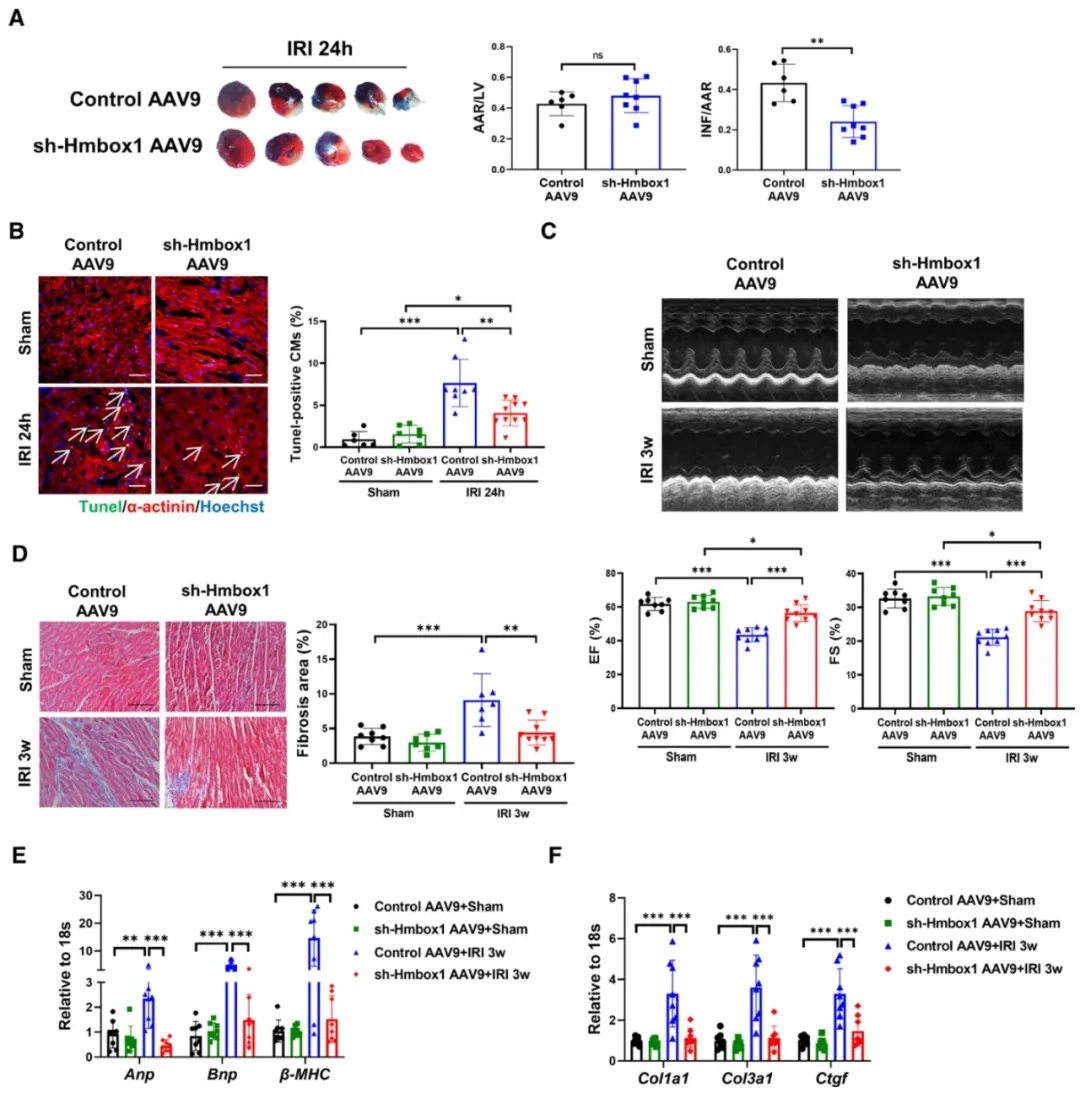
图3. AAV9介导的Hmbox1下调保护心脏免受缺血/再灌注损伤
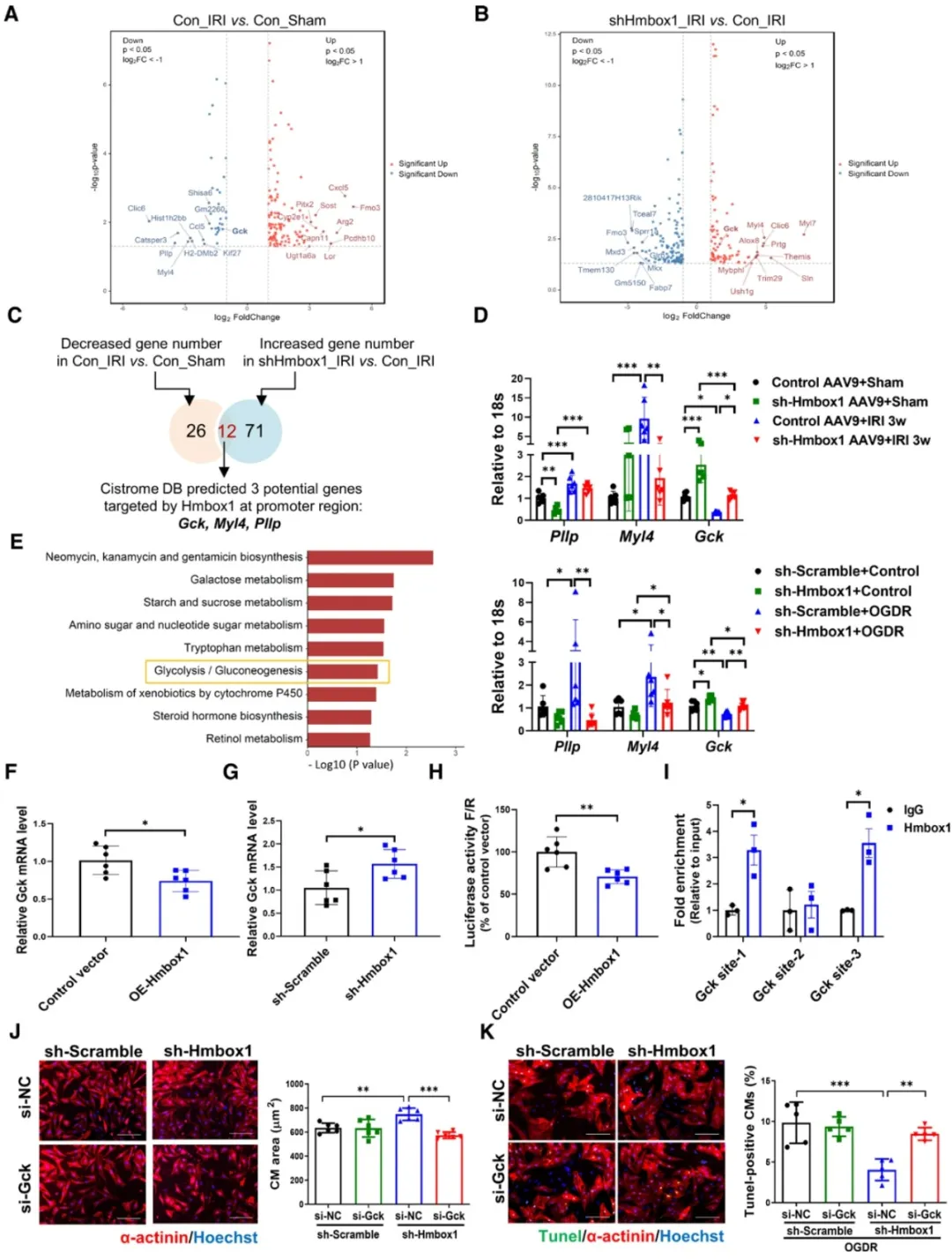
图4. Hmbox1通过糖激酶Gck发挥作用
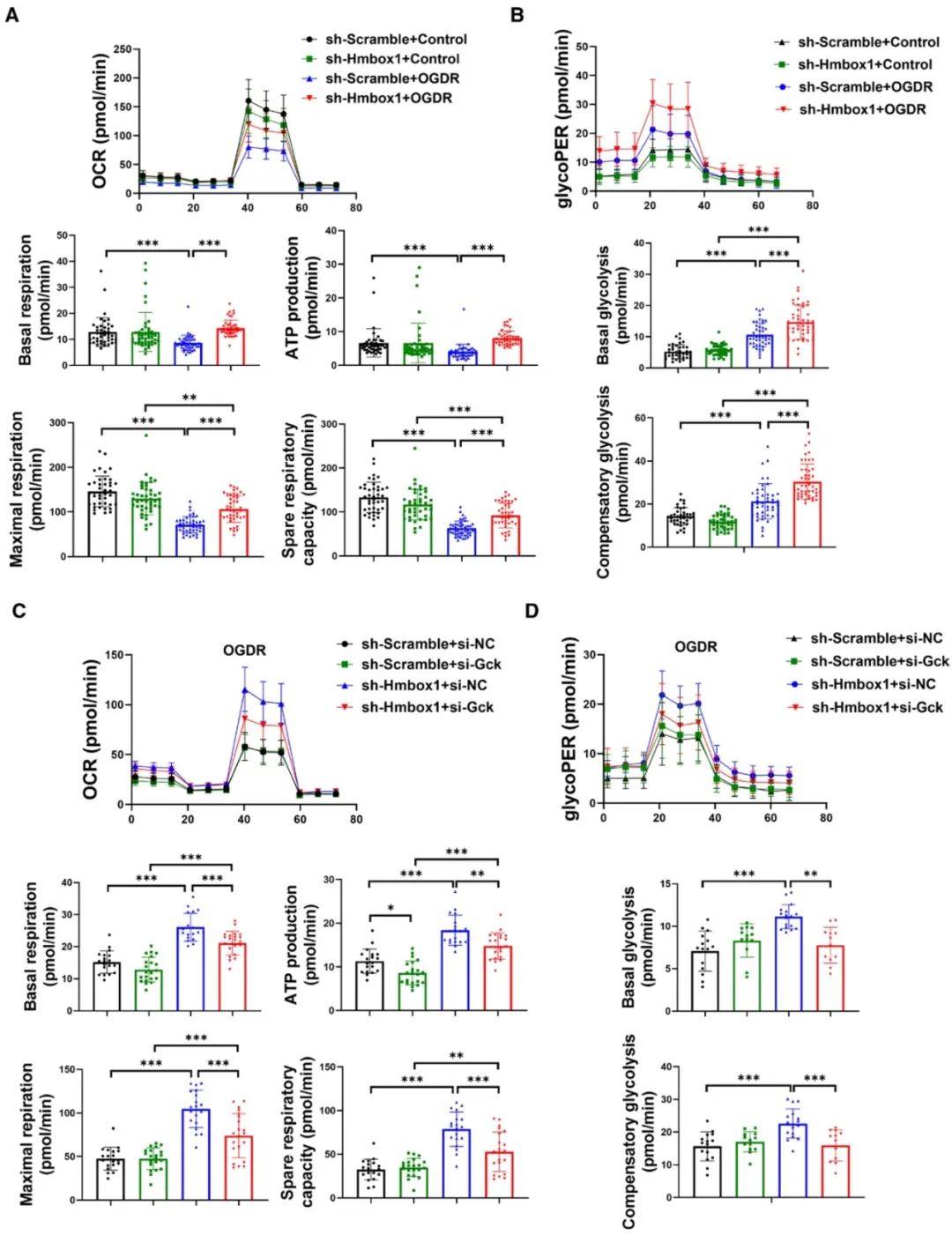
图5. 抑制Hmbox1通过激活糖激酶Gck改善OGDR应激心肌细胞的线粒体呼吸和糖酵解
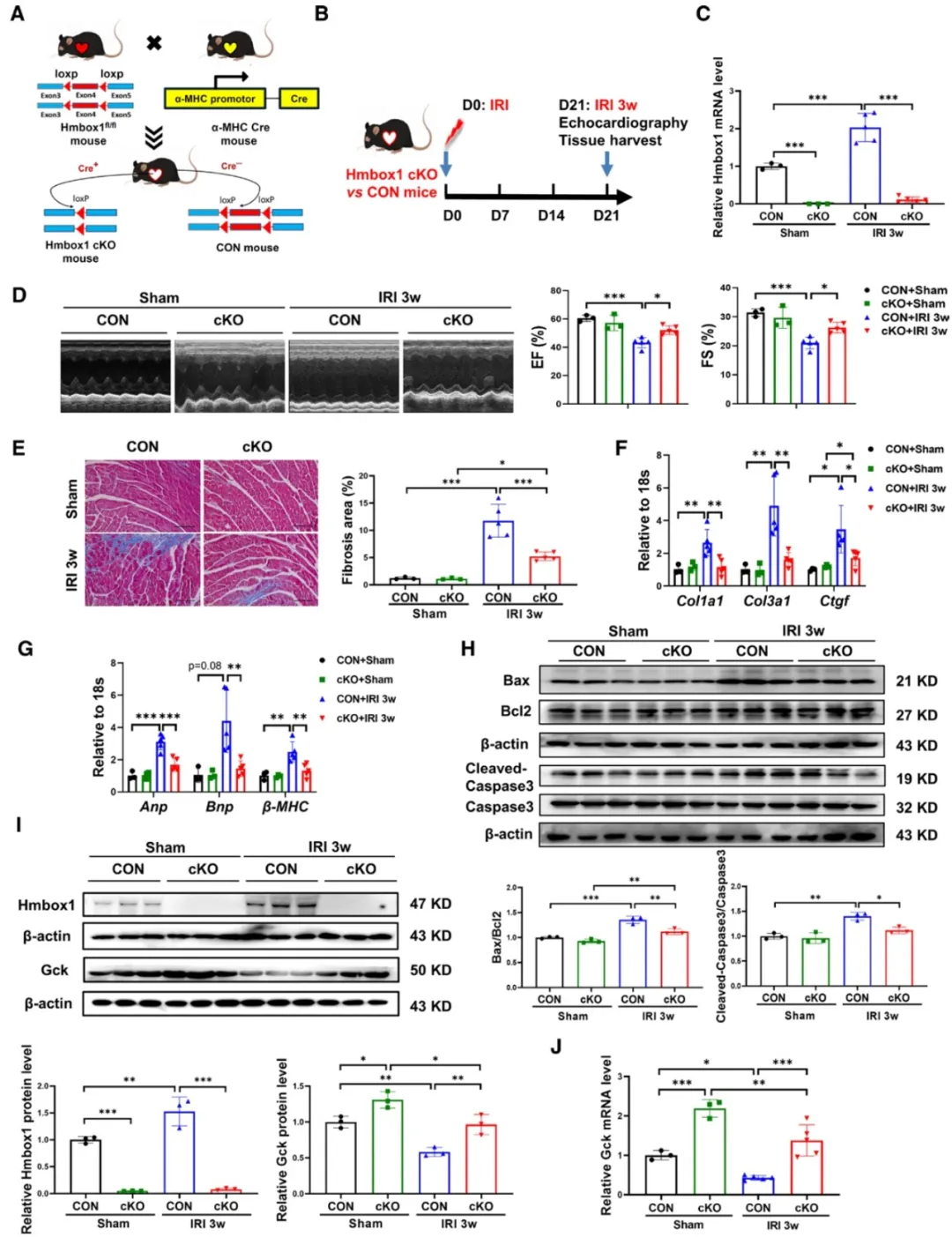
图6. 心肌细胞特异性Hmbox1敲除保护心脏免受I/R损伤
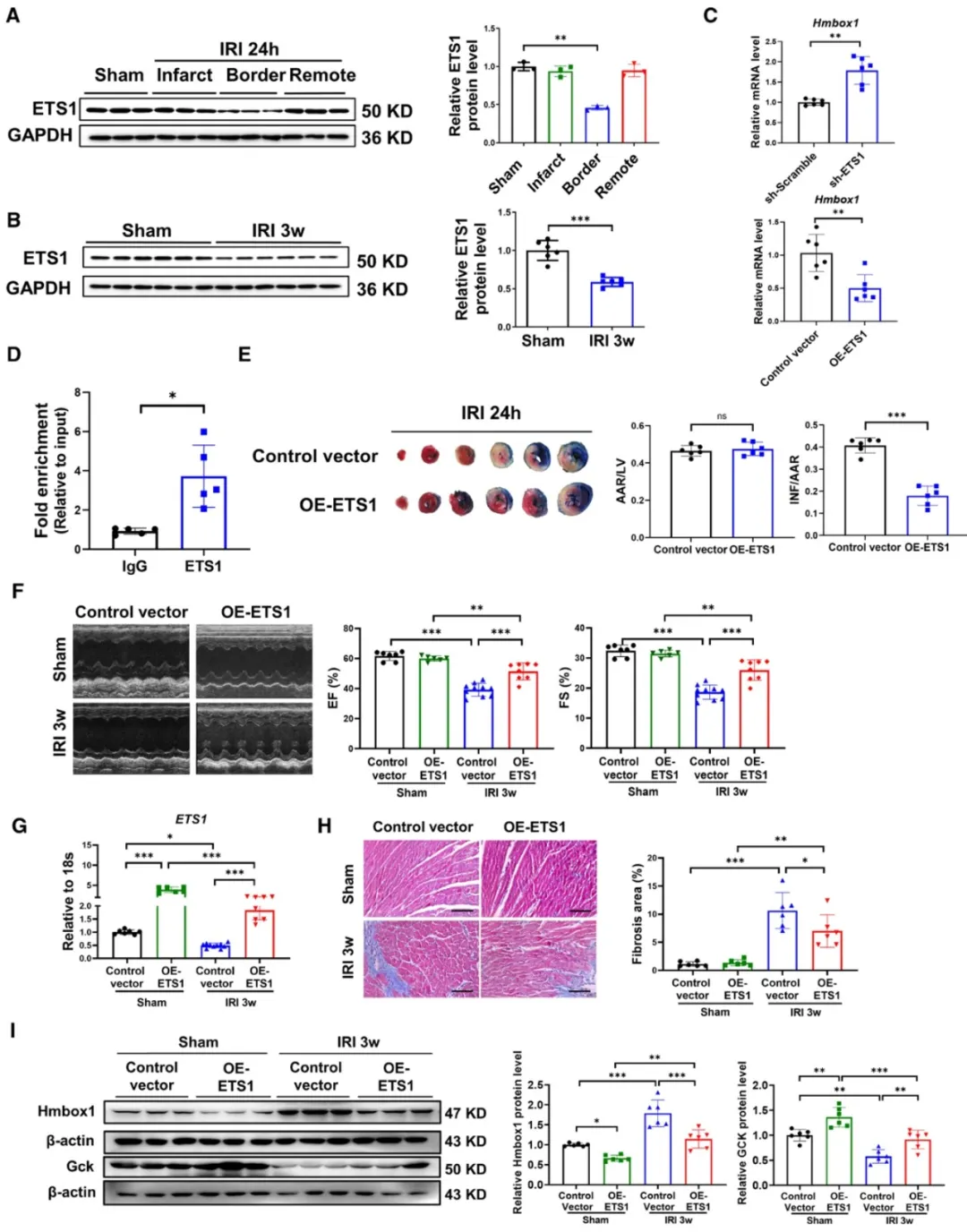
图7. 心肌细胞特异性Hmbox1敲除保护心脏免受I/R损伤
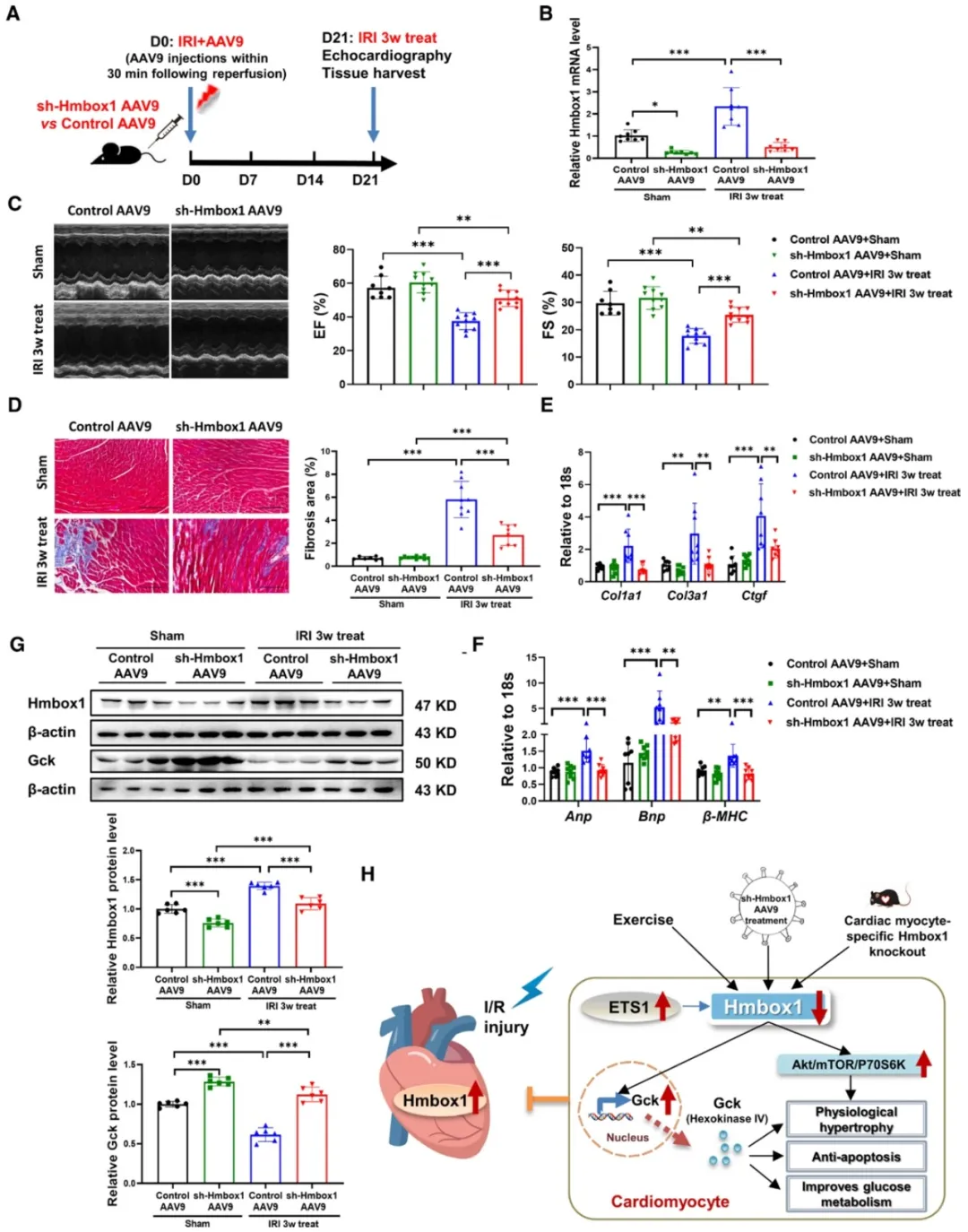
图8.AAV9治疗介导的Hmbox1敲除减轻心脏I/R损伤
结论与讨论
本研究揭示了Hmbox1在心脏生理和病理过程中的关键作用。通过在小鼠模型中抑制Hmbox1,研究显示能促进心肌细胞的存活,改善心脏的糖代谢,并通过激活Gck减少心肌细胞凋亡。此外,ETS1作为Hmbox1的上游负向调节因子,其过表达也显示出对心脏I/R损伤的保护作用。
在未,应进一步关注Hmbox1抑制剂或Gck激活剂的开发,并评估其在心脏疾病治疗中的安全性和有效性。此外,探索其他可能的上游调节因子和信号通路,以全面理解Hmbox1在心脏疾病中的作用机制。
















 {{item.name}}会员
{{item.name}}会员
