北京协和医学院突破性研究:抑制RCAN1可减轻心肌脂质积累和线粒体分裂,为糖尿病心肌病治疗提供新策略
Highlights
1. 糖尿病会促进心脏移植后的非糖尿病性心力衰竭。
2. 酰基辅酶A的增加是糖尿病心肌病的代谢标志。
3. 敲低RCAN1 改善了db/db小鼠的心脏功能和结构。
4. RCAN1-p-Drp1 Ser616轴导致心肌细胞线粒体功能障碍。
近日,“Metabolism”(IF=10.8)上发表了一篇题为“Suppression of RCAN1 alleviated lipid accumulation and mitochondrial fission in diabetic cardiomyopathy”的文章。这篇文章深入探讨了糖尿病心肌病(DbCM)的代谢特征和分子机制,并探索了RCAN1作为治疗靶点的潜力。

研究背景介绍
糖尿病心肌病(DbCM)是糖尿病患者特有的心肌疾病,表现为心肌结构和功能障碍,如心脏肥大和纤维化,以及收缩和舒张功能异常。
线粒体分裂是线粒体动态过程中的一种形态变化,涉及线粒体网络的分裂,与能量代谢、细胞死亡和疾病发展等过程密切相关。
RCAN1是一种调节钙调磷酸酶活性的蛋白,与多种细胞功能和病理过程相关,包括心脏疾病、炎症和细胞应激反应。
长链酰基辅酶A(acyl-CoAs)是脂肪酸代谢的关键中间体,参与脂肪酸的氧化过程。在DbCM中,其水平的变化与心肌细胞的脂质积累和能量代谢紊乱有关
研究思路分析
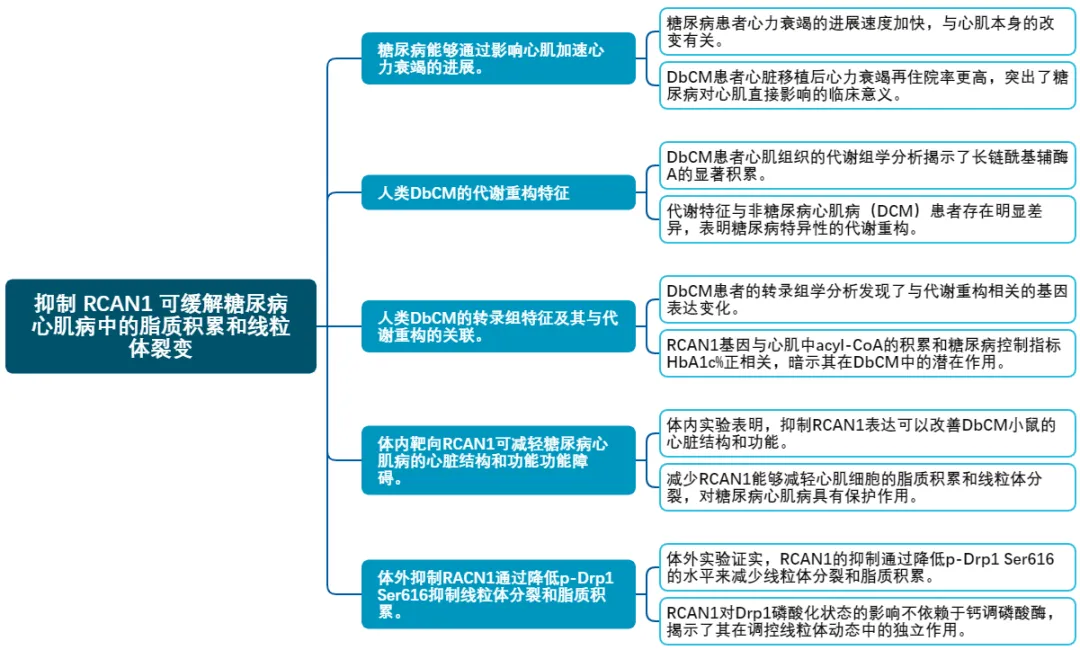
研究技术路线图
01糖尿病对心力衰竭进展的影响
①通过年龄、性别、体重指数对DbCM患者和非糖尿病性扩张型心肌病(DCM)患者进行倾向评分匹配后,发现DbCM患者在心血管症状发展为心力衰竭(HF)的速度更快,且心脏移植(HTx)的需求也较高。且DbCM患者在心脏移植后的再住院率更高。
②通过心肌组织的显微和超微结构实验,发现DbCM患者的心肌中脂质积累显著增加,且线粒体分裂活动异常增强。
02DbCM的代谢重构特征
①靶向代谢组学分析显示,HF组(DbCM和非糖尿病性DCM)与非HF组(HC)之间存在明显的代谢差异。在检测到的102种代谢物中,有16种在DbCM与非糖尿病性DCM之间存在显著差异,尤其是acyl-CoA的浓度在DbCM中增加。表明,糖尿病心肌在HF过程中的代谢紊乱与非糖尿病心肌不同,并与DbCM的疾病进展相关。
②RNA测序发现,处于HF的终末期的DbCM与非糖尿病性DCM在转录组层面上存在显著差异。DbCM中下调的基因数量远多于上调的基因,这些下调的基因主要与ATP合成、电子传递链和氧化磷酸化相关。WGCNA分析发现与acyl-CoA浓度正相关的基因模块,并在该模块中鉴定了RCAN1作为可能与acyl-CoA积累相关的基因。
03RCAN1作为治疗DbCM的潜在靶点
①通过尾静脉注射AAV9-RCAN1或对照载体到12周龄的db/db或db/m小鼠体内。实验结果显示,RCAN1的抑制可以提高db/db小鼠的存活率。
②在实验的终点,与db/m小鼠相比,28周龄的db/db小鼠显示出收缩功能障碍和结构的改变,而RCAN1的抑制减轻了这些功能和结构的功能障碍,尽管心脏肥大并未得到有效预防。
③O-red染色的结果显示RCAN1的抑制减少了心肌细胞中的脂质积累量。超微结构分析显示,db/db小鼠心脏中线粒体分裂明显,而RCAN1的抑制显著减少了线粒体分裂。
④在H9c2细胞上模拟了高糖和棕榈酸诱导的糖毒性和脂毒性。结果显示,高糖和棕榈酸处理显著增加了脂质积累和心衰标志物ANP和BNP的mRNA表达,而RCAN1敲减显著减少了这些变化。此外,RCAN1敲减还缓解了由高糖和棕榈酸诱导的线粒体功能障碍,包括减少线粒体分裂和氧化应激水平。
⑤进一步研究发现,RCAN1通过影响Drp1的磷酸化状态来调节线粒体分裂,而这种作用可能是通过独立于钙神经素的方式实现的。表明,抑制RCAN1可以缓解DbCM中的结构和功能功能障碍。
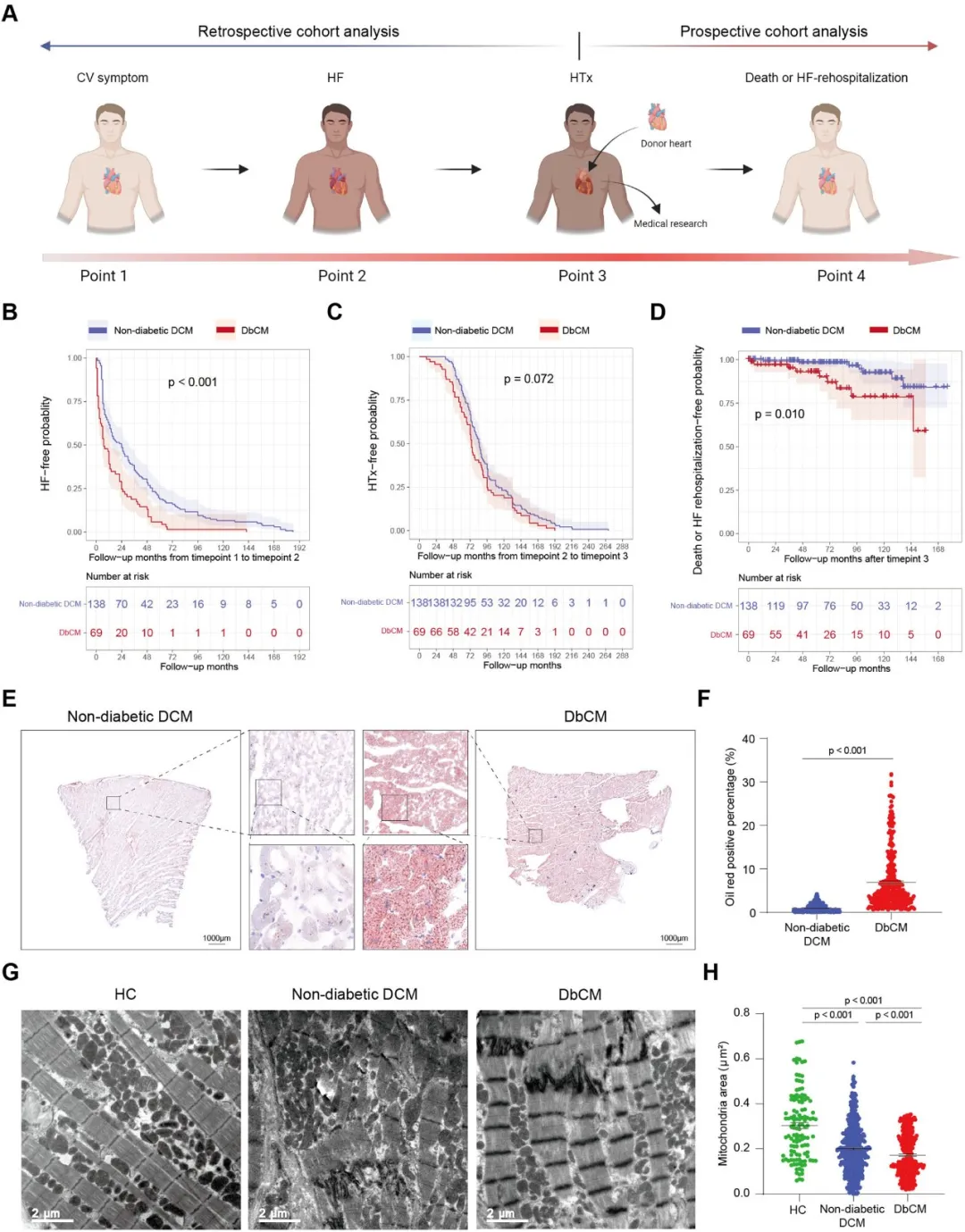
图1. 糖尿病心肌病的临床和病理特征
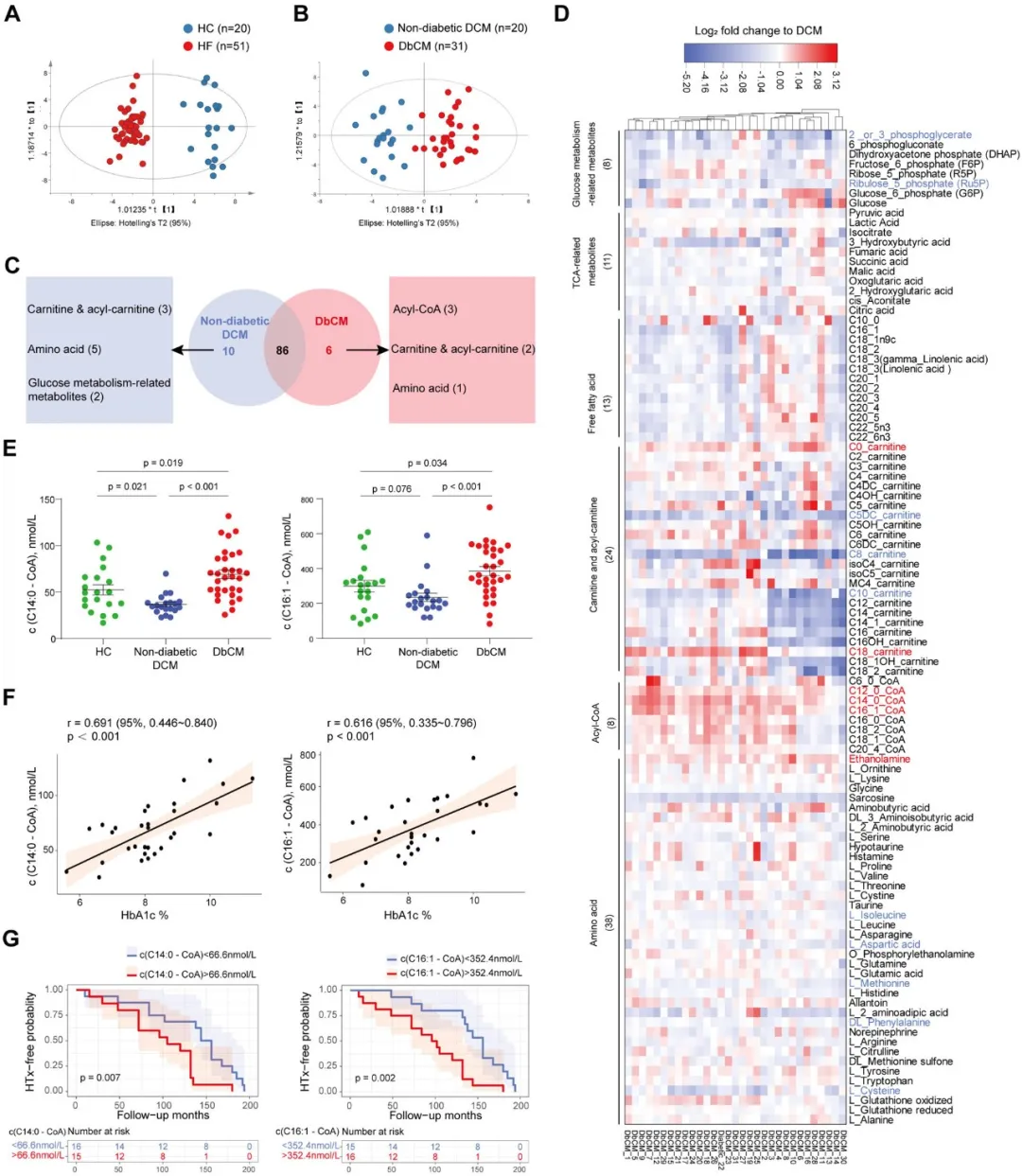
图2. 糖尿病心肌病的代谢特征
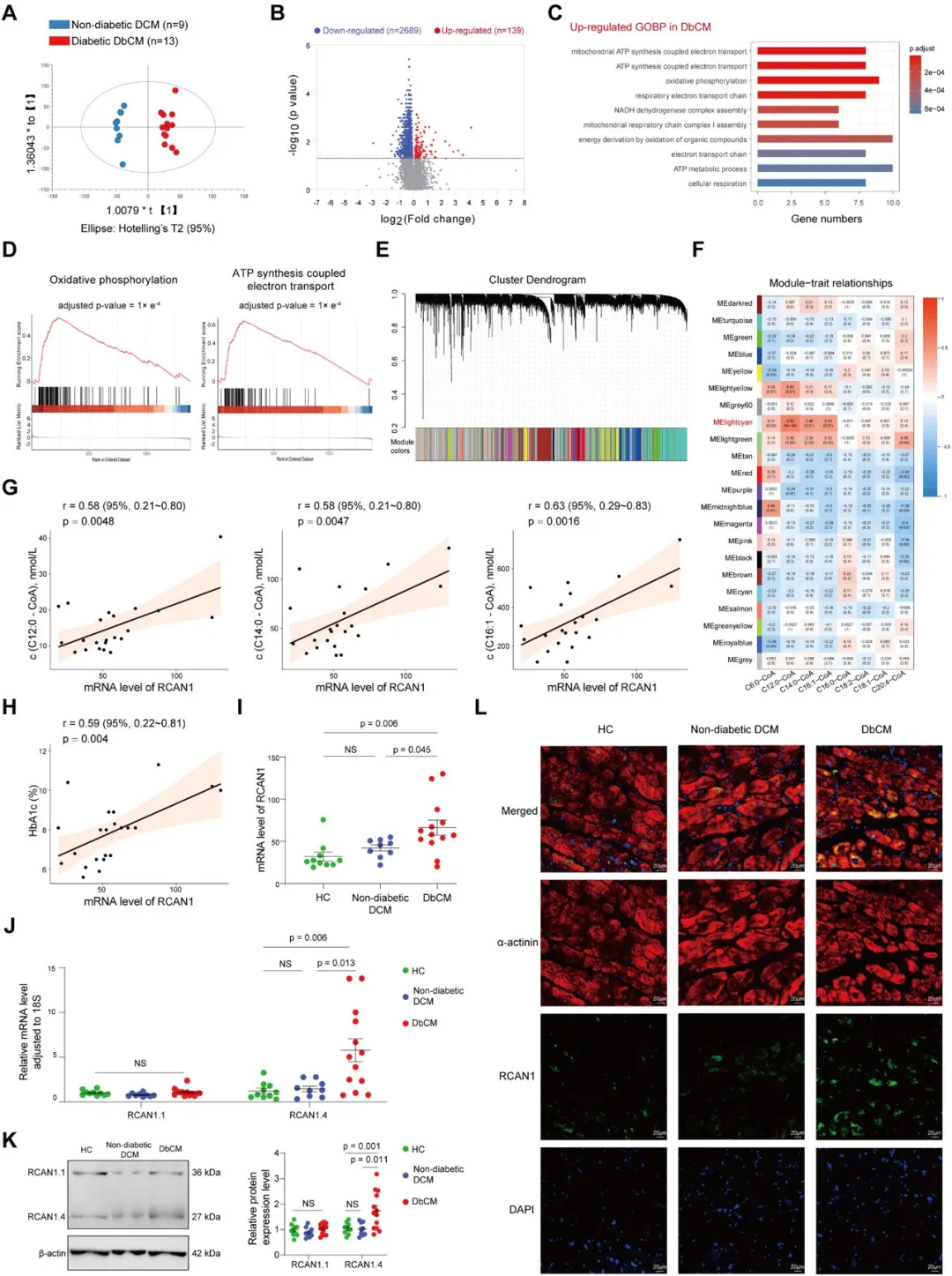
图3. 糖尿病心肌病患者心肌组织的转录组特征及其与代谢组的关联
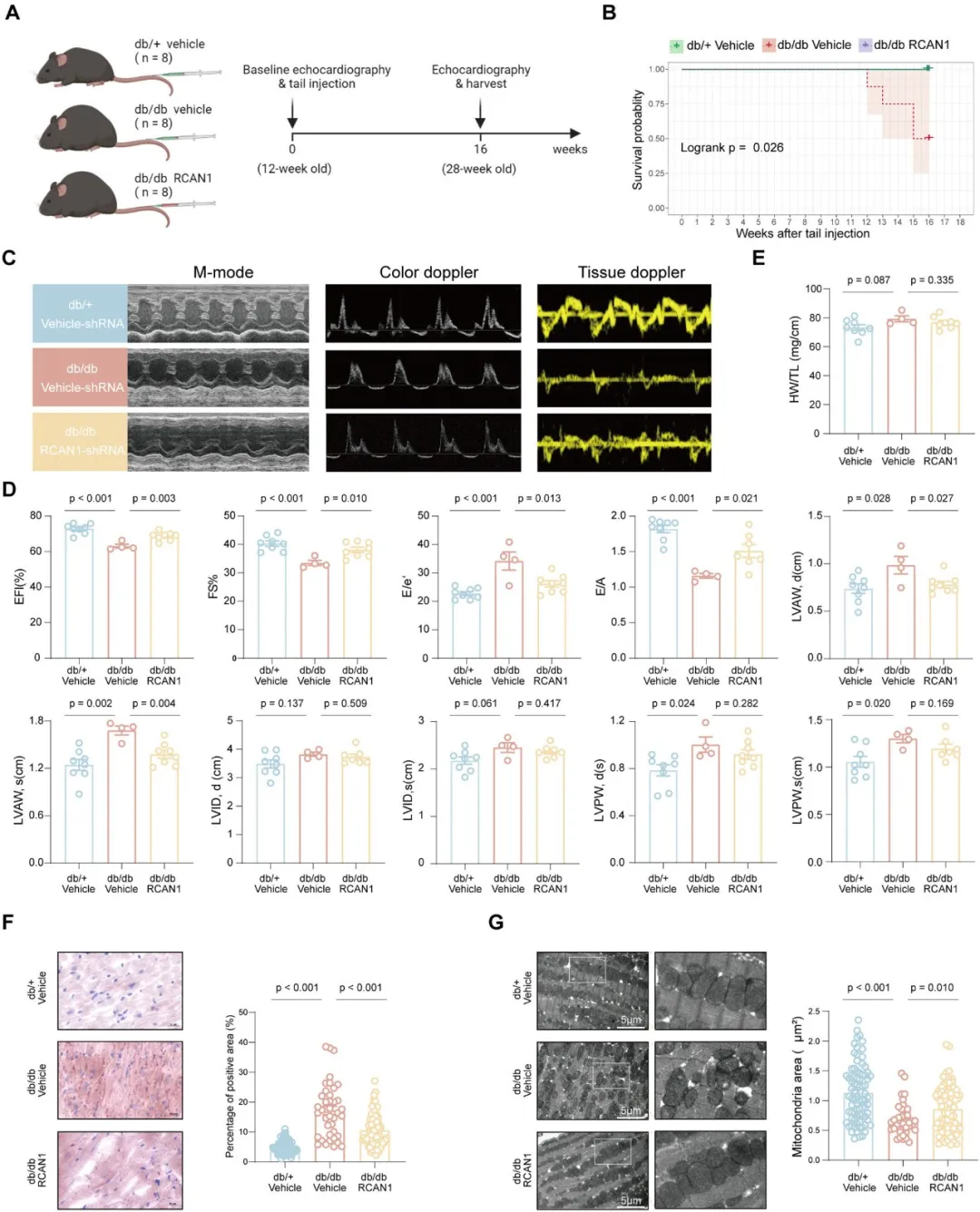
图4. RCAN1的敲低在体内减轻了糖尿病心肌病
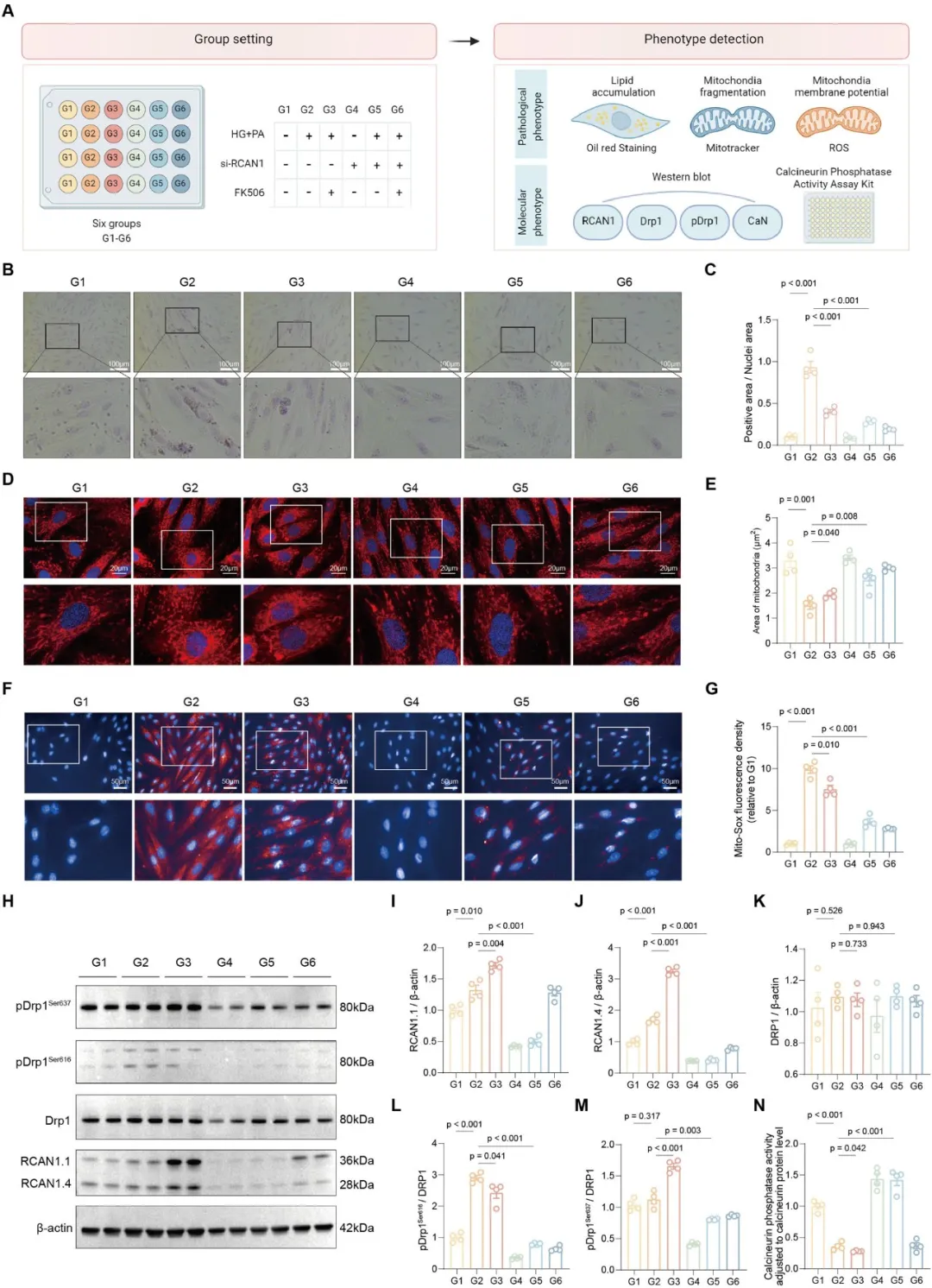
图5. RCAN1的敲低通过RCAN1-p-Drp1 Ser616轴抑制了线粒体分裂和脂质积累
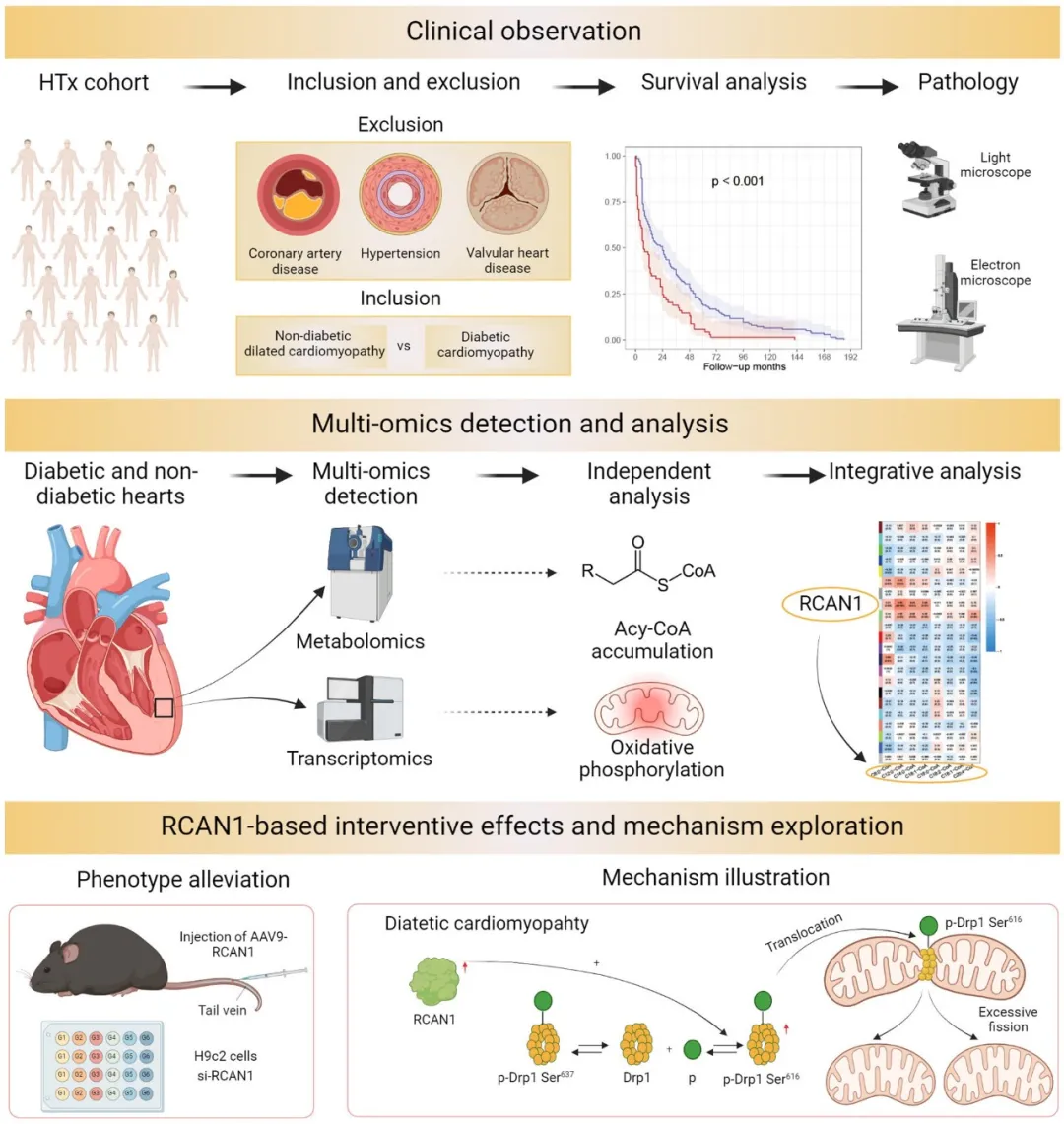
图6. 研究设计的示意图
结论与讨论
研究发现心肌组织中acyl-CoA的积累是DbCM的代谢标志,与疾病快速进展相关。RCAN1的上调与DbCM的代谢异常和心肌细胞的功能障碍有关。体内外实验证明,抑制RCAN1的表达能改善DbCM小鼠的心脏功能和结构,减轻线粒体分裂和脂质积累,表明RCAN1是DbCM治疗的潜在靶点。
然而,尽管RCAN1显示出作为DbCM治疗靶点的潜力,但对其在高糖环境下异常上调的分子机制尚不清楚,需要进一步研究。此外,未来的工作应评估RCAN1基因治疗的长期效果和安全性。研究还应探索其他潜在的治疗靶点,以开发更有效的治疗方法,改善DbCM患者的预后。
















 {{item.name}}会员
{{item.name}}会员
