新发现!川大华西揭示:中性粒细胞ROS对关节炎早期促病与晚期缓病的机制
Highlights
1. 中性粒细胞的ROS在关节炎早期促进疾病,在晚期减轻症状。
2. 特定中性粒细胞亚群在免疫启动期间激活,与疾病发展相关。
3. 中性粒细胞的代谢变化增强了炎症反应,可能影响关节炎进程。
近日,“Redox Biology”(IF=10.7)上发表了一篇题为“Neutrophils with low production of reactive oxygen species are activated during immune priming and promote development of arthritis”的文章。这篇文章研究低产生活性氧的中性粒细胞在免疫启动及关节炎发展中的作用,揭示发病机制及治疗靶点。

研究背景介绍
中性粒细胞是人体循环白细胞中数量最多的一种,具有强大的先天免疫反应能力。
类风湿性关节炎(RA)是一种慢性炎症性自身免疫疾病,以滑膜增生、骨破坏和关节畸形为特征。
NADPH氧化酶2(NOX2)是中性粒细胞中产生ROS的主要酶,它由多个亚基组成,其中NCF1是调控ROS水平的关键亚基。
中性粒细胞胞质因子1(NCF1)是NOX2复合体的一个关键亚基,通过调节ROS的生理水平来调控关节炎的发展。
研究思路分析
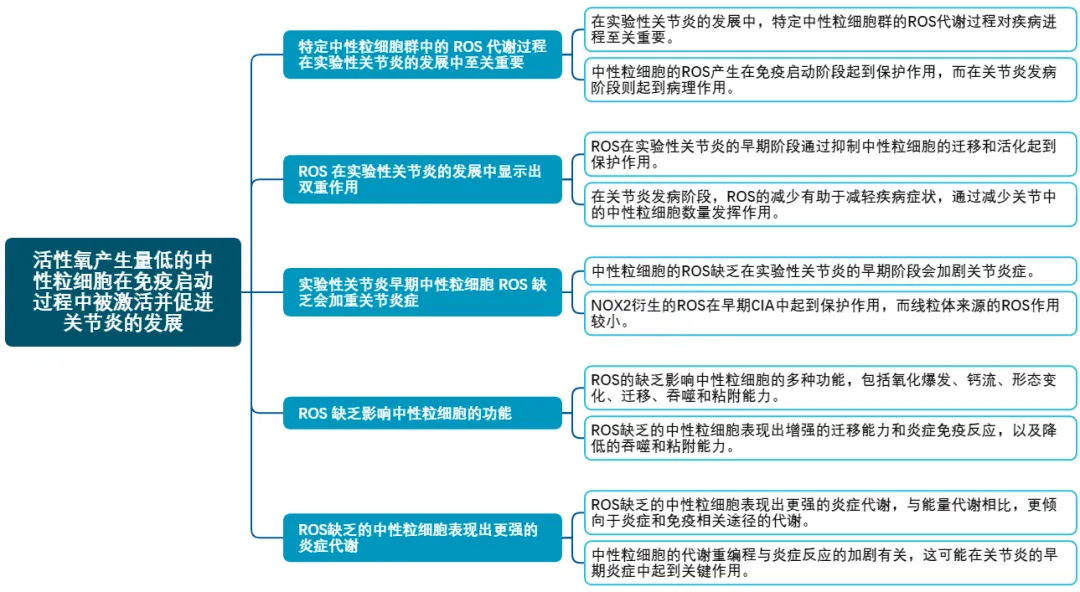
研究技术路线图
01ROS在关节炎中的作用与调节
①通过对关节炎发作期间正常、免疫启动、免疫增强状态下小鼠骨髓细胞进行单细胞RNA测序,发现中性粒细胞在正常组和启动组之间的比例差异显著。在免疫启动阶段,中性粒细胞的特定亚群G4增多,与ROS产生和炎症反应相关。G4亚群高表达Ncf1,表明其在关节炎前期通过吞噬性NADPH氧化酶产生ROS。
②此外,通过使用抗Ly6G抗体耗尽中性粒细胞,再用II型胶原(COL2)免疫,只有耗尽中性粒细胞的小鼠发展出轻度关节炎,这表明中性粒细胞在胶原诱导性关节炎(CIA)早期可防止小鼠发生关节炎。
③为探究NOX2复合体中NCF1衍生的ROS在关节炎不同阶段的作用,使用NOX抑制剂DPI来阻断ROS的产生。研究发现,在免疫启动阶段(D0)开始使用DPI治疗,会导致关节炎的发展,且增加了骨髓过氧化物酶(MPO)活性和骨破坏。而在关节炎发作前(D21)开始治疗,则能减轻关节炎症状。
④研究还发现,DPI治疗能增加血液中的中性粒细胞数量,这些中性粒细胞可能来自骨髓,从而促进了关节炎的早期发作。然而,在关节炎发作后,DPI治疗能减少关节中的中性粒细胞数量,从而减轻关节炎症状。表明,ROS在免疫启动阶段促进关节炎发展,而在关节炎发作阶段则减轻症状,即ROS双向调节关节炎。
02ROS缺乏对中性粒细胞功能的影响
①使用NOX2特异性抑制剂GSK2795039和线粒体ROS抑制剂MitoQ10治疗小鼠,发现抑制NOX2产生的ROS比抑制线粒体ROS更显著地促进了关节炎的发展。此外,还使用了Ncf1基因敲除(Ncf1-/-)小鼠模型,结果显示在免疫启动后,Ncf1-/-小鼠比野生型(WT)小鼠更容易发展成关节炎。
②研究还发现,Ncf1-/-小鼠关节中中性粒细胞和表达CXCR2的细胞水平增加,以及在关节炎发病时血液中性粒细胞的ROS水平升高。同时Ncf1-/-小鼠的中性粒细胞表现出上调的趋化因子受体CXCR1和CXCR2,以及炎症因子的表达。表明,早期实验性关节炎中ROS的缺乏促使中性粒细胞表现出促炎特性,从而促进了关节炎的发展。
③中性粒细胞的生存能力与其氧化爆发活动有关,该活动产生ROS。研究发现,所有ROS抑制剂在约30分钟时对中性粒细胞ROS水平有显著抑制作用,并呈剂量依赖性。ROS抑制剂还能剂量依赖性地降低由PMA或fMLF刺激的中性粒细胞钙流,影响其形态变化和吞噬作用。ROS缺乏的中性粒细胞迁移能力增加,但粘附和吞噬能力降低。
④ROS抑制剂还影响了中性粒细胞趋化因子受体和炎症因子的表达。ROS缺乏的中性粒细胞表现出更长的寿命、更少的凋亡和更低的吞噬能力。此外,ROS的抑制增加了CD4+T细胞、Th1和Th17细胞的比例,这可能促进了关节炎的发展。综上表明,ROS缺乏的中性粒细胞通过减少氧化爆发、钙流和形态变化自我维持,导致中性粒细胞功能转变,从而快速迁移到炎症部位发挥作用。
03ROS缺乏与中性粒细胞的炎症代谢
①为表征ROS调节的中性粒细胞激活相关的代谢变化,研究了WT和Ncf1-/-小鼠的中性粒细胞在有或无PMA和fMLF刺激时的反应。未刺激时,Ncf1-/-和WT中性粒细胞代谢物无差异,PMA刺激后分别在Ncf1-/-和WT中性粒细胞中鉴定出92和61种差异表达代谢物(DEMs),说明Ncf1-/-中性粒细胞有独特代谢组。
②PMA刺激下,Ncf1-/-中性粒细胞代谢途径与WT不同,前者侧重于炎症和免疫相关途径,后者侧重于无炎症的能量代谢和生物降解途径。fMLF刺激的Ncf1-/-中性粒细胞还会上调涉及药物作用的代谢途径。表明ROS缺乏导致中性粒细胞代谢异常,与炎症和免疫激活异常以及能量和药物代谢失衡有关。在免疫启动环境中,ROS缺乏的中性粒细胞从能量代谢和生物降解途径向炎症和免疫代谢途径发生表型转变,从而促进炎症。
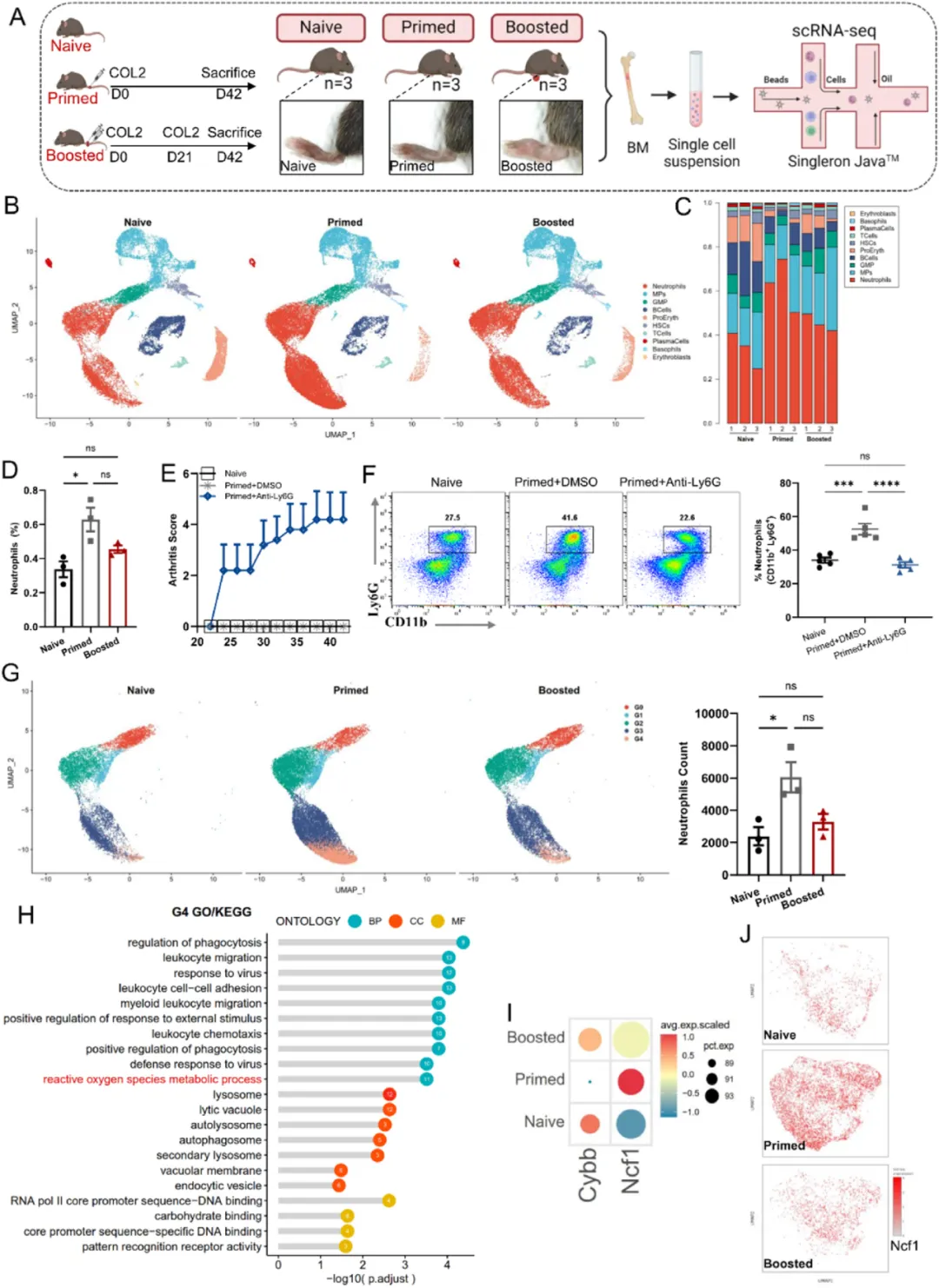
图1. scRNA-seq分析关节炎模型中的骨髓中性粒细胞
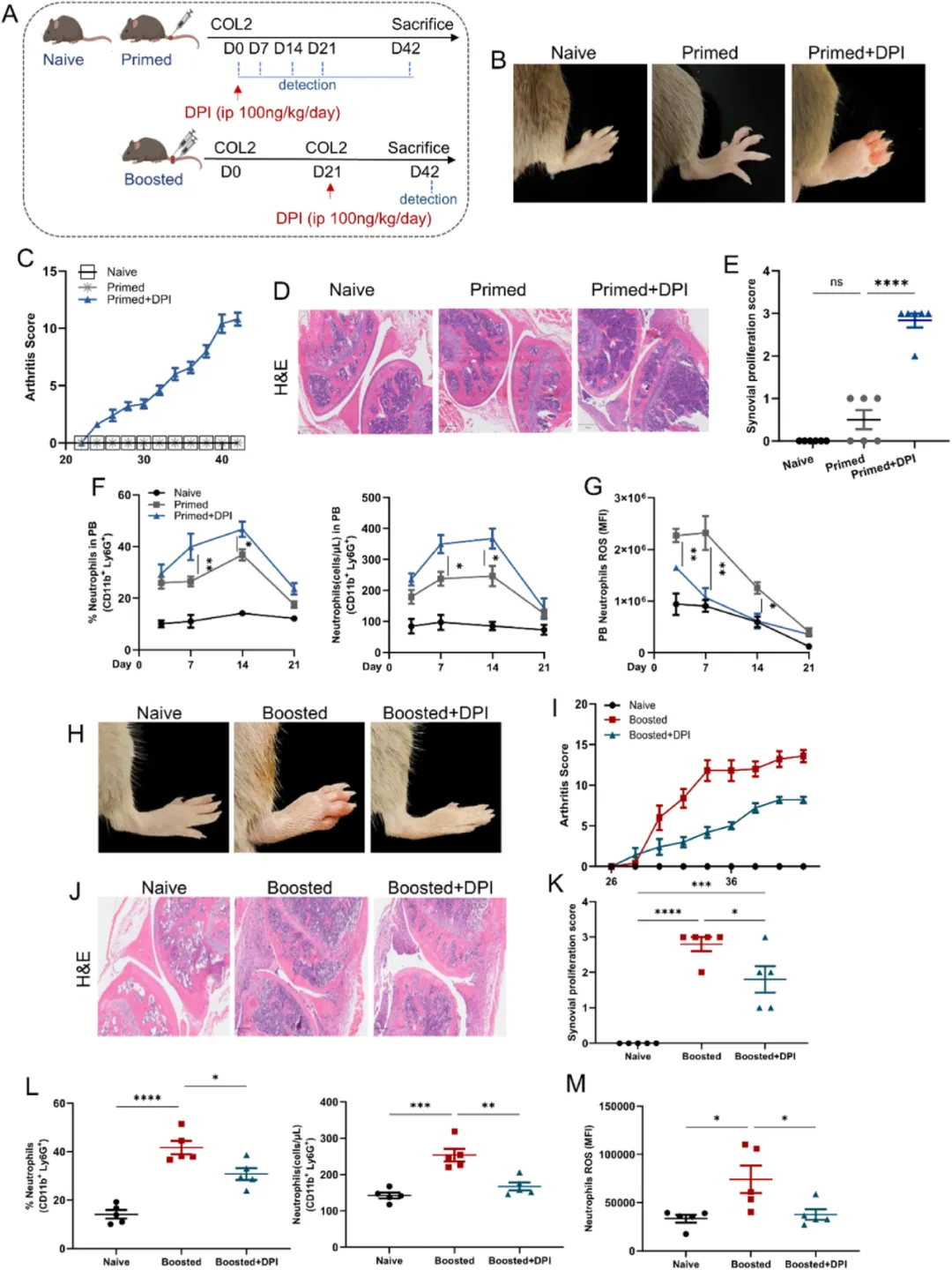
图2.ROS在早期保护和晚期病理发展中发挥双向作用
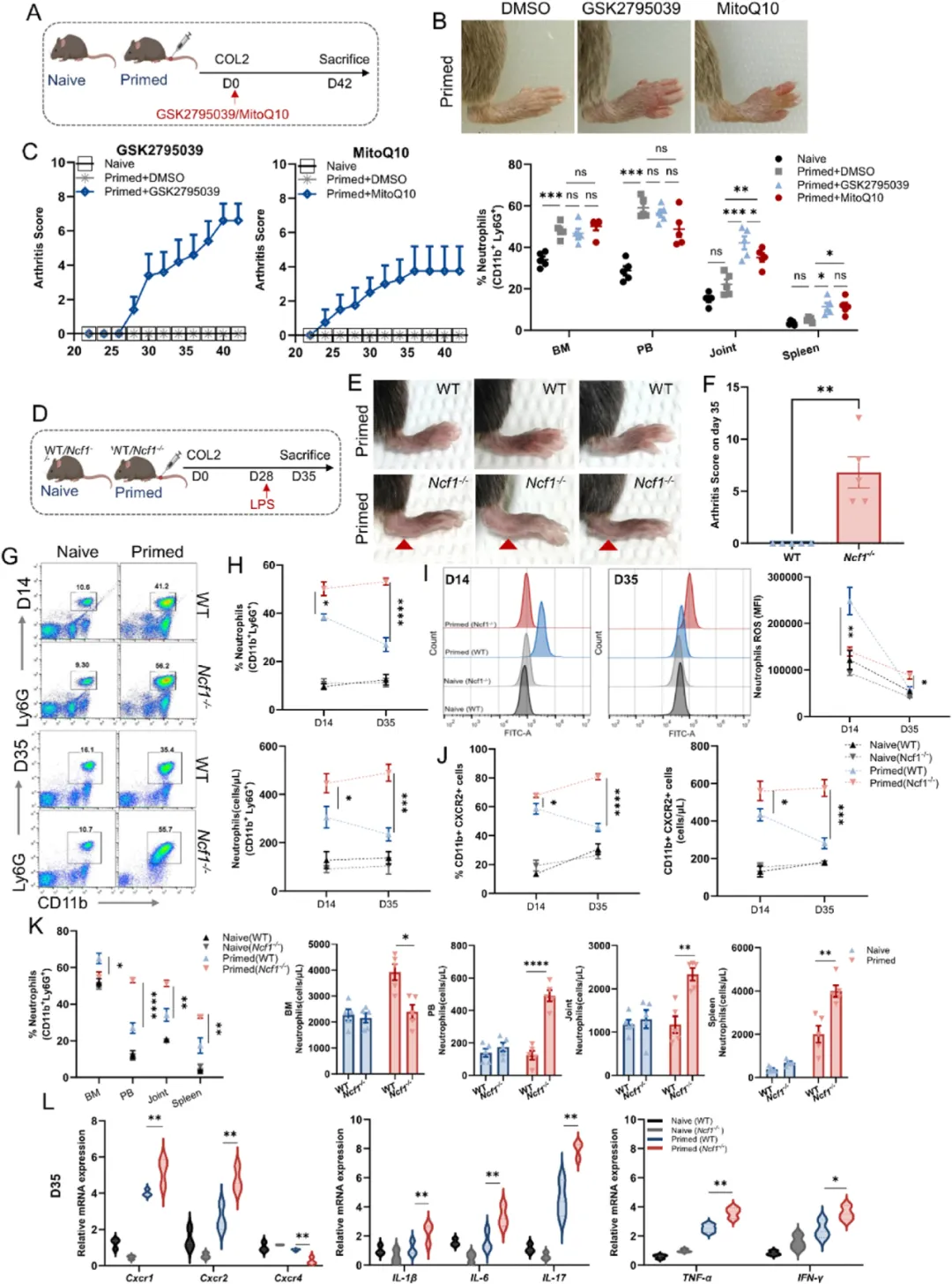
图3. ROS缺乏在实验性关节炎早期阶段通过招募中性粒细胞触发关节炎
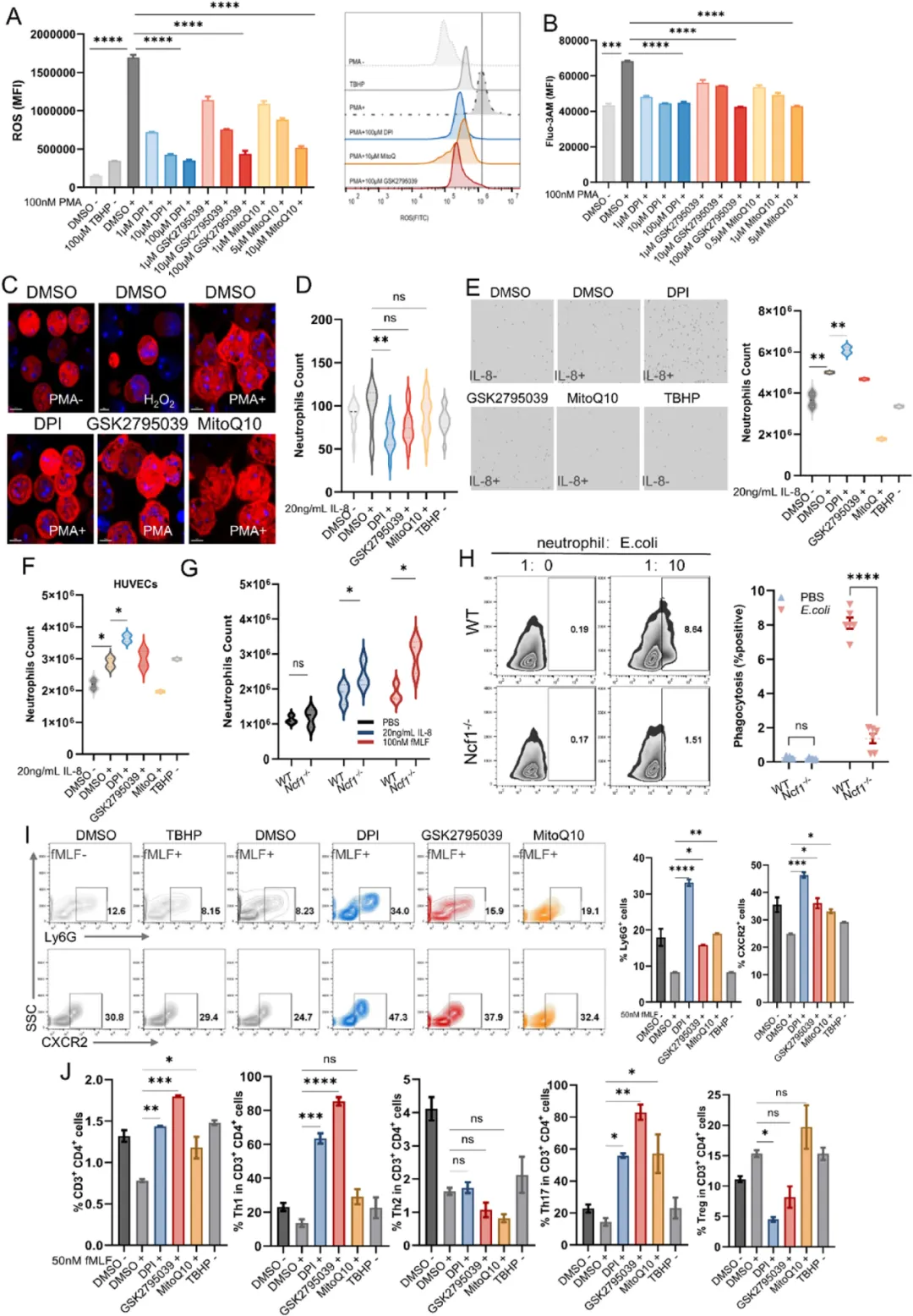
图4. ROS缺乏改变中性粒细胞的功能和炎症表型
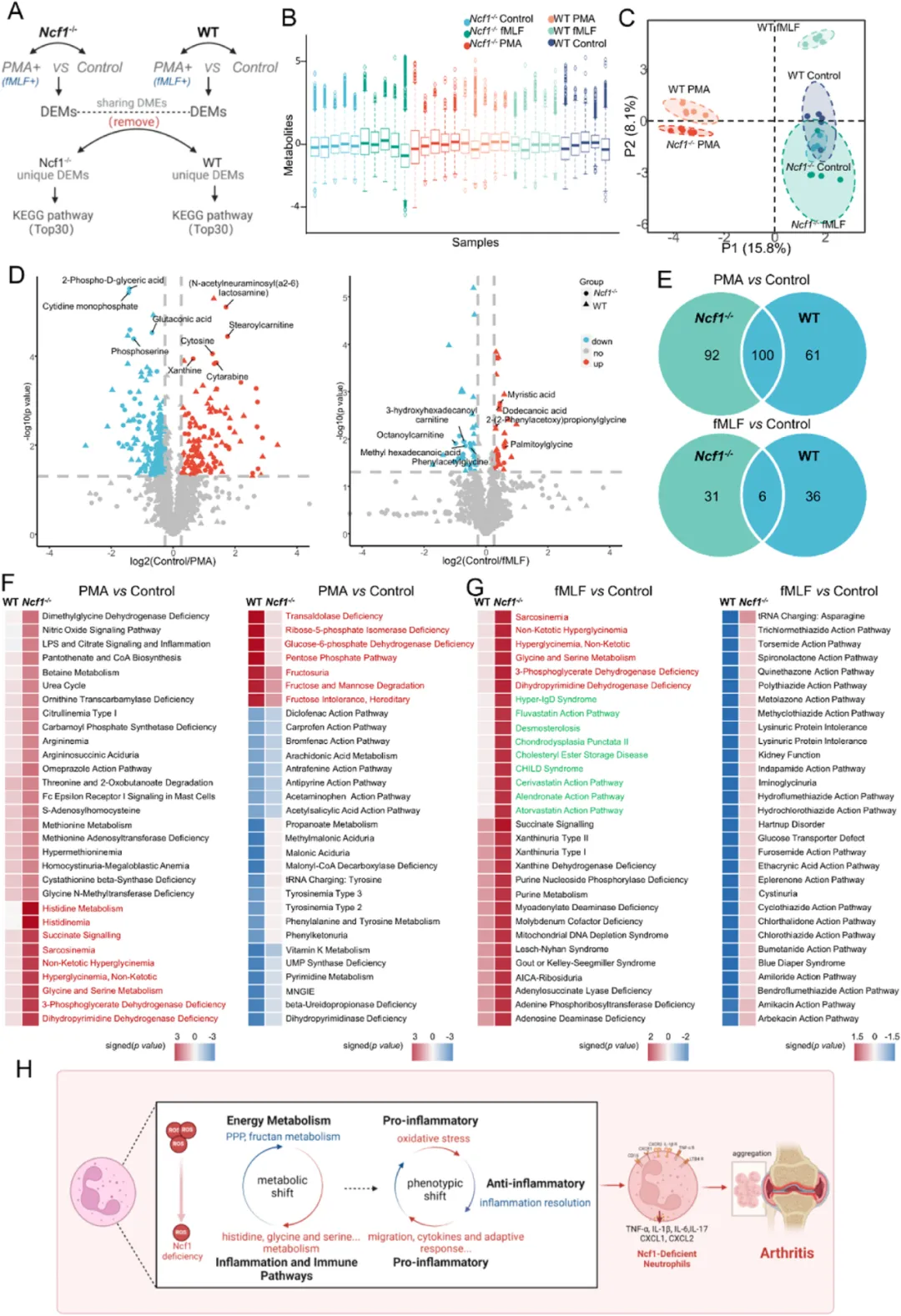
图5. ROS缺乏的中性粒细胞表现出更强大的炎症代谢重编程
结论与讨论
在接受PCI治疗的AMI患者中,血浆RIPK3水平的升高与不良心血管事件的风险增加有关。实验表明,细胞外RIPK3通过与RAGE结合激活CaMKII,进而促进心肌细胞死亡和炎症反应。这些结果揭示了RIPK3作为一个潜在的生物标志物和治疗靶点,用于改善心脏I/R损伤的临床结果。
尽管研究取得了初步成果,但血浆RIPK3作为生物标志物的诊断价值和阈值需要在更大规模的多中心随机临床试验中进一步验证。未来的研究还应包括对不同性别和种族的患者进行研究,以确保结果的普适性。此外,还需要进一步探索RIPK3/RAGE/CaMKII信号通路在其他心脏疾病中的作用,以及开发针对该通路的新型治疗策略。
















 {{item.name}}会员
{{item.name}}会员
