陆军医科大学cell子刊重磅研究:线粒体丝氨酸代谢在造血干细胞铁死亡防御中的关键作用
Highlights
1. HSC是高度依赖外源性丝氨酸的丝氨酸营养缺陷型生物
2. 活性线粒体丝氨酸分解代谢表征和维持HSC
3. 线粒体丝氨酸分解代谢产生NAD(P)H以抑制HSC铁死亡
4. 外源性丝氨酸可保护HSC免受照射诱导的骨髓抑制性损伤
近日,“Cell Stem Cell”(IF=19.8)上发表了一篇题为“Mitochondrial serine catabolism safeguards maintenance of the hematopoietic stem cell pool in homeostasis and injury”的文章。这篇文章探讨了造血干细胞如何通过线粒体丝氨酸代谢来维持自身在稳态和损伤后的存活和功能。

研究背景介绍
造血干细胞(HSCs)是存在于骨髓中的多功能干细胞,具有自我更新和分化成所有类型血细胞的能力,包括红细胞、白细胞和血小板。
丝氨酸代谢是细胞内一种重要的代谢途径,涉及丝氨酸的分解和转化。线粒体丝氨酸代谢特指在线粒体内进行的丝氨酸分解过程,这一过程对于细胞的能量产生和氧化还原平衡具有重要作用。
SHMT2-MTHFD2轴:SHMT2(丝氨酸羟甲基转移酶2)和MTHFD2(甲酰四氢叶酸脱水酶2)是线粒体丝氨酸代谢途径中的关键酶。SHMT2负责将丝氨酸转化为甘氨酸和一碳单位,而MTHFD2则参与将这些一碳单位进一步转化为NAD(P)H,这对于维持细胞的氧化还原平衡至关重要。
研究思路分析
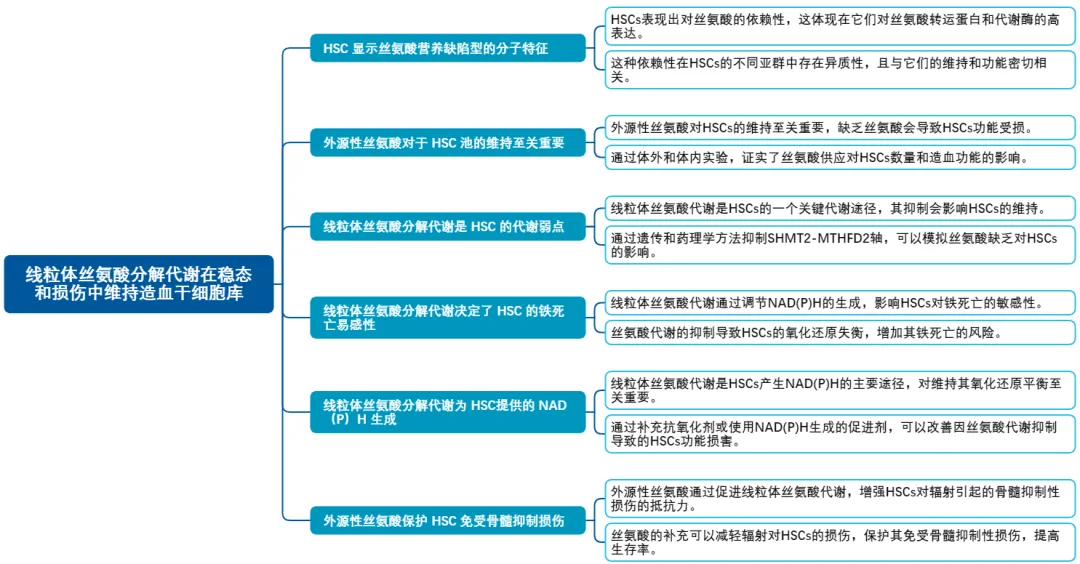
研究技术路线图
01HSCs的丝氨酸代谢特征
①基于已发表的RNA测序数据集分析发现,小鼠造血干细胞和祖细胞(HSPCs)中存在三个明显的聚类,其中HSCs具有独特的特征,表明丝氨酸代谢具有高度异质性。
②最原始的LSK细胞(被认为是HSCs)在丝氨酸转运蛋白和丝氨酸分解酶的表达上,比下游的造血祖细胞(HPCs)更高。相比之下,HSCs中负责丝氨酸新合成的关键酶PHGDH的表达较低。表明,HSCs表现出丝氨酸营养缺陷的分子特征
③在缺乏丝氨酸和甘氨酸的培养液(SGFM)中培养HSCs,发现细胞输出量降低,数量显著减少,HSC维持受损。这种影响在缺乏单一氨基酸的培养基中并未观察到。
④在体内实验中,给小鼠喂食缺乏丝氨酸和甘氨酸的饮食(SGFD),发现其对小鼠体重没有明显影响,但血液中丝氨酸水平显著降低,且出现白细胞减少、贫血和血小板减少等症状,表现出明显的髓系偏向性。表明,丝氨酸缺乏损害了HSC池的维持。
02线粒体丝氨酸代谢与HSCs的铁死亡
①丝氨酸分解由SHMTs启动,SHMT1在细胞质中催化,SHMT2在线粒体中催化。生成SHMT2条件性敲除(Shmt2CKO)小鼠模型,发现小鼠出现白细胞减少、血小板减少和髓系偏向性,且HSCs的维持能力受损。表明,丝氨酸分解代谢在HSCs的维持中起着关键作用。
②药理学抑制SHMT2可以模拟丝氨酸缺乏对HSCs的影响,而补充肌氨酸可以通过另一途径产生线粒体中的甲基四氢叶酸,从而恢复缺乏丝氨酸培养条件下HSCs的维持。表明,线粒体SHMT2在驱动HSCs中的丝氨酸分解中发挥主导作用。
③对SGFD小鼠的HSCs进行RNA测序分析,发现HSCs表现出髓系偏倚的转录特征,并且线粒体丝氨酸代谢和丝氨酸生物合成在这些HSCs中被特异性上调。通路富集分析显示,铁死亡途径被激活。在Shmt2CKO小鼠中,也观察到了HSCs铁死亡敏感性的增加。
④此外,使用铁死亡抑制剂Lip-1治疗小鼠,几乎完全消除了SGFD和Shmt2CKO小鼠HSCs的维持障碍和髓系偏向。Lip-1治疗还显著恢复了SGFD和Shmt2CKO小鼠的造血表型。表明线粒体丝氨酸分解的阻断使HSCs,尤其是平衡HSCs,更容易受到铁死亡的影响,从而损害了HSC池的维持。
03丝氨酸代谢在HSCs保护中的作用
①线粒体丝氨酸分解不仅生成一碳单位,还是铁死亡的主要防御物质NAD(P)H的主要来源。研究发现,SHMT2下游的甲酰四氢叶酸脱氢酶2(MTHFD2)在人类和小鼠HSCs中的表达高于下游的HPCs,这将HSCs的抗氧化需求与线粒体丝氨酸分解代谢联系起来。而在SGFD小鼠和Shmt2CKO小鼠的HSCs中检测到NAD(P)H/NAD(P)+比率降低,伴随着GSH/GSSG比率下降和ROS增加。
②在体外补充抗氧化剂N-乙酰半胱氨酸(NAC)或GSH,显著消除了HSCs铁死亡敏感性的增加,并恢复了SGFM中的HSC池维持。NAC处理挽救了SGFD和Shmt2CKO小鼠的骨髓造血表型。表明,由SHMT2-MTHFD2轴驱动的线粒体丝氨酸分解代谢主要为HSCs提供NAD(P)H生成,从而维持氧化还原平衡并提供铁死亡防御。
③研究发现,在受到5 Gy电离辐射(IR)后,HSCs的铁死亡在1天达到高峰。在IR后,线粒体而非细胞质的丝氨酸分解代谢在HSCs中迅速上调。而SGFD小鼠在IR后,血清中丝氨酸缺乏加剧,HSCs对铁死亡更加敏感。
④给予小鼠富含丝氨酸的饮食(SED),这显著减轻了IR后血清中丝氨酸的缺乏,以及NADPH/NADP+比率的降低和HSCs的铁死亡。然而,SED未能改善Shmt2CKO小鼠在受到辐射后的NADPH/NADP+比率降低、铁死亡以及骨髓抑制,也未能提高这些小鼠在受到6.0 Gy辐射后的存活率。表明外源性丝氨酸通过为线粒体丝氨酸分解提供燃料,保护HSC免受致命性骨髓抑制性损伤,进一步巩固了外源性丝氨酸在HSC维持中的保护作用。
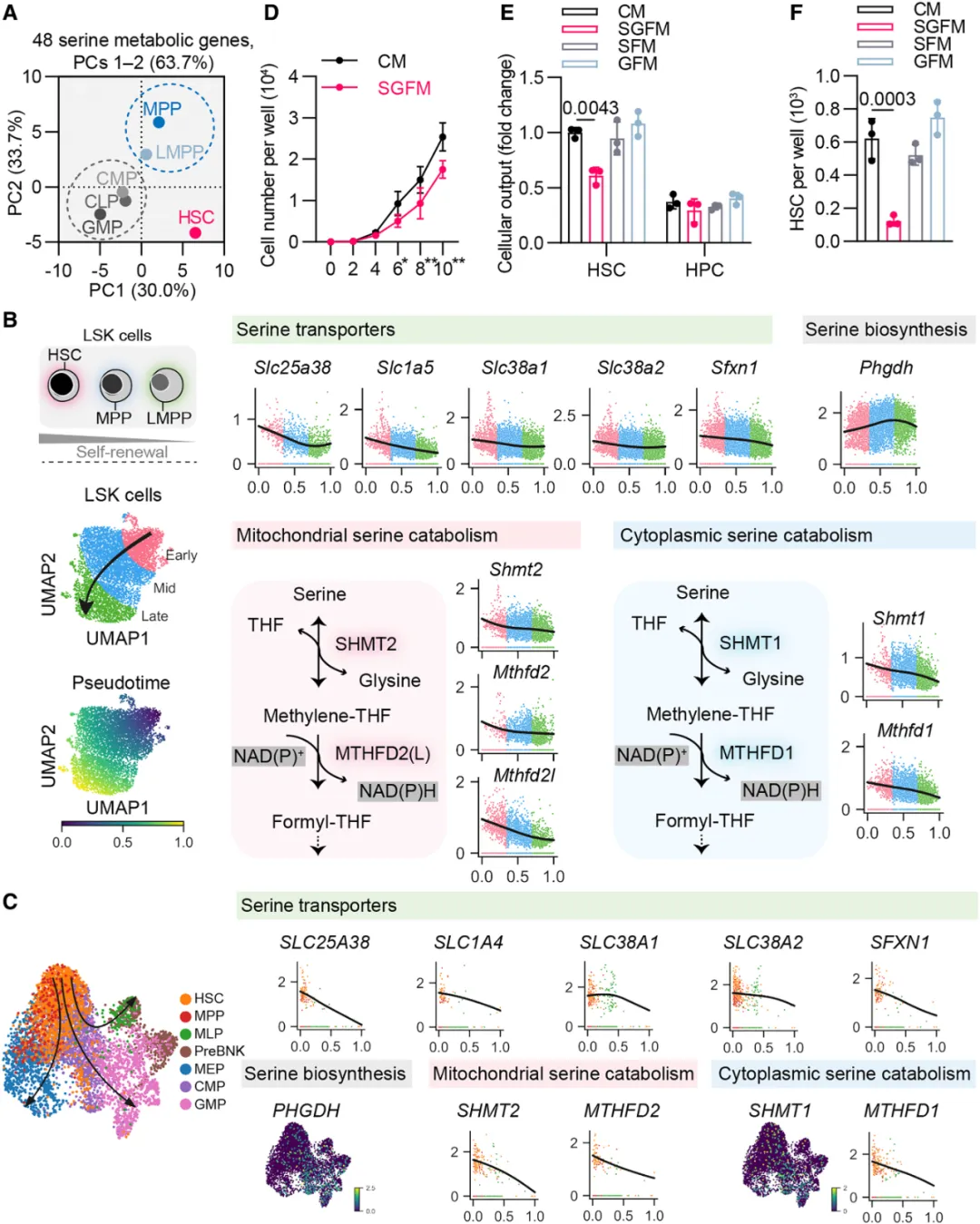
图1. 造血干细胞(HSCs)表现出丝氨酸营养缺陷的分子特征
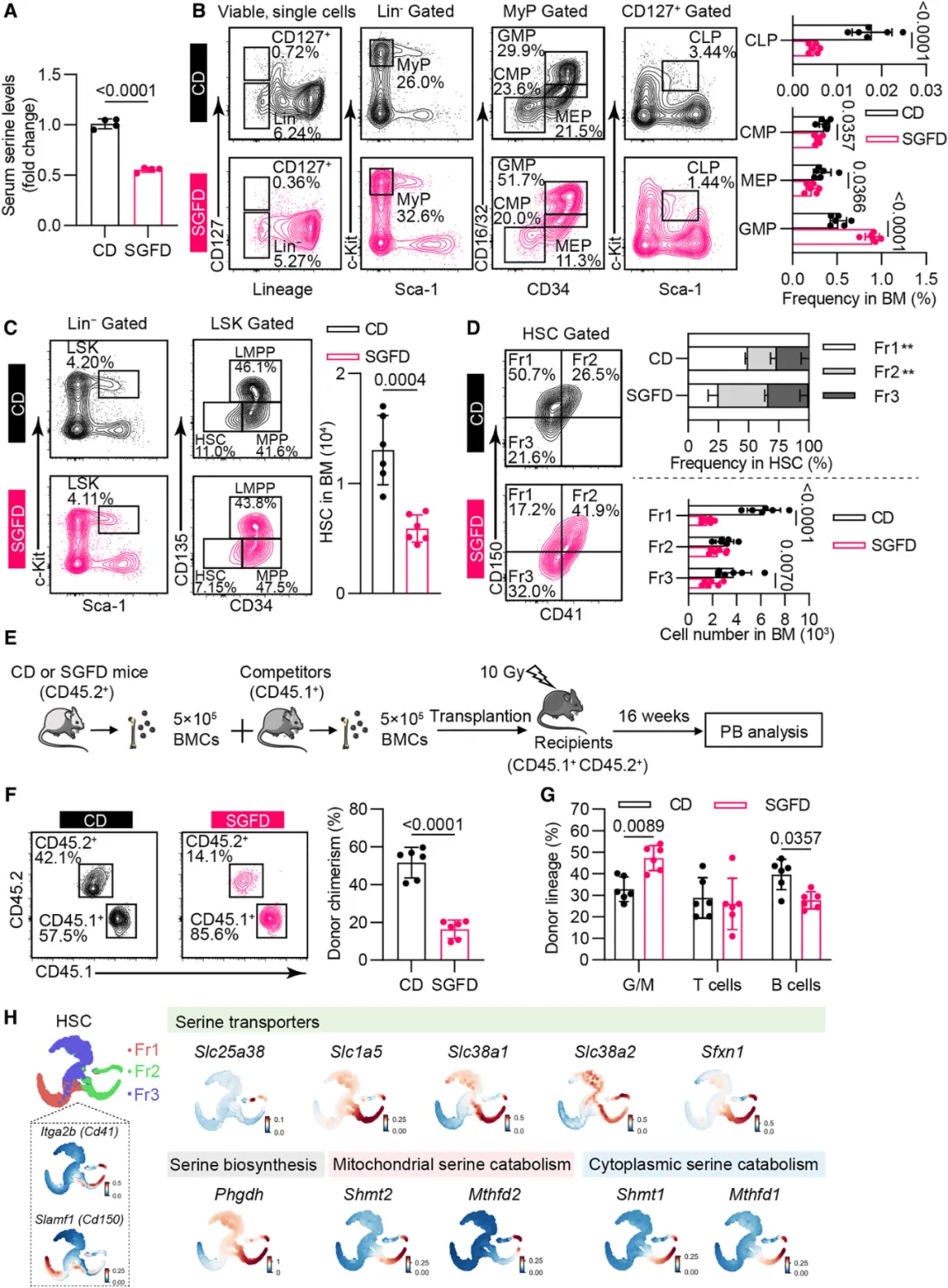
图2. 外源性丝氨酸对HSC池的维持至关重要
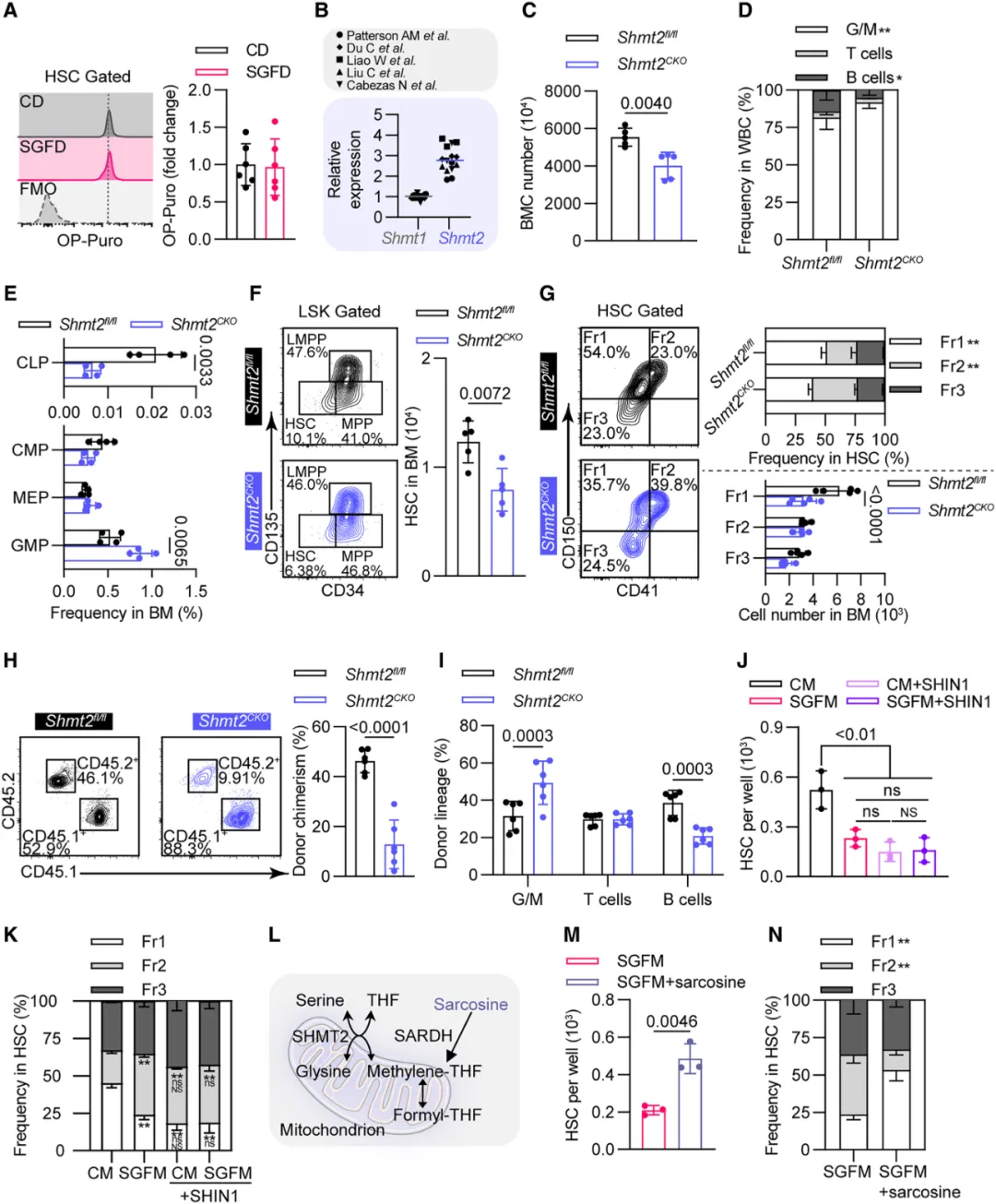
图3. 线粒体丝氨酸代谢是HSCs的代谢弱点
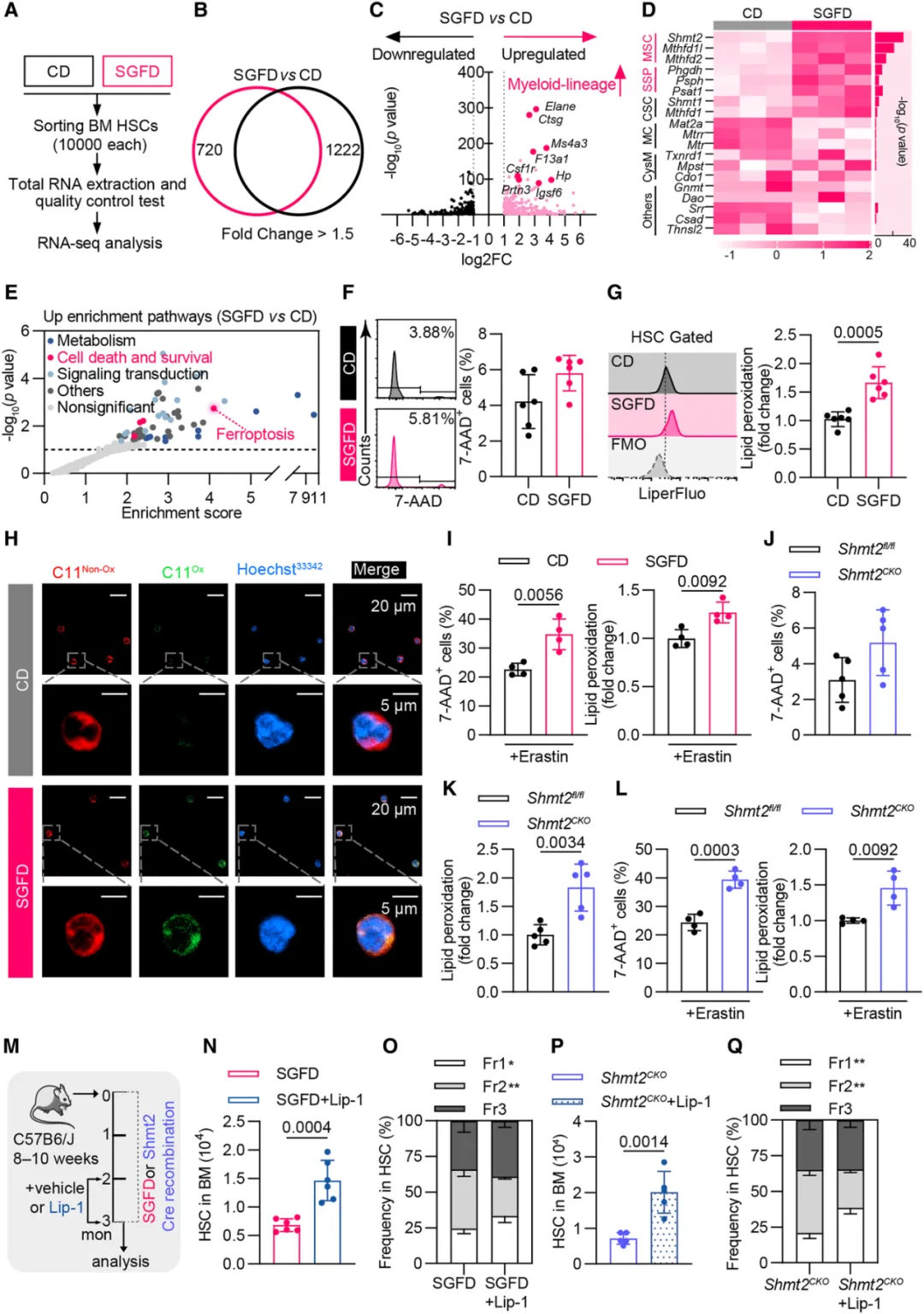
图4. 线粒体丝氨酸代谢决定HSCs的铁死亡敏感性
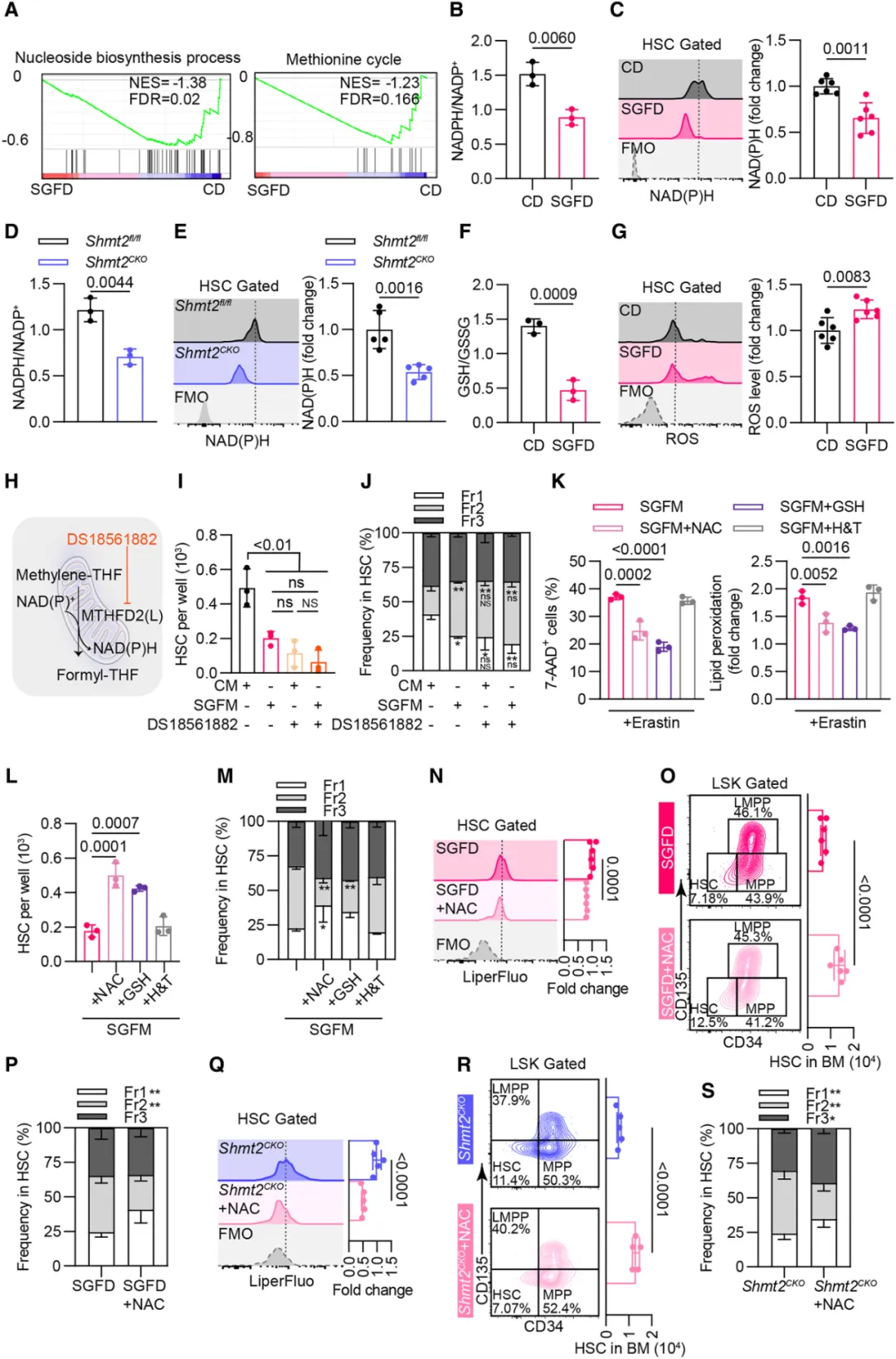
图5. 线粒体丝氨酸代谢为HSCs提供NAD(P)H生成
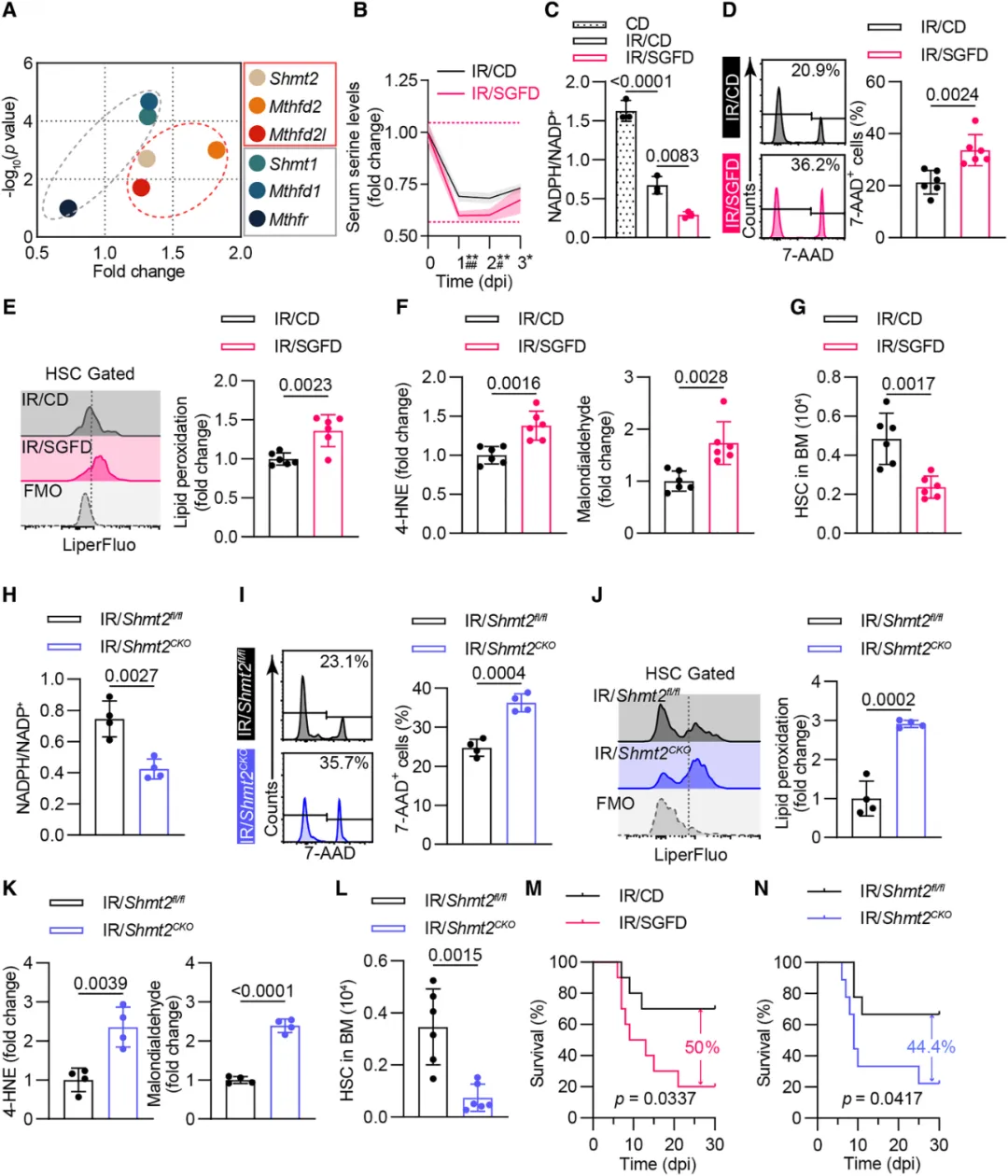
图6.外源性丝氨酸缺乏特征化并促成骨髓抑制性损
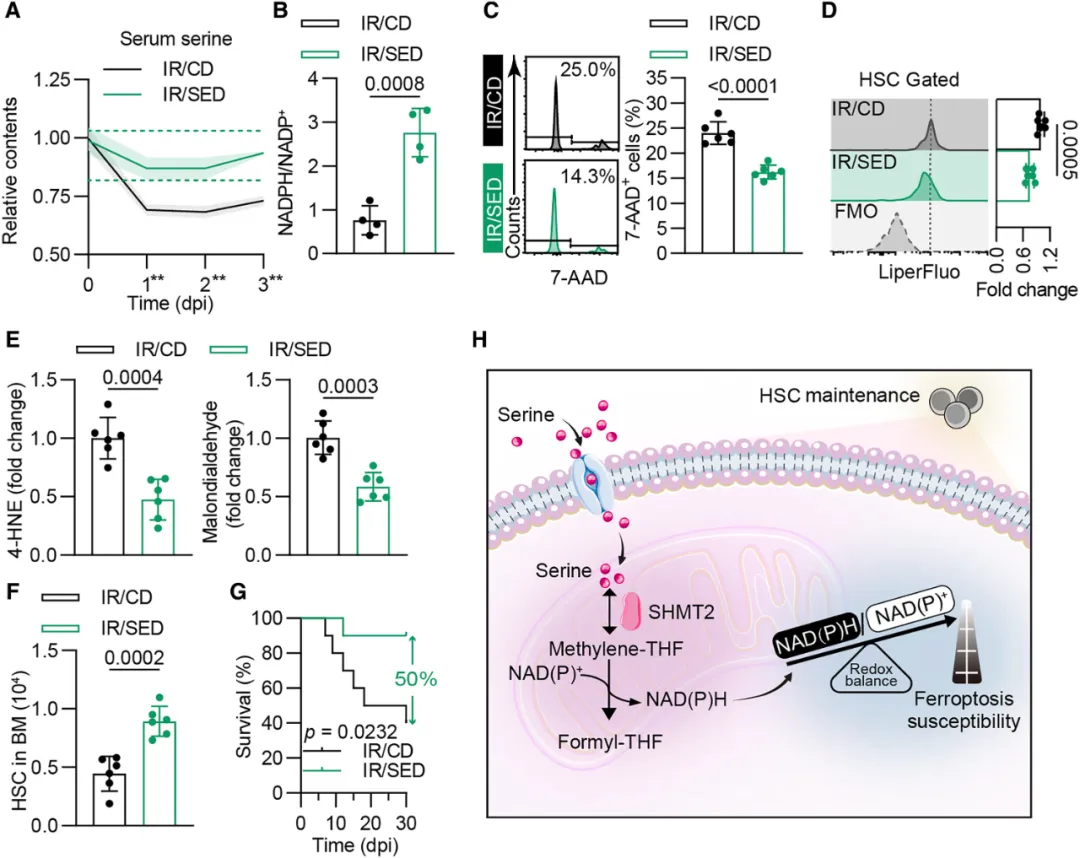
图7. 外源性丝氨酸保护HSCs免受骨髓抑制性损伤
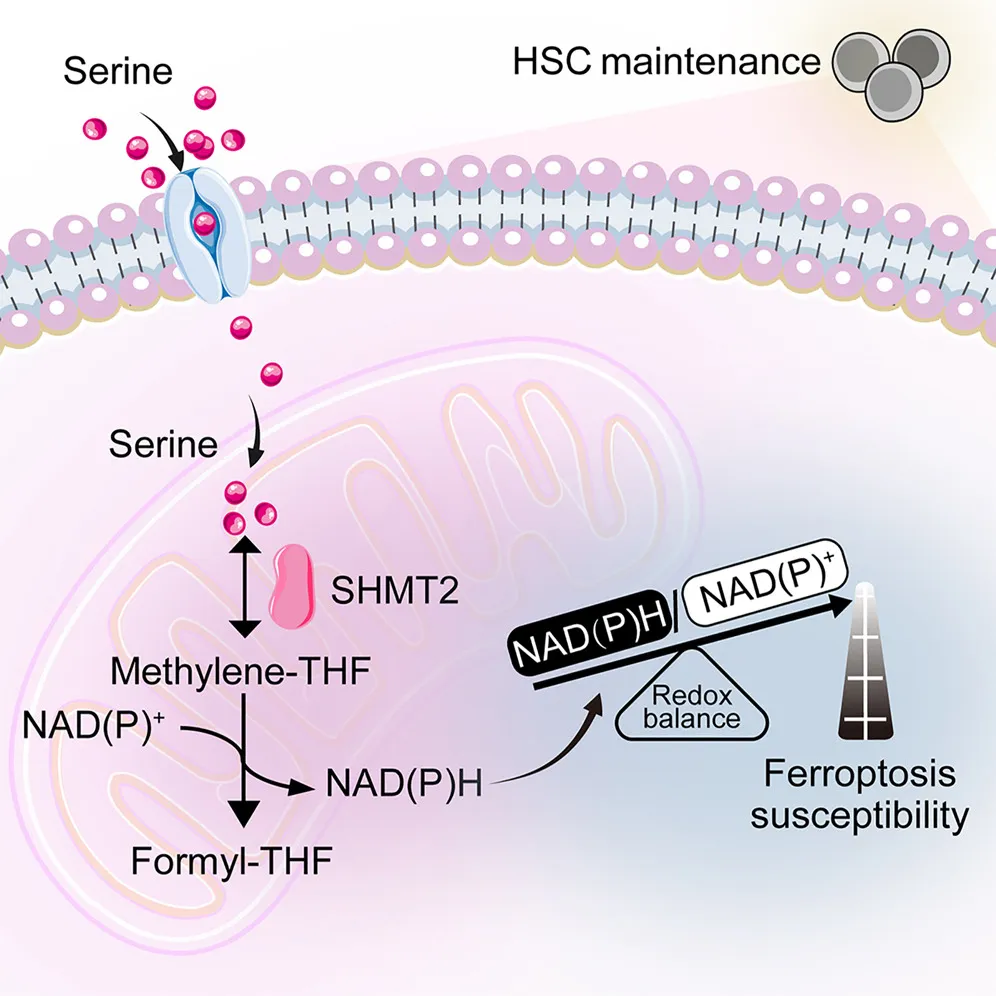
图8. Abstract
结论与讨论
本文研究发现,HSCs依赖于线粒体丝氨酸代谢来维持其在稳态和损伤后的池维护。外源性丝氨酸的供应对HSCs至关重要,其缺乏会导致HSCs的铁死亡敏感性增加,进而影响其功能。此外,丝氨酸代谢通过产生NAD(P)H来维持HSCs的氧化还原平衡,保护它们免受氧化应激。
在未来,研究需要进一步探索丝氨酸代谢在不同病理状态下HSCs中的作用,以及如何通过药物干预来调节这一代谢途径以增强HSCs的治疗效果。此外,研究还应关注丝氨酸代谢在其他干细胞类型中的作用,以及其在癌症治疗和血液疾病治疗中的潜在应用。
















 {{item.name}}会员
{{item.name}}会员
