揭开心肌梗死治疗的新篇章:miRNA与线粒体的互动
心肌梗死(MI)是全球范围内导致死亡和残疾的主要原因之一,其病理机制复杂,涉及氧化应激、炎症反应、细胞凋亡和线粒体功能障碍等多种因素。
近年来,微小RNA(miRNA)作为调节基因表达的重要分子,逐渐被认为在心血管疾病中发挥关键作用。研究表明,miRNA不仅参与心肌细胞的生长和分化,还在心肌缺血和再灌注损伤中发挥重要的保护作用。因此,探索miRNA在心肌梗死中的作用机制,尤其是其对线粒体功能的调节潜力,具有重要的科学意义和应用价值。在“心肌梗死和线粒体”领域,近年来的研究主要集中在以下几个方向:
✦线粒体功能与心肌梗死的关系
✦线粒体自噬与心肌保护
✦微小RNA与线粒体动态
✦药物干预与线粒体靶向治疗
基于当前研究进展,以下是三个待研究的核心方向:
✦线粒体质量控制机制的深入研究
✦微小RNA在心肌梗死中的作用机制
✦线粒体自噬与心肌重塑的关系
基于上述研究方向,以下是三个研究切入点:
✦特定疾病模型的选择
✦线粒体动态对心肌环境的影响
✦药物干预的机制研究
随后基于待研究的核心方向及其切入点,拟定以下标题:
核心方向1:线粒体质量控制机制的深入研究-切入点:“探讨线粒体质量控制在心肌梗死后心肌细胞存活中的关键作用及其机制”“线粒体质量监控机制对心肌梗死后心脏功能恢复的影响研究”“心肌梗死后线粒体质量控制的调节机制及其潜在治疗靶点”
核心方向2:微小RNA在心肌梗死中的作用机制-切入点:“微小RNA在心肌梗死中调控线粒体功能的机制研究”“miR-210与miR-146a在心肌梗死后线粒体动态调节中的作用及其临床意义”“探索微小RNA作为心肌梗死治疗新靶点的潜力:线粒体功能的调节”
核心方向3:线粒体自噬与心肌重塑的关系-切入点:“线粒体自噬在心肌梗死后心肌重塑中的作用及其机制研究”“心肌梗死后线粒体自噬对心脏功能恢复的影响及其潜在机制”“探讨线粒体自噬在心肌梗死后心肌重塑中的调节作用及其临床应用前景”
在确定了“探索微小RNA作为心肌梗死治疗新靶点的潜力:线粒体功能的调节”为研究方向后,接下来就要写出我们的立项报告啦~
课题摘要与关键词
课题摘要心肌梗死(MI)是全球主要的死亡原因之一,其病理机制复杂,涉及线粒体功能的损伤和细胞凋亡。近年来,微小RNA(miRNA)作为调节基因表达的重要分子,逐渐被认为在心血管疾病中发挥关键作用。然而,miRNA在心肌梗死中的具体作用机制尚不明确,尤其是其对线粒体功能的调节潜力。因此,本研究旨在探索微小RNA作为心肌梗死治疗新靶点的潜力,特别关注其对线粒体功能的影响。
已有研究表明,miR-210在缺血条件下上调,并与线粒体代谢和细胞存活密切相关(10.1161/CIRCULATIONAHA.121.056929, 2022)。基于此,我们假设miRNA能够通过调节线粒体功能,减轻心肌梗死后的细胞损伤。为验证这一假设,我们将采用体外细胞实验和体内动物模型,评估特定miRNA(如miR-210和miR-146a)对心肌细胞存活、线粒体功能及自噬过程的影响。
实验设计包括使用缺氧再灌注模型,分析miRNA对线粒体生物能量学、ROS生成及细胞凋亡的调控作用。预期结果为miRNA的调节能够显著改善心肌细胞的线粒体功能,降低细胞凋亡率,从而促进心肌细胞的存活。
本研究的科学意义在于揭示miRNA在心肌梗死中的新机制,为心血管疾病的治疗提供新的分子靶点。临床上,miRNA的靶向治疗可能成为心肌梗死患者的新策略,改善心脏功能和预后,具有重要的应用前景。
研究关键词:微小RNA;心肌梗死;线粒体功能;细胞凋亡;心血管疾病
立项依据与研究内容
1. 项目的立项依据
科学意义和应用价值心肌梗死(MI)是全球范围内导致死亡和残疾的主要原因之一,其病理机制复杂,涉及氧化应激、炎症反应和细胞凋亡等多种因素。近年来,微小RNA(miRNA)作为调节基因表达的重要分子,逐渐被认为在心血管疾病中发挥关键作用。研究表明,miRNA不仅参与心肌细胞的生长和分化,还在心肌缺血和再灌注损伤中发挥重要的保护作用。因此,探索miRNA在心肌梗死中的作用机制,尤其是其对线粒体功能的调节潜力,具有重要的科学意义和应用价值。
中国与国际上的研究概况目前,国内外对miRNA在心血管疾病中的研究逐渐增多,尤其是miR-210和miR-146a等在心肌梗死中的作用已被初步探讨。然而,关于miRNA如何具体调节线粒体功能、影响心肌细胞存活的机制尚不明确,尤其是在不同的缺血再灌注模型中。此外,现有研究多集中于单一miRNA的作用,缺乏对miRNA网络调控的系统性研究。因此,如何利用 miRNA 作为心肌梗死的治疗靶点仍然是一个亟待解决的问题。
前期工作结果我们在前期研究中发现,miR-210在缺氧条件下显著上调,并与线粒体代谢密切相关。通过对心肌细胞进行miRNA干预实验,我们观察到miR-210能够改善线粒体功能,降低细胞凋亡率。这些结果为我们提出的假设提供了支持:miRNA能够通过调节线粒体功能,减轻心肌梗死后的细胞损伤。
课题目标和价值本课题旨在研究微小RNA作为心肌梗死治疗新靶点的潜力,特别关注其对线粒体功能的影响。通过深入探讨miRNA在心肌梗死中的作用机制,我们希望为心血管疾病的治疗提供新的分子靶点,推动临床应用的发展,最终改善心肌梗死患者的预后。
2.项目的研究内容、研究目标及拟解决的关键科学问题
2.1研究内容miRNA对心肌细胞线粒体功能的影响:通过体外细胞实验,评估miR-210和miR-146a对心肌细胞线粒体生物能量学、ROS生成及细胞凋亡的调控作用。miRNA在缺血再灌注模型中的作用:建立缺血再灌注动物模型,观察miRNA干预对心肌细胞存活率和心脏功能的影响。miRNA与线粒体自噬的关系:探讨miRNA如何通过调节线粒体自噬过程来影响心肌细胞的存活和功能。
2.2研究目标探索miRNA在心肌梗死中的作用机制,明确其对线粒体功能的调节关系。评估miRNA作为心肌梗死治疗新靶点的潜力,探索其在临床应用中的前景。
2.3拟解决的关键科学问题关键的技术问题:如何有效地在体外和体内模型中干预特定miRNA的表达,并评估其对线粒体功能和心肌细胞存活的影响。理论问题:miRNA如何通过调节线粒体功能和自噬过程,影响心肌细胞的生存和心脏功能的机制尚不明确。本研究将揭示miRNA在心肌梗死中的新机制,为心血管疾病的治疗提供理论基础和实践指导。
拟采取的研究方案及可行性分析
3. 研究方案
技术路线图
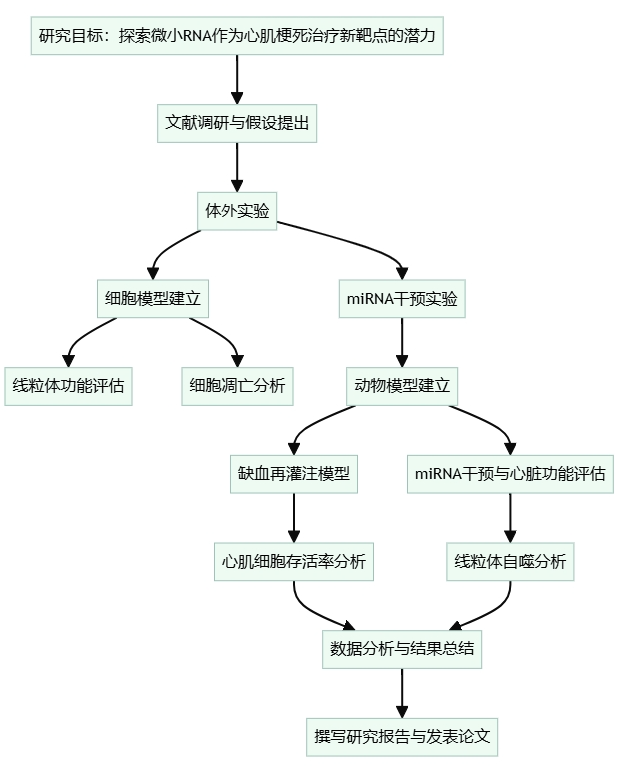
*点击放大实验步骤①细胞模型建立,动物模型建立②miRNA干预实验③线粒体功能评估:④细胞凋亡分析⑤心肌细胞存活率分析⑥线粒体自噬分析
4. 可行性分析
4.1关键问题分析实验材料与关键技术说明:实验材料:H9c2心肌细胞、雄性Wistar大鼠、miRNA模拟物、缺氧再灌注诱导剂(如CoCl2)、JC-1染色试剂、流式细胞术试剂盒等。关键技术:细胞转染技术、Seahorse XF分析、流式细胞术、Western blot、TUNEL染色等。
4.2研究技术思路说明:本研究采用体外细胞实验与体内动物模型相结合的方式,系统评估miRNA对心肌细胞线粒体功能的影响。通过建立缺氧再灌注模型,能够模拟心肌梗死后的真实病理状态,确保研究结果的临床相关性。miRNA干预技术的成熟和线粒体功能评估技术的可靠性为本研究提供了坚实的基础。
4.3项目组成员技术力量:项目组成员包括心血管生物学、分子生物学和药理学领域的专家,具备丰富的实验经验和技术积累,曾参与多项相关研究项目,具有较强的科研能力和团队合作精神。
项目的特色与创新之处
5. 研究内容的独特性
本研究聚焦于微小RNA(miRNA)在心肌梗死(MI)中的作用,特别是其对线粒体功能的调节。尽管已有研究探讨了miRNA在心血管疾病中的作用,但系统性研究miRNA如何通过调节线粒体功能来影响心肌细胞存活的内容尚未见于国内外文献。我们将采用综合的实验设计,结合体外细胞实验与体内动物模型,深入探讨特定miRNA(如miR-210和miR-146a)在缺氧再灌注条件下对心肌细胞线粒体功能的影响。
此外,本研究将采用多种技术手段,如Seahorse XF分析、流式细胞术和Western blot等,全面评估miRNA对线粒体生物能量学、细胞凋亡及自噬的调控作用。这种多维度的研究方法将为理解miRNA在心肌梗死中的作用提供新的视角,具有显著的独特性和新颖性。
6. 科学意义及吸引力
本研究聚焦于微小RNA(miRNA)在心肌梗死(MI)中的作用,特别是其对线粒体功能的调节。尽管已有研究探讨了miRNA在心血管疾病中的作用,但系统性研究miRNA如何通过调节线粒体功能来影响心肌细胞存活的内容尚未见于国内外文献。我们将采用综合的实验设计,结合体外细胞实验与体内动物模型,深入探讨特定miRNA(如miR-210和miR-146a)在缺氧再灌注条件下对心肌细胞线粒体功能的影响。
此外,本研究将采用多种技术手段,如Seahorse XF分析、流式细胞术和Western blot等,全面评估miRNA对线粒体生物能量学、细胞凋亡及自噬的调控作用。这种多维度的研究方法将为理解miRNA在心肌梗死中的作用提供新的视角,具有显著的独特性和新颖性。
年度计划及预期结果
7. 年度计划
第1年:文献综述与初步实验第2年:主要实验第3年:数据分析与论文撰写
8. 预期结果
解决问题:可望解决miRNA在心肌梗死中的具体作用及其对线粒体功能的调节问题。
机制阐明:阐明miRNA如何通过调节线粒体自噬和细胞存活机制,影响心肌细胞的生存和功能。
意义明确:明确miRNA在心肌梗死治疗中的潜在应用价值,为心血管疾病的治疗提供新的思路。
临床应用:有可能提供新的临床诊断指标或潜在的治疗靶点,推动miRNA靶向治疗的临床应用。
学术论文:预计发表至少1-2篇高水平的学术论文。
















 {{item.name}}会员
{{item.name}}会员
