山东大学发27.7分cell子刊,揭秘高脂饮食破坏胆汁酸耐受性进而加剧结肠炎的机制
Highlights
1. 短暂性HFD通过提高肠道BA促进结肠炎进展和复发
2. TNF受损的BA耐受性赋予BA对肠上皮细胞的细胞毒性
3. TNF引起的BA在ER中的积聚通过IRE/XBP1诱导肠上皮细胞凋亡
4. 高肠BA阻碍UC和实验性结肠炎中英夫利昔单抗的反应性
近日,“Cell Metabolism”(IF=27.7)上发表了一篇题为“TNF compromises intestinal bile-acid tolerance dictating colitis progression and limited infliximab response”的文章。这篇文章探讨了TNF如何通过影响肠道对胆汁酸的耐受性来加剧溃疡性结肠炎(UC)的进展,并限制了抗TNF药物英夫利昔单抗的疗效。

公众号后台回复关键词【TNF】
��免费获取本篇
研究背景介绍
英夫利昔单抗是一种抗TNFα的单克隆抗体,用于治疗包括UC在内的多种炎症性疾病。它通过结合并中和TNFα,减少炎症反应。
胆汁酸(BAs)耐受性是指肠道上皮细胞对胆汁酸的解毒能力。当这种耐受性受损时,胆汁酸可能在肠道积累,导致细胞损伤和炎症反应。
研究思路分析
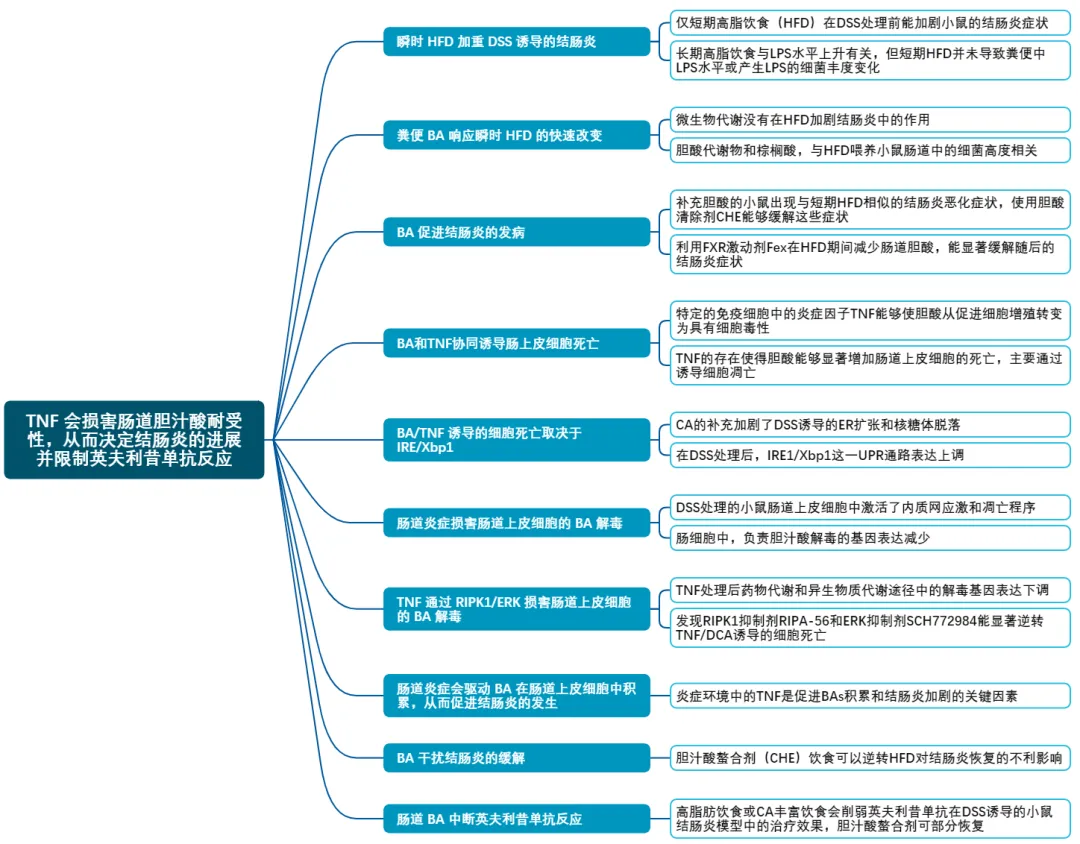
研究技术路线图01高脂饮食对结肠炎的影响
①通过研究不同饮食对结肠炎进展的影响,发现仅短期高脂饮食(HFD)在DSS处理前能加剧小鼠的结肠炎症状,包括疾病活动指数的增加、结肠缩短、上皮损伤加重和免疫细胞浸润增多。尽管长期高脂饮食与LPS水平上升有关,但短期HFD并未导致粪便中LPS水平或产生LPS的细菌丰度变化,说明结肠炎的加剧不是由LPS引起的。
②研究发现HFD显著改变了肠道微生物的多样性。尽管某些与UC进展负相关的菌群在HFD后减少,但另一菌群veillonellaceae的减少却与UC患者的升高相矛盾,这表明微生物组的变化可能不是HFD加剧结肠炎的直接原因。此外,研究没有发现两组间微生物代谢途径有显著差异,排除微生物代谢在HFD加剧结肠炎中的作用。同时,还发现肠道微生物群代谢产生的某些物质,特别是两种胆汁酸代谢物和棕榈酸,与HFD喂养小鼠肠道中的细菌高度相关,并在HFD喂养的小鼠中显著增加。说明HFD可能通过改变肠道微生物群的代谢产物,特别是胆汁酸水平,来影响结肠炎的进展。
02胆汁酸对结肠炎进展的影响
①给DSS处理的小鼠额外补充了两种主要的初级胆汁酸:胆酸(CA)和鹅去氧胆酸(CDCA),发现补充胆汁酸的小鼠出现与短期HFD相似的结肠炎恶化症状,包括更早的疾病活动指数增加和更明显的组织损伤。使用胆汁酸清除剂CHE能够缓解这些症状,而补充外源性CA则会加重损伤。进一步发现利用FXR激动剂Fex在HFD期间减少肠道胆汁酸,能显著缓解随后的结肠炎症状。此外,通过肝脏特异性敲减Cyp7a1酶来减少胆汁酸合成,也能减少粪便中的胆汁酸水平,并使小鼠对HFD引起的结肠炎具有抵抗力。
②通过单细胞RNA测序,发现在结肠炎早期,特定的免疫细胞(如髓系细胞和成纤维细胞)中的炎症因子TNF表达增加,而TNF能够使胆汁酸从促进细胞增殖转变为具有细胞毒性。进一步实验表明,TNF的存在使得胆汁酸能够显著增加肠道上皮细胞的死亡,主要通过诱导细胞凋亡。这些结果表明,在结肠炎的炎症环境中,TNF可能使肠道上皮细胞对胆汁酸变得敏感,从而导致细胞损伤。
03胆汁酸和TNF的协同作用
①通过TEM观察小鼠结肠组织,发现CA的补充加剧了DSS诱导的ER扩张和核糖体脱落。特别是肠上皮细胞在ER损伤上表现得更为明显,而其他类型的上皮细胞则未出现明显损伤。ER应激激活了未折叠蛋白反应(UPR),其中三种主要的ER传感器包括ATF6、IRE1和PERK。单细胞RNA测序数据揭示,在DSS处理后,仅IRE1/Xbp1这一UPR通路表达上调。进一步实验显示,当细胞同时暴露于DCA和TNF时,剪接体Xbp1(Xbp1s)的水平较单独暴露于DCA或TNF时更高。这表明TNF可能在胆汁酸引起的细胞毒性中起到协同作用。
②通过分析DSS处理小鼠和对照组小鼠结肠组织的单细胞RNA测序数据,发现DSS处理的小鼠肠道上皮细胞中激活了内质网应激和凋亡程序,同时异生物质和药物代谢途径下调。进一步分析发现,这些变化主要发生在肠细胞中,尤其是负责胆汁酸解毒的基因表达减少,如Cyp2c55、Cyp3a13和Sult1d1。通过对肠细胞进行重新聚类,发现两个主要在近端结肠的亚群在胆汁酸解毒方面受损。结肠组织的RNA测序验证了DSS处理过程中胆汁酸代谢的失调,类似变化也在溃疡性结肠炎患者中观察到。表明,肠道炎症阻碍了肠道上皮细胞对胆汁酸的解毒。
04TNF对胆汁酸解毒途径的影响
①通过共培养实验,发现TNF直接抑制了在DSS诱导的结肠炎早期阶段表达的胆汁酸解毒基因。RNA测序比较了TNF处理或未处理的肠道类器官,发现TNF处理后药物代谢和异生物质代谢途径中的解毒基因表达下调。公共数据库中的人类肠道类器官数据也显示,TNF处理后多种胆汁酸解毒基因表达显著减少。通过筛选抑制剂,发现RIPK1抑制剂RIPA-56和ERK抑制剂SCH772984能显著逆转TNF/DCA诱导的细胞死亡,并在小鼠肠道类器官中验证了这一发现。这些结果表明,TNF通过RIPK1/ERK途径破坏胆汁酸解毒系统,使肠道上皮细胞对胆汁酸更为敏感。
②TNF导致BAs在肠道上皮细胞中积累,增强其细胞毒性。在炎症条件下,BAs在细胞中的积累增加,导致结肠炎恶化。激活PXR或CAR可以减轻这种毒性作用和结肠炎的严重程度。磺酸化的BAs不会与TNF协同引发细胞毒性,表明炎症环境中的TNF是促进BAs积累和结肠炎加剧的关键因素。
05胆汁酸积累与结肠炎治疗响应
①研究发现,短暂的HFD会影响结肠炎的恢复。经过DSS处理和3天清水喂养后,接受HFD的小鼠结肠炎恢复较差,表现为结肠缩短和更严重的组织病理学变化。与HFD类似,CA喂养也加剧了DSS诱导的结肠炎的恢复。胆汁酸螯合剂(CHE)饮食可以逆转HFD对结肠炎恢复的不利影响,并且CHE在正常饮食下也能促进结肠炎的恢复,表明生理水平的BAs也会干扰结肠炎的缓解。
②研究发现,高脂肪饮食或CA丰富饮食会削弱英夫利昔单抗在DSS诱导的小鼠结肠炎模型中的治疗效果。使用胆汁酸螯合剂可以部分恢复治疗效果。对UC患者的研究表明,对英夫利昔单抗无应答的患者粪便中胆汁酸水平显著高于应答者,特别是CA和ACA这两种胆汁酸。这些发现表明,胆汁酸水平可能与英夫利昔单抗在UC治疗中的疗效抵抗有关。
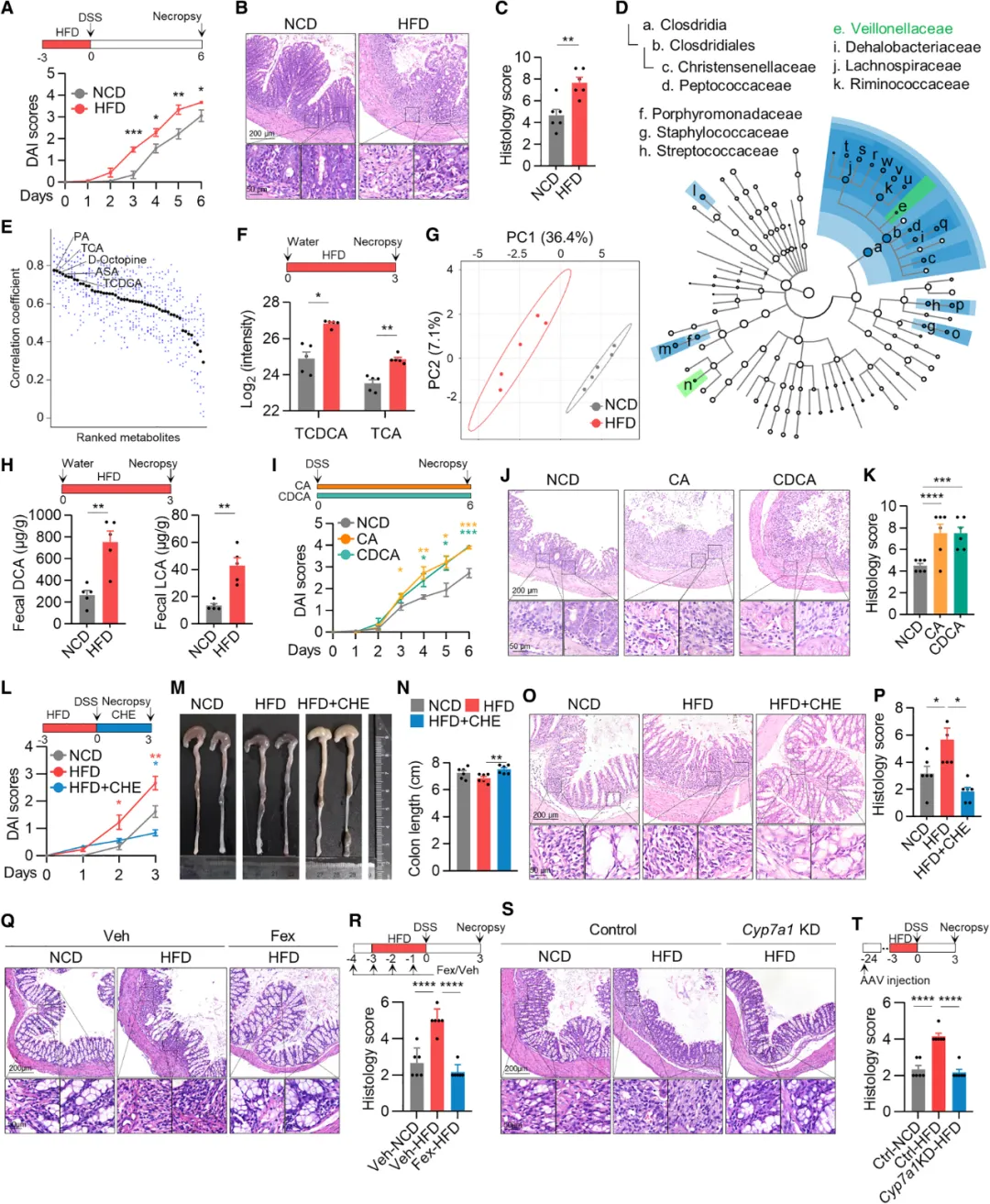
图1. 短期高脂饮食通过胆汁酸加剧DSS诱导的结肠炎
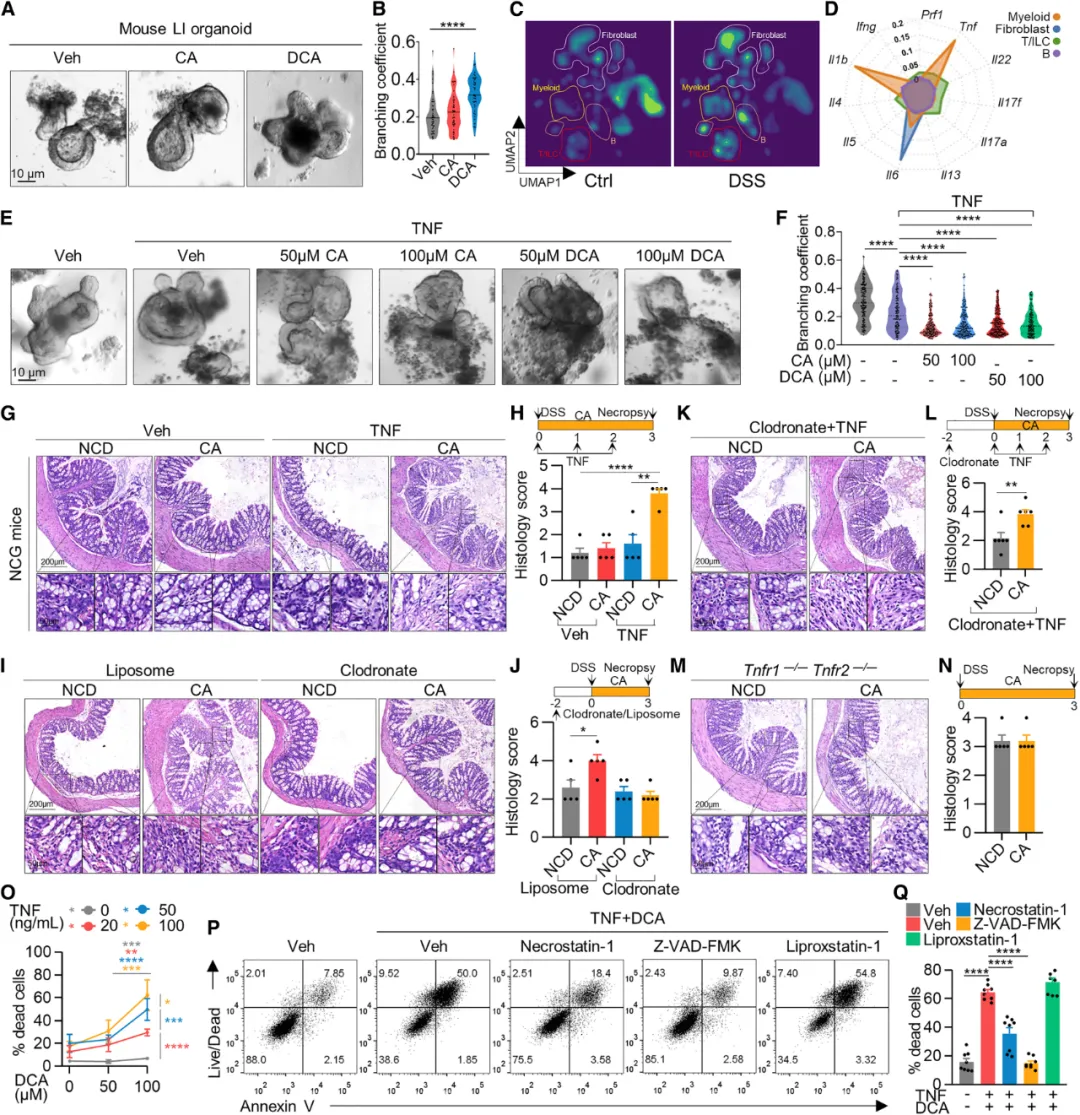
图2. 胆汁酸和TNF协同诱导肠道上皮细胞死亡
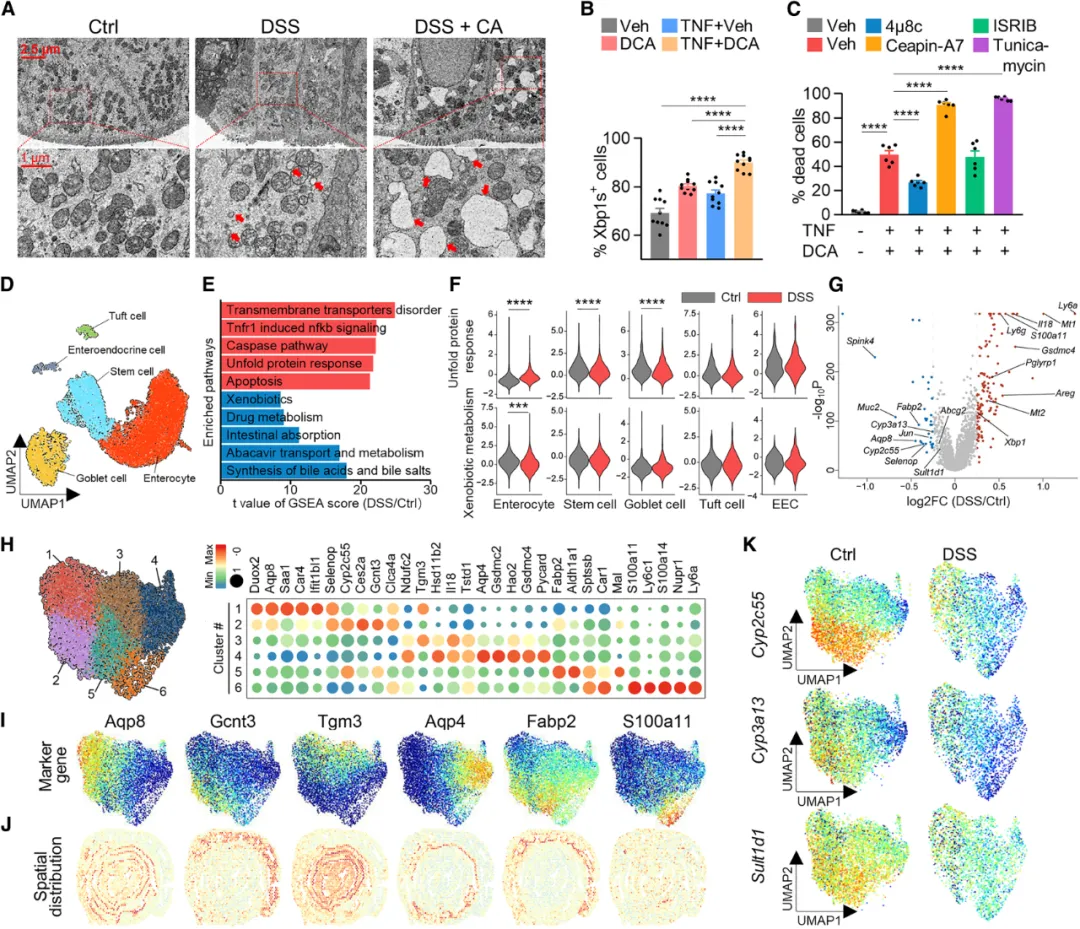
图3. BA/TNF诱导的细胞死亡依赖于IRE/Xbp1
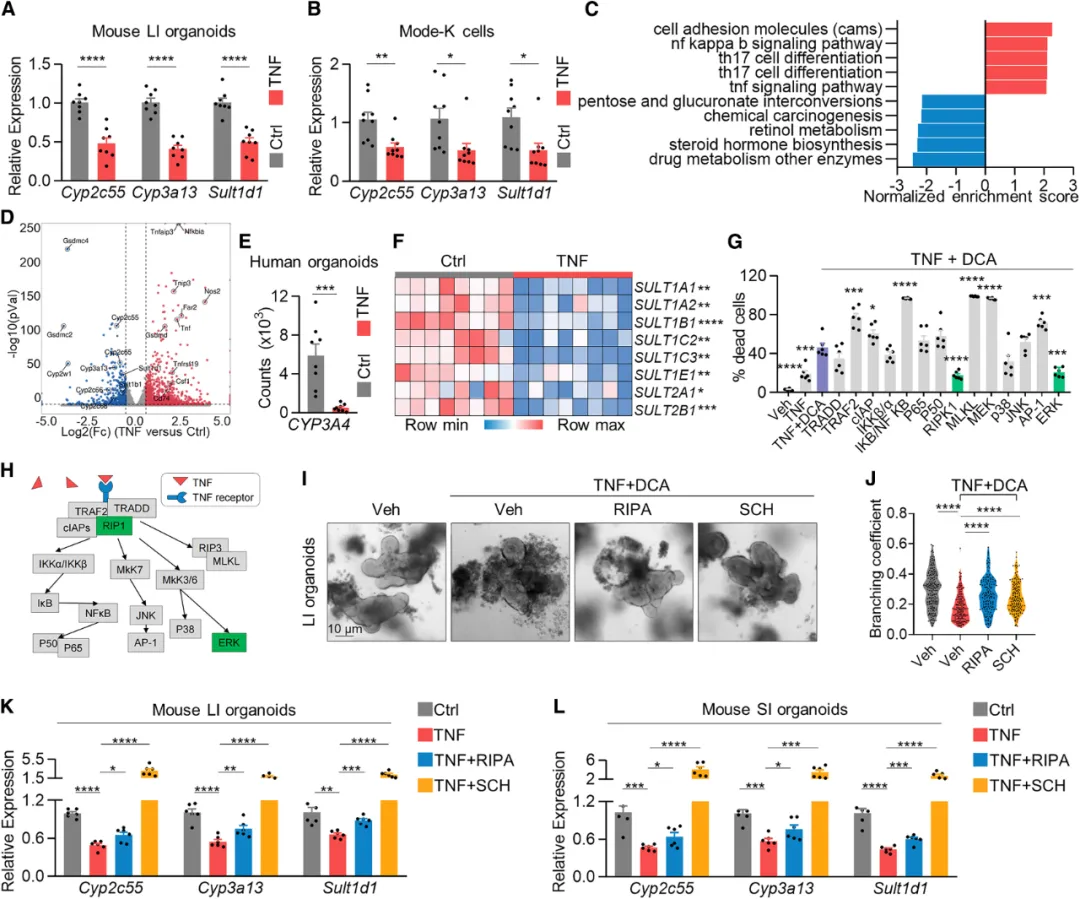
图4. TNF通过RIPK1/ERK损害肠道上皮细胞的胆汁酸解毒能力
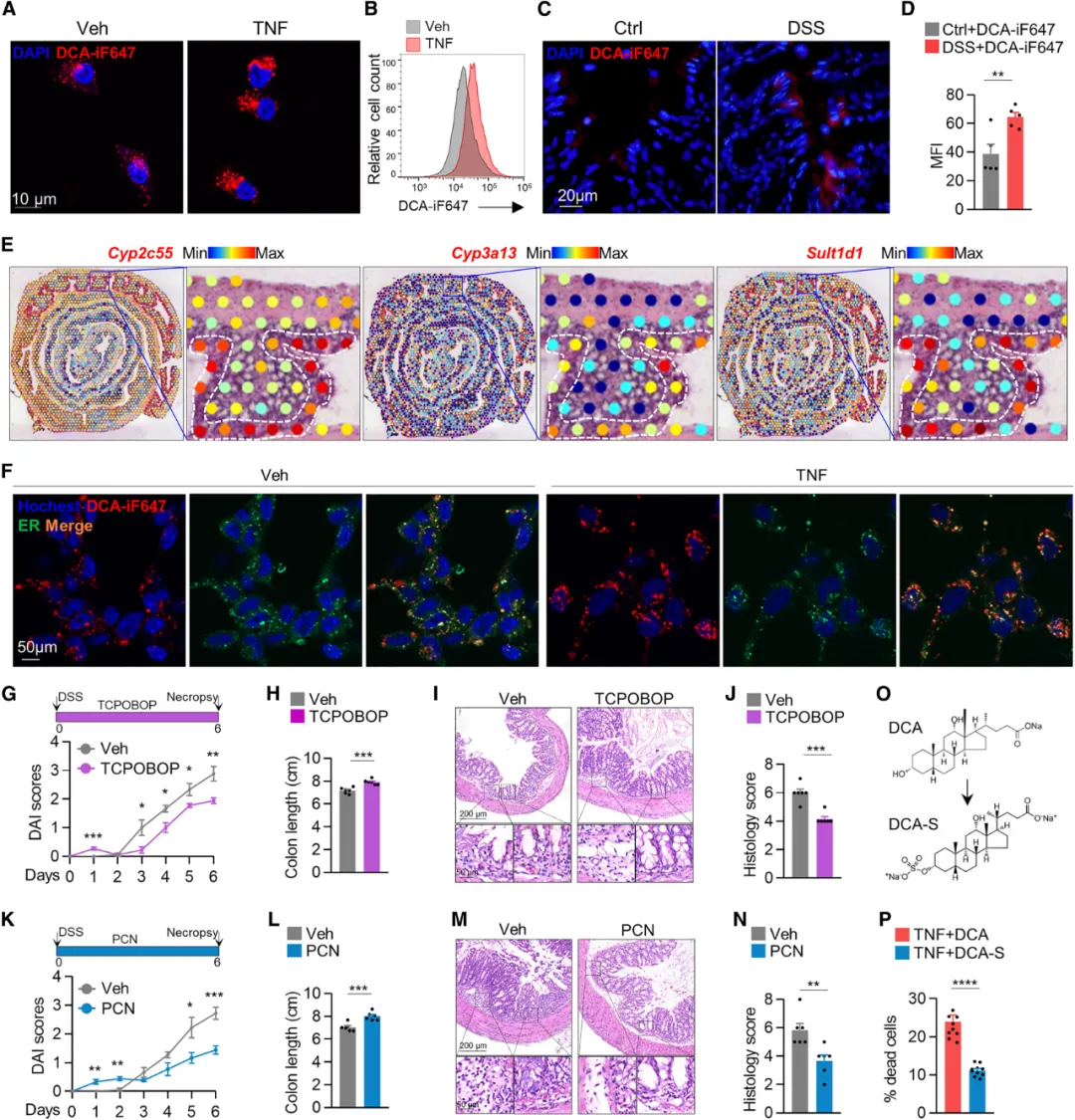
图5. TNF诱导的BA积累由于受损的BA耐受性
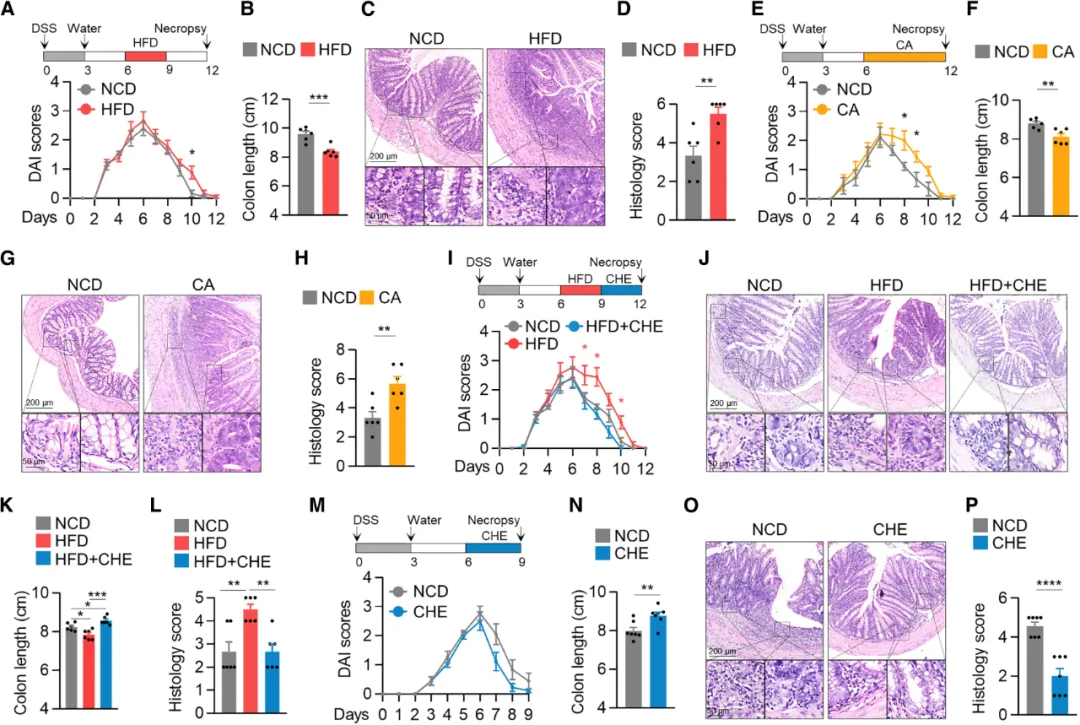
图6. BAs干扰结肠炎的缓解
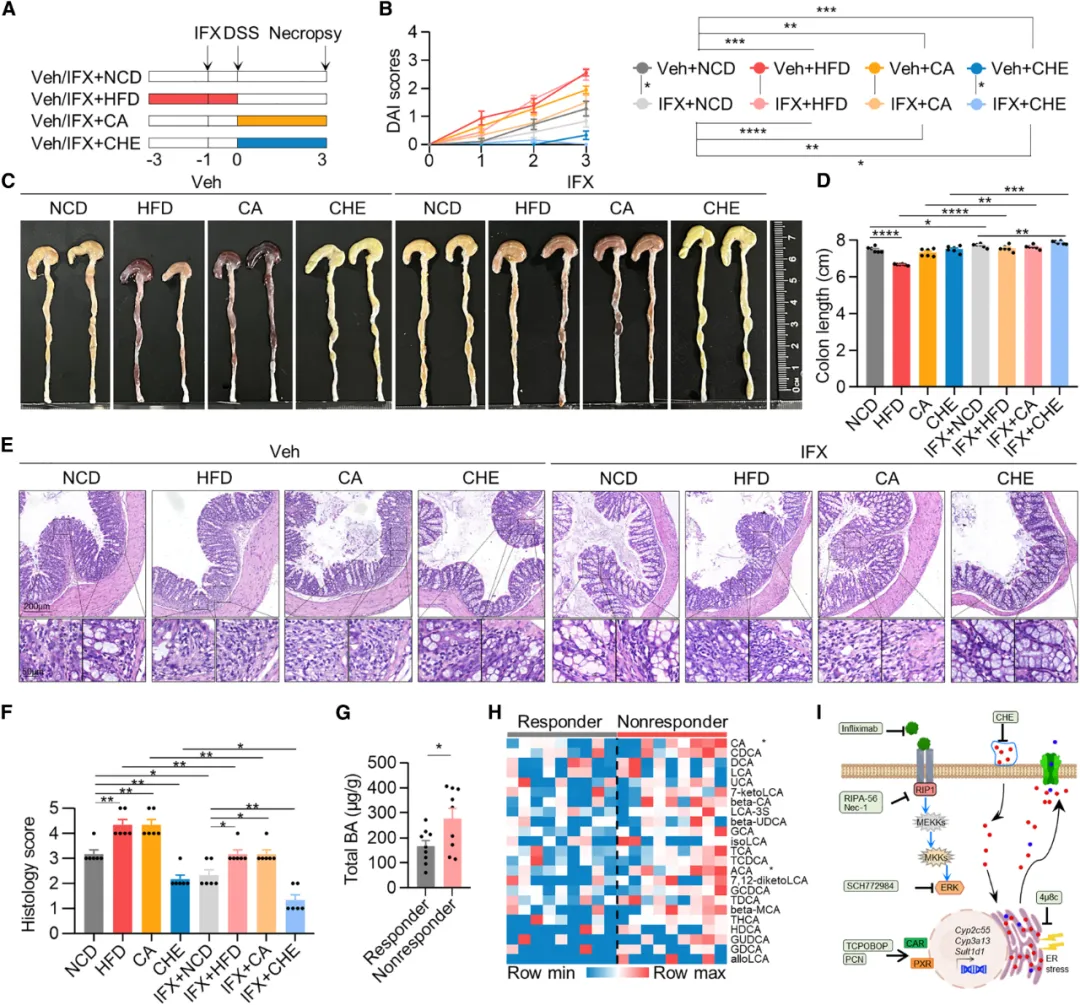
图7. 肠道BAs中断英夫利昔单抗的响应性
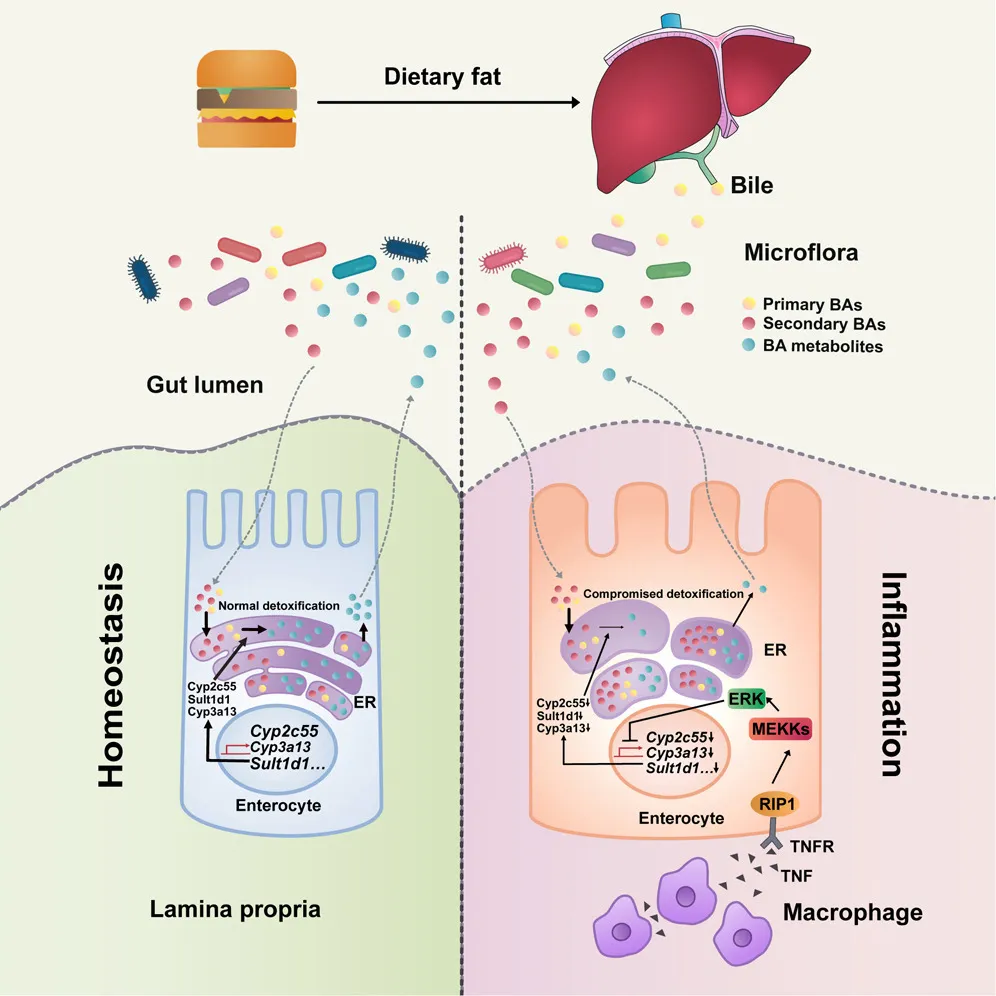
图8. abstract
结论与讨论
本文研究发现,短期高脂饮食通过提升肠道胆汁酸水平加剧UC,并且TNF通过RIPK1/ERK信号通路干扰胆汁酸解毒,导致内质网应激和细胞凋亡。此外,肠道胆汁酸的积累与英夫利昔单抗治疗反应不良相关,而胆汁酸清除可提高治疗的有效性。
然而,尽管研究揭示了胆汁酸在UC中的致病作用,但胆汁酸在肠道环境中对其他细胞类型的影响仍需进一步研究。此外,TNF对胆酸解毒的干扰机制在不同细胞亚型中的表现及其对细胞功能的影响也需深入探讨。未来研究还应关注胆酸水平的精确调节时机,以优化UC的临床治疗策略。
















 {{item.name}}会员
{{item.name}}会员
