Cell子刊 | 重庆医科大学重磅研究:Nynrin通过抑制线粒体膜通透性转换孔维持造血干细胞功能
Highlights
1. Nynrin在稳定和应激状态下在HSC中高度表达
2. Nynrin缺乏影响HSC维持
3. Nynrin通过转录抑制Ppif表达抑制mPTP开放
4. Nynrin的过表达降低了HSC中辐射诱导的致死率
近日,“Cell Stem Cell”(IF=19.8)上发表了一篇题为“Nynrin preserves hematopoietic stem cell function by inhibiting the mitochondrial permeability transition pore opening”的文章。这篇文章主要研究了Nynrin蛋白在造血干细胞(HSCs)中的作用,特别是在维持HSCs功能和抵御辐射诱导的损伤方面。

研究背景介绍
造血干细胞(HSCs)是一类具有自我更新能力和多向分化潜能的干细胞,它们负责维持终身的造血功能,包括在骨髓中的长期驻留和在血液应激时的快速响应。
线粒体膜通透性转换孔(mPTP)是位于线粒体内膜上的一个通道,其开启与细胞死亡(如坏死和凋亡)密切相关。mPTP的调控对于维持细胞内线粒体功能和细胞命运至关重要。
Ppif:编码环孢素D的基因,是mPTP的关键组成部分。
研究思路分析
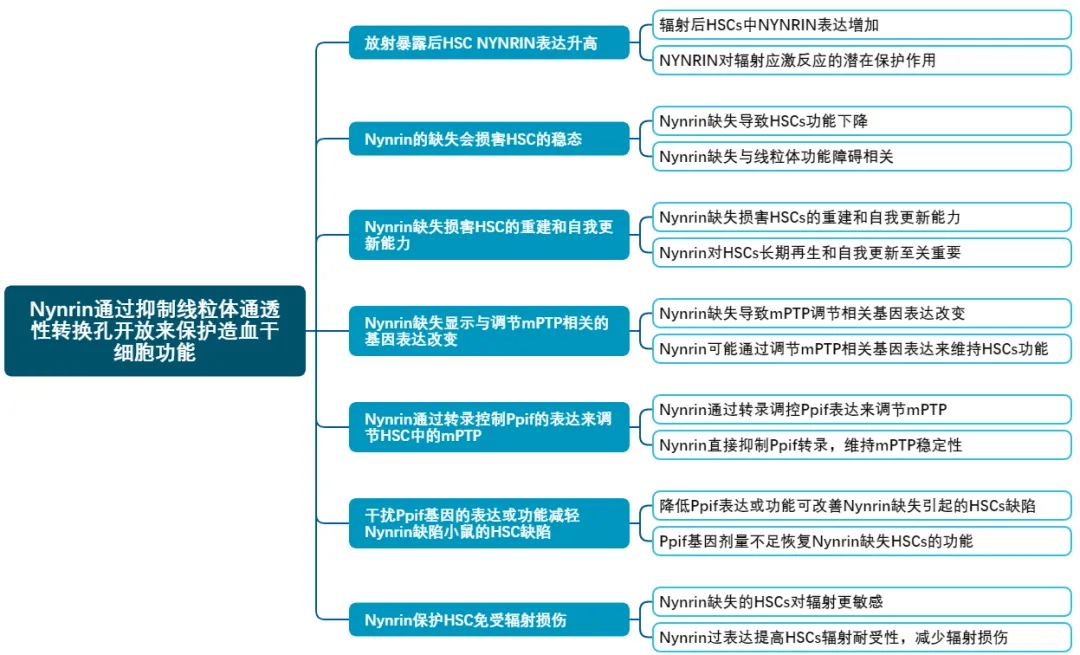
研究技术路线图
01Nynrin的表达与功能
①研究招募了八名患者,分析了他们在接受化疗放疗前后的周围血单核细胞 (PBMCs),发现治疗后某些造血干/祖细胞(HSPCs)亚群显著增加,但线粒体膜电位(MMP)下降,ROS水平上升,mPTP开启增强。
②对照射后的CD34+HSCs进行了转录组分析,Nynrin的表达发生了最大的变化。而在鼠模型中,辐射照射后,(Lin Sca-1+c-Kit+)LSKs、多能祖细胞和HSCs中Nynrin的表达显著增加。暴露于不同剂量的辐射也增强了Nynrin在各种造血谱系中的表达。
③单细胞测序分析小鼠LSK细胞,研究发现Nynrin在长期HSC(LT-HSCs)中表达显著。Nynrin缺失(Nynrin-CKO)小鼠表现出白血细胞、红细胞计数和血小板显著减少。Nynrin缺失还导致总骨髓有核细胞(BMNCs)显著减少,以及LSK、Cd34^-LSK和HSC频率和数量显著下降。此外,Nynrin缺失的HSCs表现出增加的细胞增殖和减少的G0期细胞比例,表明Nynrin对维持HSC的静止状态至关重要。
02Nynrin对HSCs长期功能的影响
①进行竞争性骨髓移植(BMT)实验,发现Nynrin缺失的小鼠在移植后,自我更新能力显著降低,其供体来源的外周血细胞和骨髓细胞的嵌合率逐渐降低,表明Nynrin对于HSCs的长期再生潜力和自我更新至关重要。
②进一步观察Nynrin缺失小鼠对IR的应激反应。结果显示,Nynrin缺失小鼠在接受全身照射后的生存率显著低于对照组。此外,Nynrin缺失小鼠在接受细胞周期依赖性药物5-氟尿嘧啶(5-FU)处理后,其死亡率高达80%,而对照组小鼠90%以上存活。进一步证实了Nynrin在维持HSCs功能和应激反应中的关键作用。
③对Nynrin敲除(Nynrinfl/flTie2-Cre)和对照(Nynrinfl/fl)小鼠的HSCs进行了RNA测序分析,基因集富集分析(GSEA)显示,Nynrin缺失的HSCs中与线粒体组分相关的通路发生了显著变化,包括细胞器内膜、线粒体蛋白复合体、线粒体呼吸链复合体组装和NADH脱氢酶复合体。
④研究还发现,Nynrin缺失导致HSCs的MMP显著降低,而线粒体质量并未改变。此外,Nynrin缺失的HSCs中ROS水平升高,线粒体肿胀,并且mPTP开启增加。这些变化与细胞凋亡和坏死的关键蛋白的表达上调有关,表明Nynrin缺失导致HSCs中线粒体mPTP开启和线粒体去极化,最终导致多种形式的细胞死亡。
03Nynrin的分子机制与辐射保护作用
①利用ChIP-seq和qPCR技术验证发现,Nynrin敲除的HSCs中Ppif mRNA表达显著上调,Ppif基因编码的环孢素D与mPTP开启和细胞死亡有关。进一步的研究表明,Nynrin能够结合Ppif基因启动子的特定位点,抑制其转录,并且Nynrin过表达会显著降低Ppif启动子的活性。表明,Nynrin通过抑制Ppif的表达来维持HSC的线粒体功能和功能稳态。
②培育了Ppif基因杂合突变的Ppif+/-Nynrinfl/flTie2-Cre小鼠。结果显示,这些双敲除小鼠的Ppif表达显著降低,而Ppif基因的单倍剂量不足降低ROS水平,抑制了mPTP的激活,显著恢复了双重敲除HSCs的MMP。
③将不同基因型的小鼠骨髓细胞移植到经过致死辐射的受体中,发现Ppif基因剂量不足增强了Nynrin缺失小鼠HSPCs的频率和静息状态。进一步的体外实验证实了Ppif+/-Nynrinfl/flTie2-Cre骨髓细胞在多次重植中保持了更高的克隆数量,表明其长期植入能力增强。环孢素A(CsA)和N-乙酰半胱氨酸(NAC)这两种药物的处理分别逆转了线粒体功能障碍并改善了HSC计数,证实了Nynrin通过下调Ppif表达、抑制mPTP的开放和减少ROS积累来保护HSC功能。
④此外,研究还发现Nynrin缺陷的HSCs对辐射更加敏感,照射后死亡率高,血细胞计数和HSC数量显著下降。Nynrin过表达的HSCs显示出更强的辐射保护能力,提高了植入效率和生存时间,并减少了辐射引起的损伤。Nynrin表达在发育和衰老过程中降低,可能影响HSCs的老化,但其保护作用并非在所有情景下都有效。
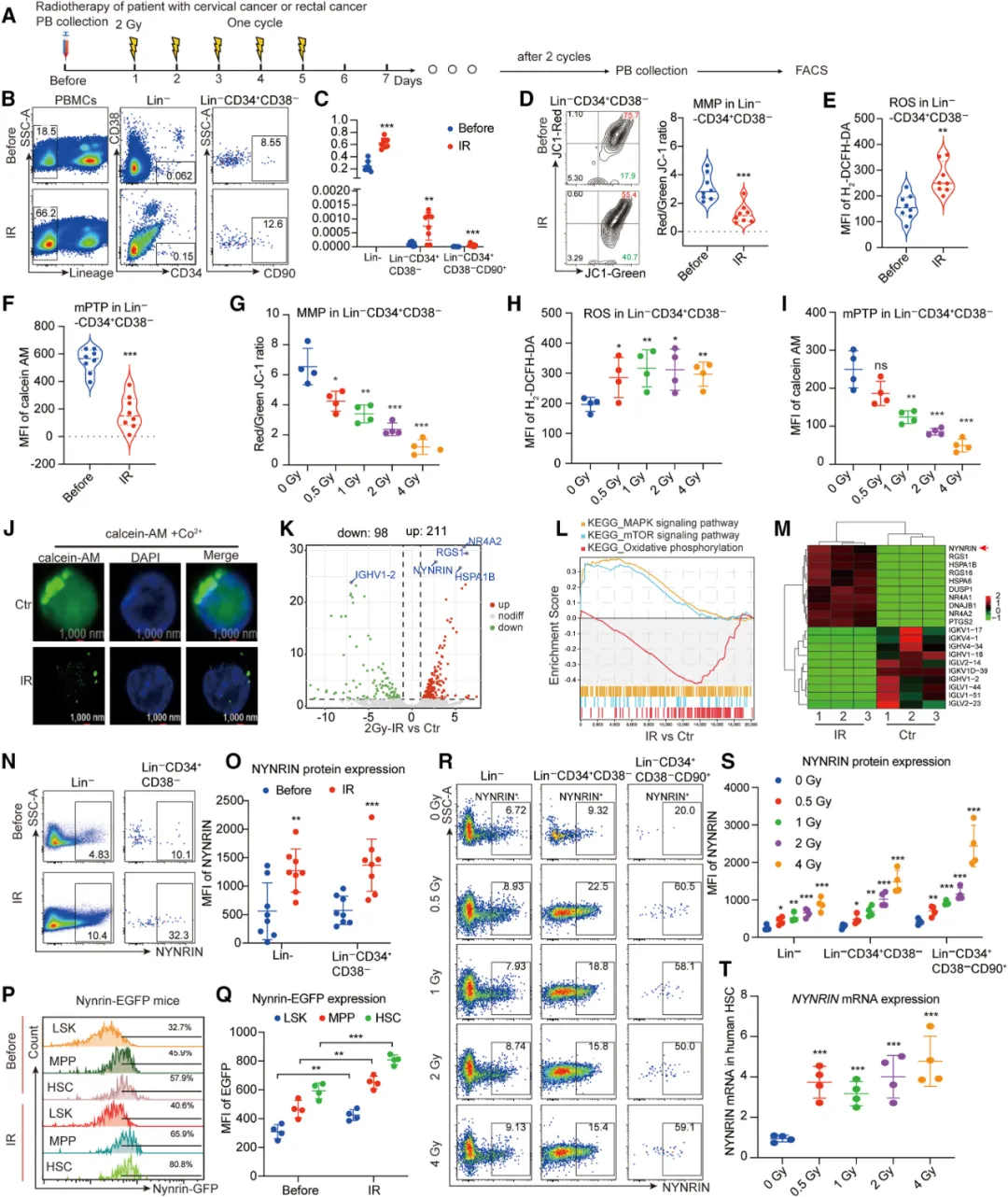
图1. 辐射暴露后造血干细胞中Nynrin表达增强
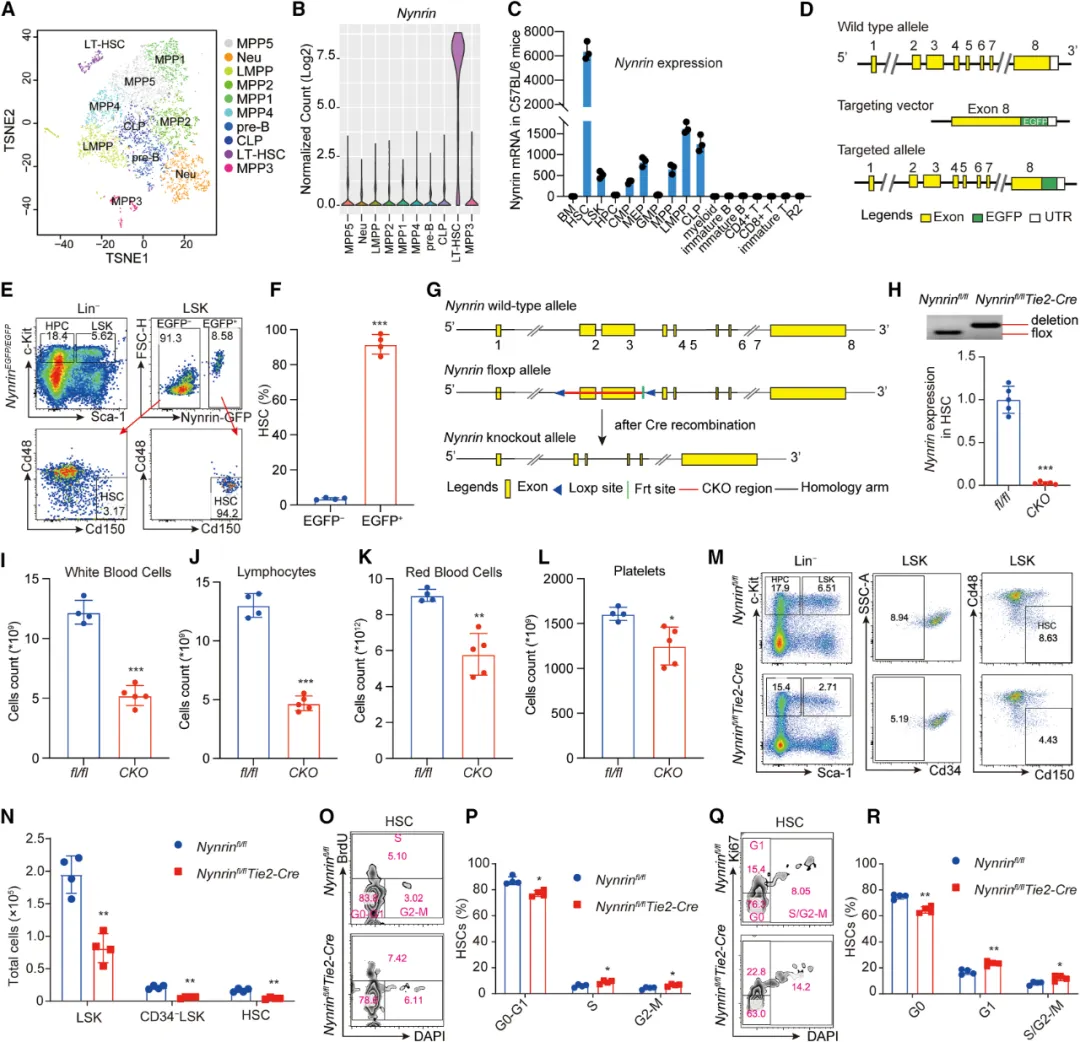
图2. Nynrin缺乏会破坏造血干细胞稳态
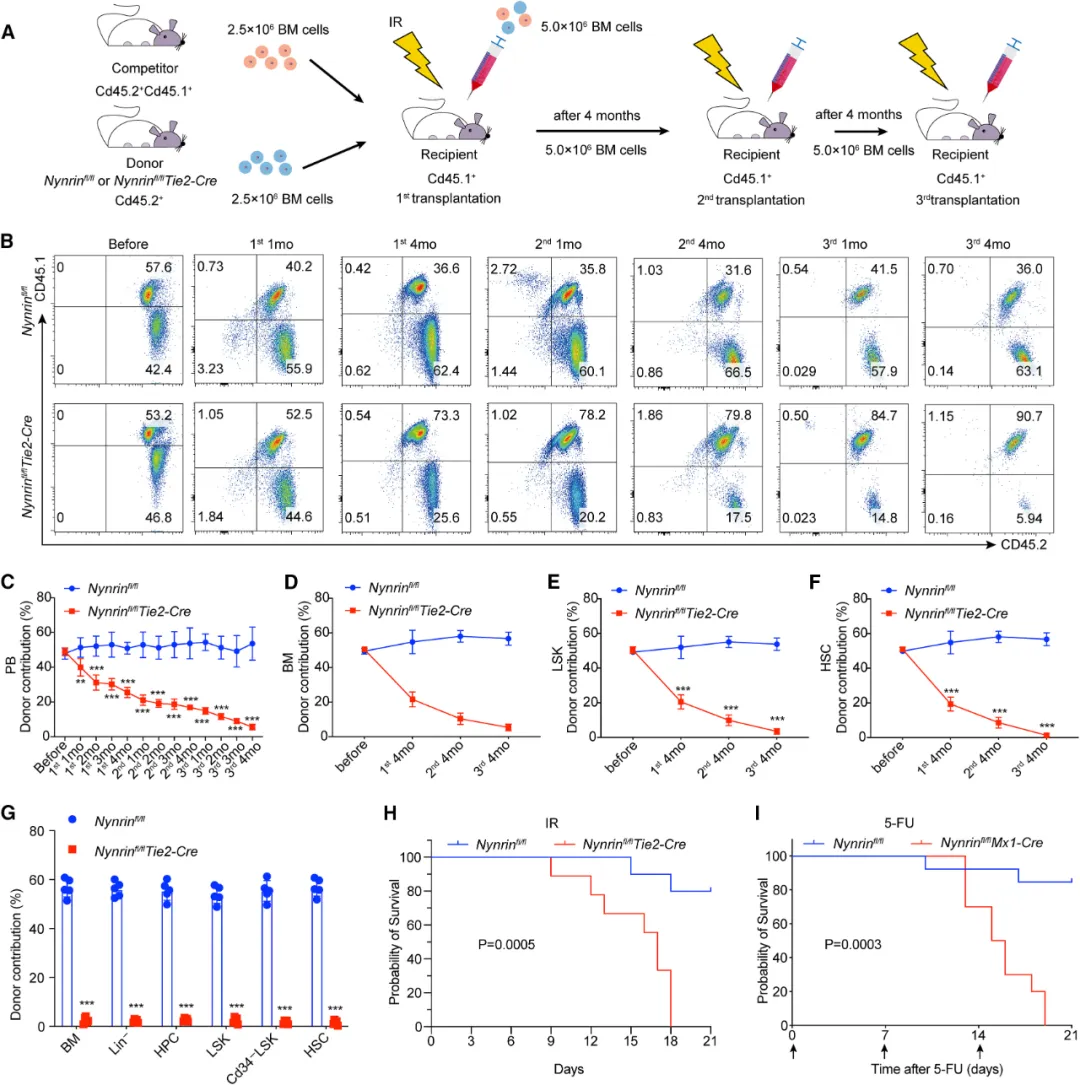
图3. 由于Nynrin缺失导致造血恢复和自我更新受损
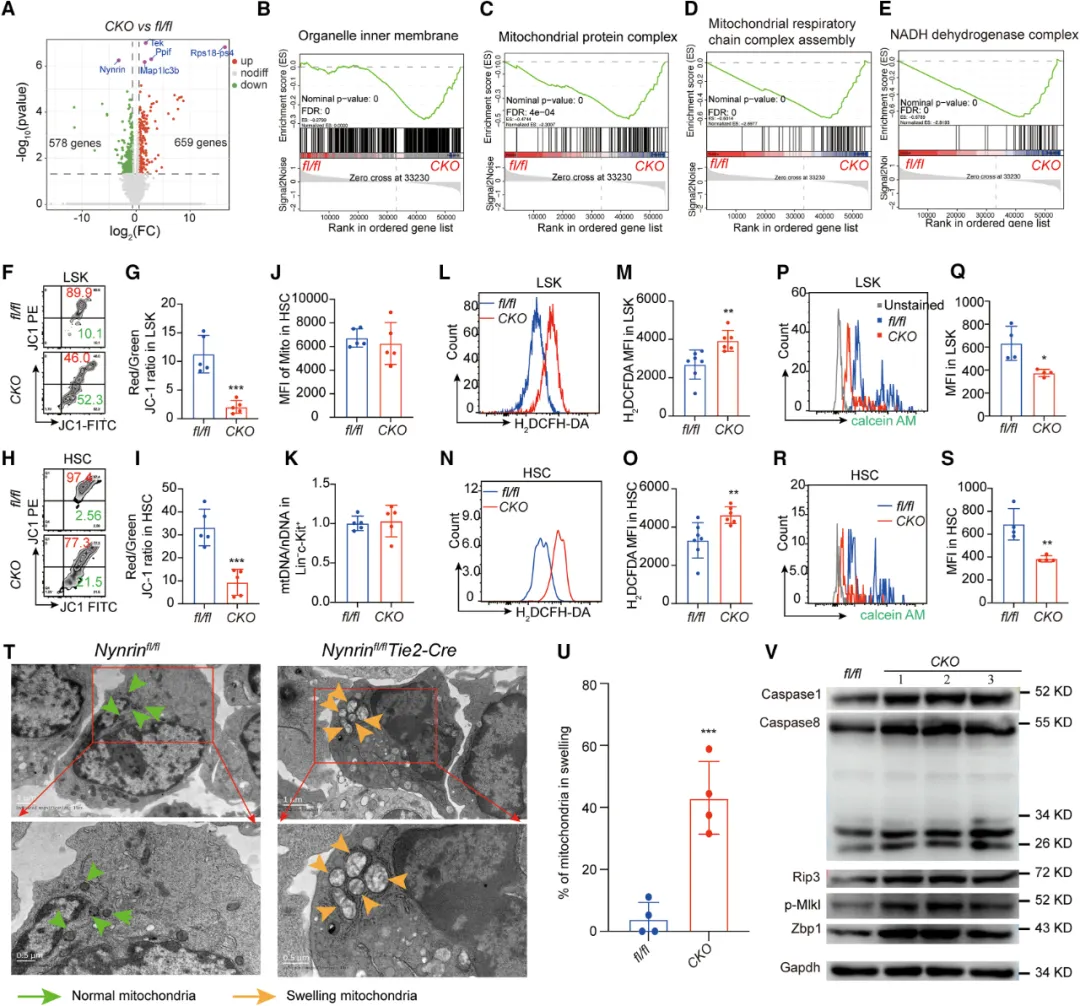
图4. 由Nynrin敲除引起的造血干细胞线粒体失调
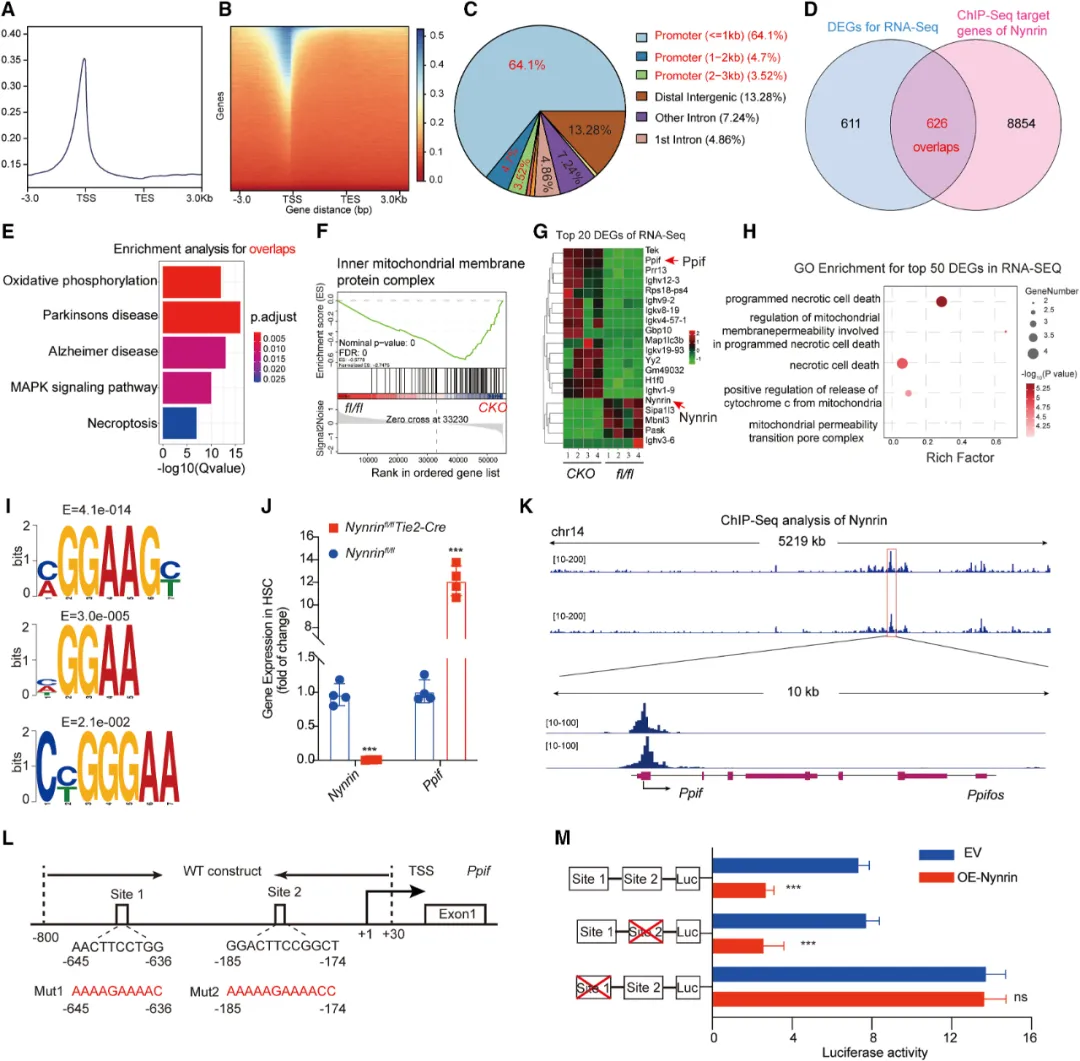
图5. Nynrin通过转录调节造血干细胞中的Ppif来调节mPTP
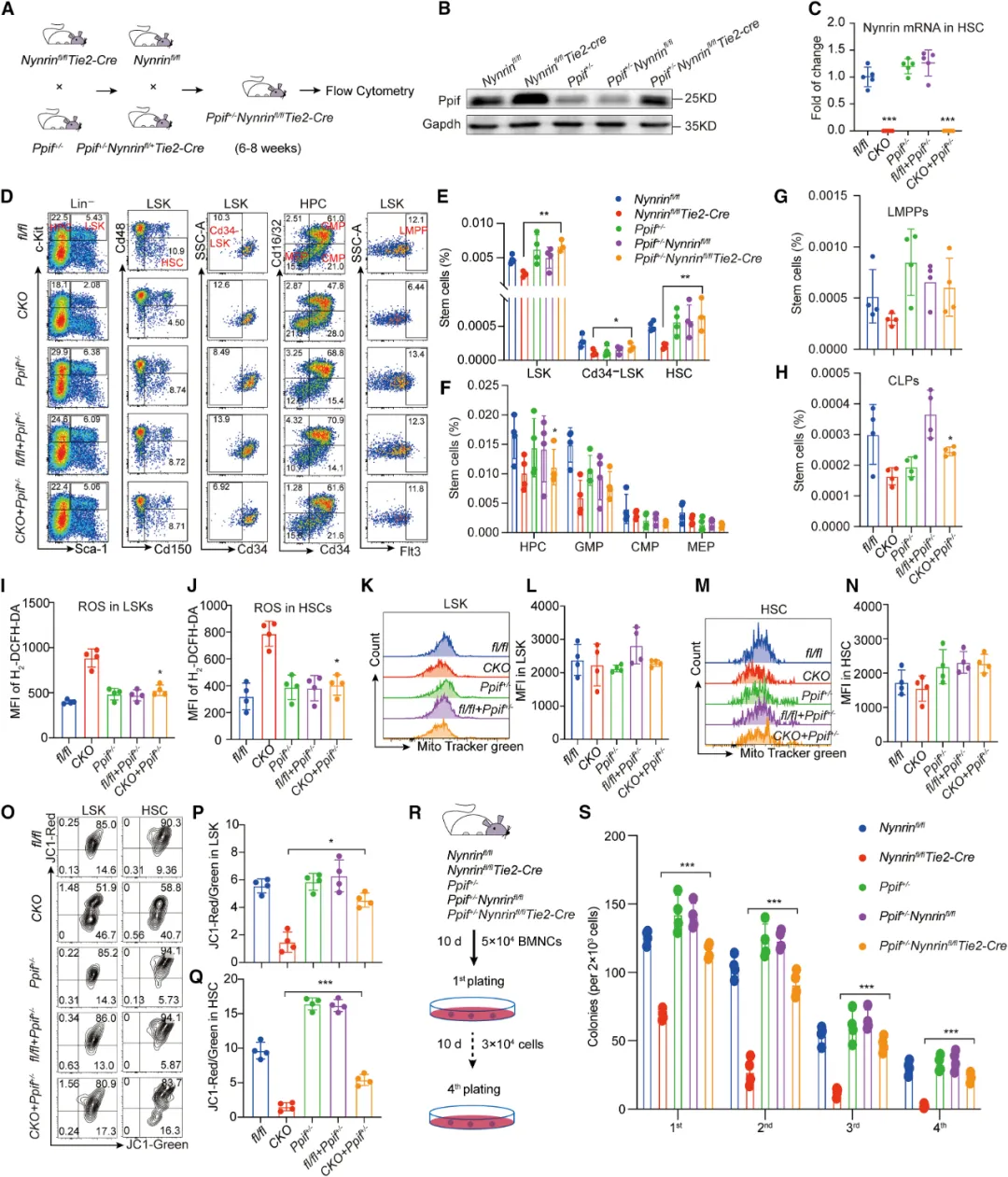
图6. 通过Ppif抑制在Nyrin缺陷小鼠中增强线粒体功能和HSC恢复
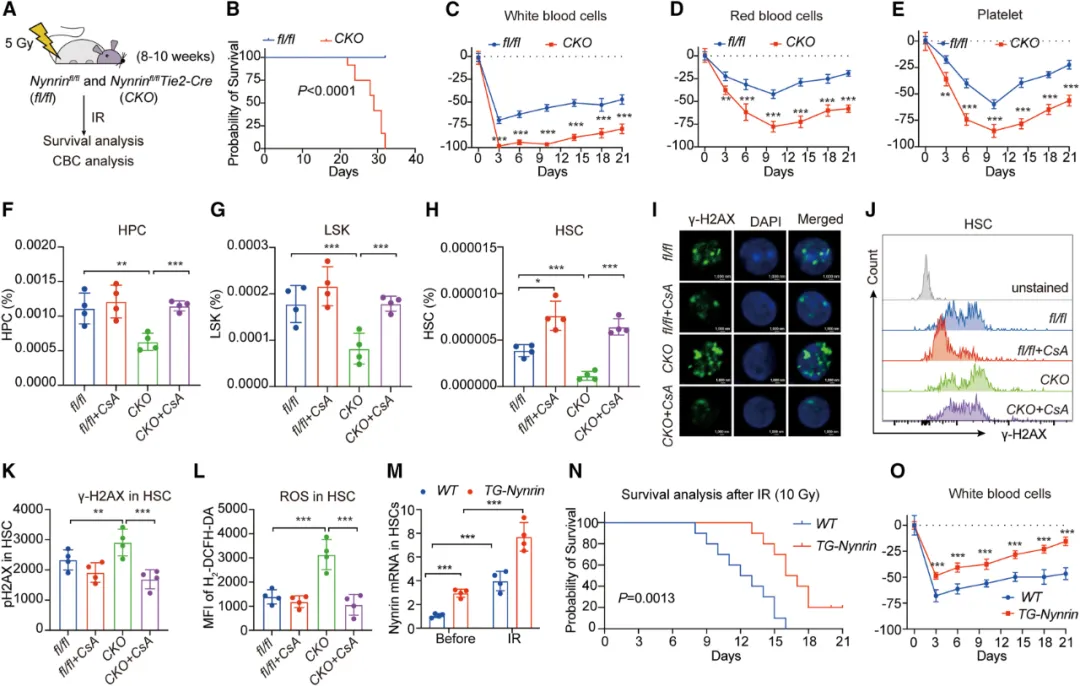
图7. 缺乏Nynrin的造血干细胞对辐射的敏感性增加
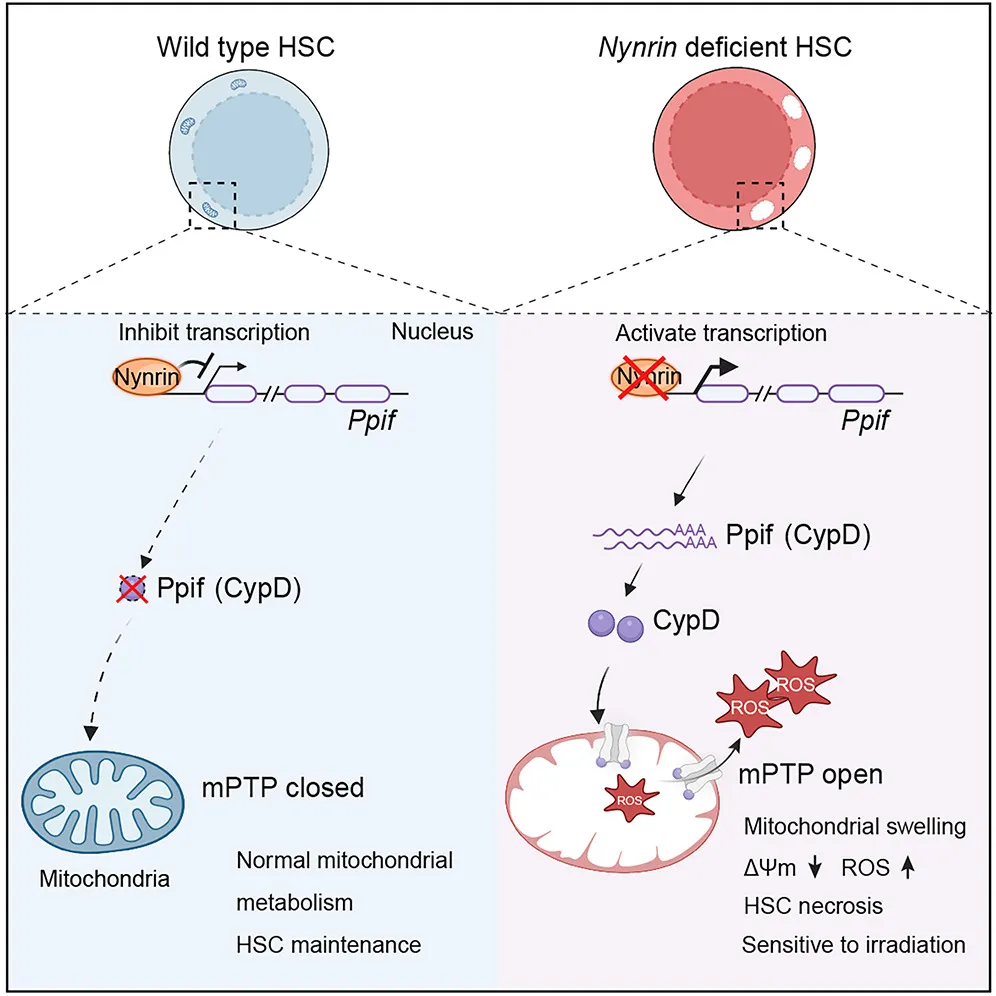
图8. Abstract
结论与讨论
本文发现Nynrin是维持HSCs功能的关键因素,通过抑制mPTP的开启来保护HSCs免受辐射损伤。Nynrin缺失导致HSCs的自我更新能力下降,而Nynrin过表达则提高了HSCs的辐射耐受性。此外,Nynrin通过调控Ppif基因的表达来抑制mPTP的活性,减少ROS的产生,从而维持HSCs的稳态。
在未来,可以进一步探索Nynrin在不同应激条件下的保护机制,以及如何通过药物或其他干预手段来调节Nynrin的活性,以增强HSCs的辐射耐受性和改善造血功能,特别是在癌症治疗和血液疾病中的应用。
















 {{item.name}}会员
{{item.name}}会员
