STTT | 北京大学研发pH/酶双重响应性纳米PROTAC,实现肿瘤细胞内精准递送和增强降解效果
Highlights
1. 设计pH/酶响应纳米粒子 PSRNs,克服PROTACs局限,实现精准细胞内递送。
2. PSRNs增强CDK4/6降解,提高抗肿瘤效果,增强肿瘤对免疫治疗敏感性。
近日,“Signal Transduction and Targeted Therapy”(IF=40.8)上发表了一篇题为“Sequential responsive nano-PROTACs for precise intracellular delivery and enhanced degradation efficacy in colorectal cancer therapy”的文章。这篇文章介绍了一种新型的纳米PROTACs(PSRNs),它们能够响应酸性环境和酶,以实现在结直肠癌治疗中的精准细胞内递送和增强的降解效果。

研究背景介绍
PROTACs是一种新型的蛋白质降解技术,通过利用细胞内的泛素-蛋白酶体系统来特异性地降解目标蛋白质。与传统的小分子抑制剂不同,PROTACs能够催化目标蛋白质的降解,从而提供了一种新的疾病治疗策略。
免疫检查点阻断(ICBs)是一种通过激活患者自身免疫系统来攻击肿瘤细胞的癌症治疗策略。然而,许多肿瘤微环境存在免疫抑制性,限制了ICBs的疗效。
CDK4/6是细胞周期调控的关键蛋白,其异常活化与多种癌症的发生发展有关。
研究思路分析
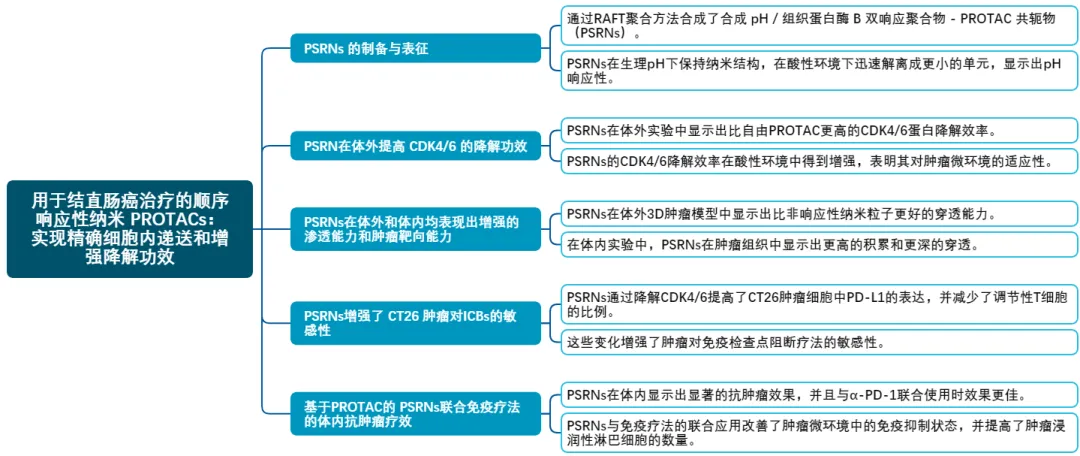
研究技术路线图
01设计与表征
①合成了一种新型的基于Von Hippel-Lindau(VHL)的CDK4/6靶向PROTAC,它能够在癌细胞中有效降解CDK4/6蛋白,并且与现有的小分子抑制剂不同,它通过泛素-蛋白酶体途径实现降解,而不是导致蛋白水平的增加。②此外,合成pH敏感单体EPA-MA和组织蛋白酶B响应单体MAGFLG-PROTAC,通然后用RAFT聚合法合成PEG-b-P(EPA-r-PROTAC)。同时合成对比用的pH非响应聚合物-PROTAC共轭物、pH响应和非响应聚合物,分别自组装得到PSRNs和PNRNs。
②PSRNs和PNRNs在pH7.4时平均直径分别为41.5nm和53.8nm。多分散性指数分别为0.270和0.228。在酸性pH6.6下,PSRNs完全解离成约8.9nm的无定形单体,而PNRNs保持相同大小。PROTAC从PSRNs释放是酶响应性的,需要弱酸性环境和酶降解,且酸性解离应先于酶切,PNRNs因维持纳米结构阻碍酶切,PROTAC释放量少。
02体外效果评估
①评估了非PROTAC纳米颗粒PEG-b-P(EPA)和PEG-b-P(EH)在CT26肿瘤细胞中的生物安全性,发现它们在pH7.4和pH6.6的培养基中,浓度高达1mg/mL时,细胞毒性有限。接着研究了PSRNs的细胞内吞和药物释放,发现PSRNs在pH6.6时的细胞内吞率明显高于pH7.4,而PNRNs的细胞内吞率较低。
②还观察到,PSRNs在细胞内吞后,在CT26细胞中,超过90%的PROTAC在1小时内迅速释放。评估PSRNs在体外对CDK4/6蛋白的降解效率,发现PSRNs和自由PROTAC在各种肿瘤细胞中均表现出高效的蛋白降解能力。最后,评估PROTAC制备物在肿瘤细胞上的细胞毒性,发现PSRNs在pH6.6时表现出优异的细胞毒性,与自由PROTAC相似或超过。
03体内效果评估与治疗策略
①利用3D多细胞肿瘤球体模型在不同pH下用Cy5标记的PSRNs和PNRNs孵育肿瘤球体,发现PSRNs荧光强度高于PNRNs且在pH 6.6时可深入肿瘤球体45μm,PNRNs荧光弱且位于边缘;在健康小鼠中,PSRNs和PNRNs都能迅速在肿瘤部位积累,但PSRNs在肿瘤内的穿透更深。
②研究发现,抑制CDK4/6可以增强CT26肿瘤对ICBs的敏感性。实验中,PSRNs处理CT26肿瘤细胞后,发现CDK4/6的降解能够增加PD-L1蛋白水平。此外,PSRNs比PNRNs更容易被Treg细胞摄取,且Treg细胞对PSRNs的摄取量比CD8+T细胞高1.6倍。在CT26荷瘤小鼠中,经过5次CDK4/6靶向PROTAC的腹腔注射后,肿瘤和脾脏中的Treg/CD8+T细胞比例显著下降,表明PSRNs能有效调节免疫抑制性肿瘤微环境(TME)。表明PSRNs能够增强CT26肿瘤对ICBs的敏感性,并为将CDK4/6 PROTAC治疗与α-PD-1免疫疗法相结合提供了分子依据。
③在CT26荷瘤小鼠中研究单次静脉注射后蛋白降解效果,PSRNs对CDK4/6的降解效果比游离PROTAC高2.6-3.0倍,且PSRNs在体内有延长的降解效果。在CT26肿瘤异种移植的小鼠中评估PSRNs的抗肿瘤效果,与游离PROTAC组相比,pH/组织蛋白酶B响应递送系统显著提高了抗肿瘤效果,降低了肿瘤中CDK4/6表达,增加了肿瘤坏死。将PSRNs与ICBs联合治疗进一步提高了抗肿瘤效果,延长了中位生存时间,主要器官无明显组织损伤。
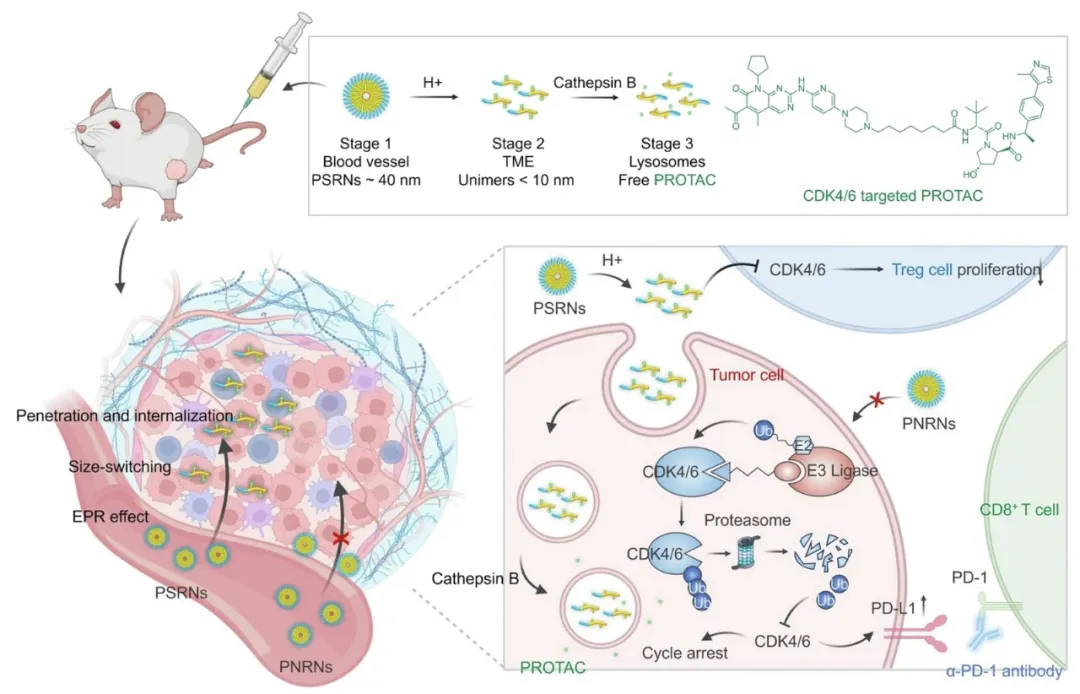
图1. 针对CDK4/6的PROTAC结构,静脉给药后 PSRN 的顺序反应过程示意图
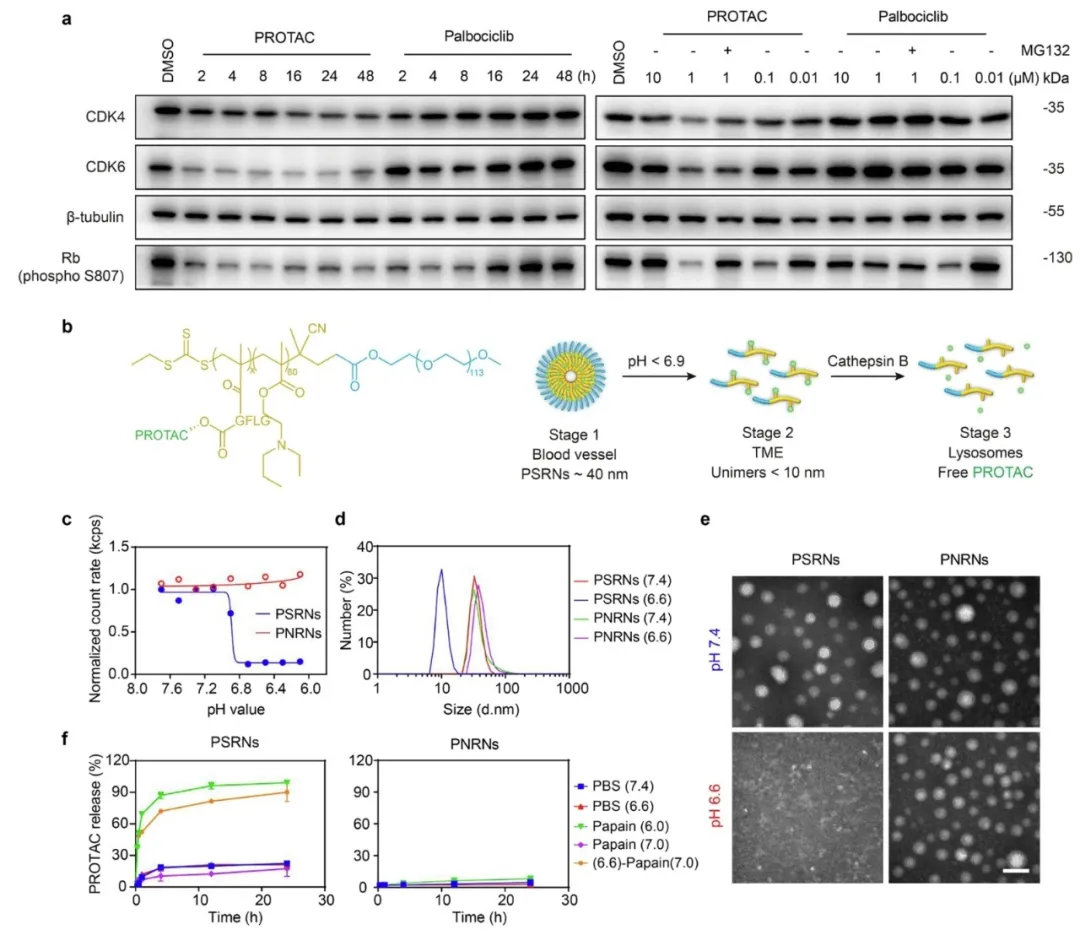
图2. CDK4/6降解PSRNs的制备与表征
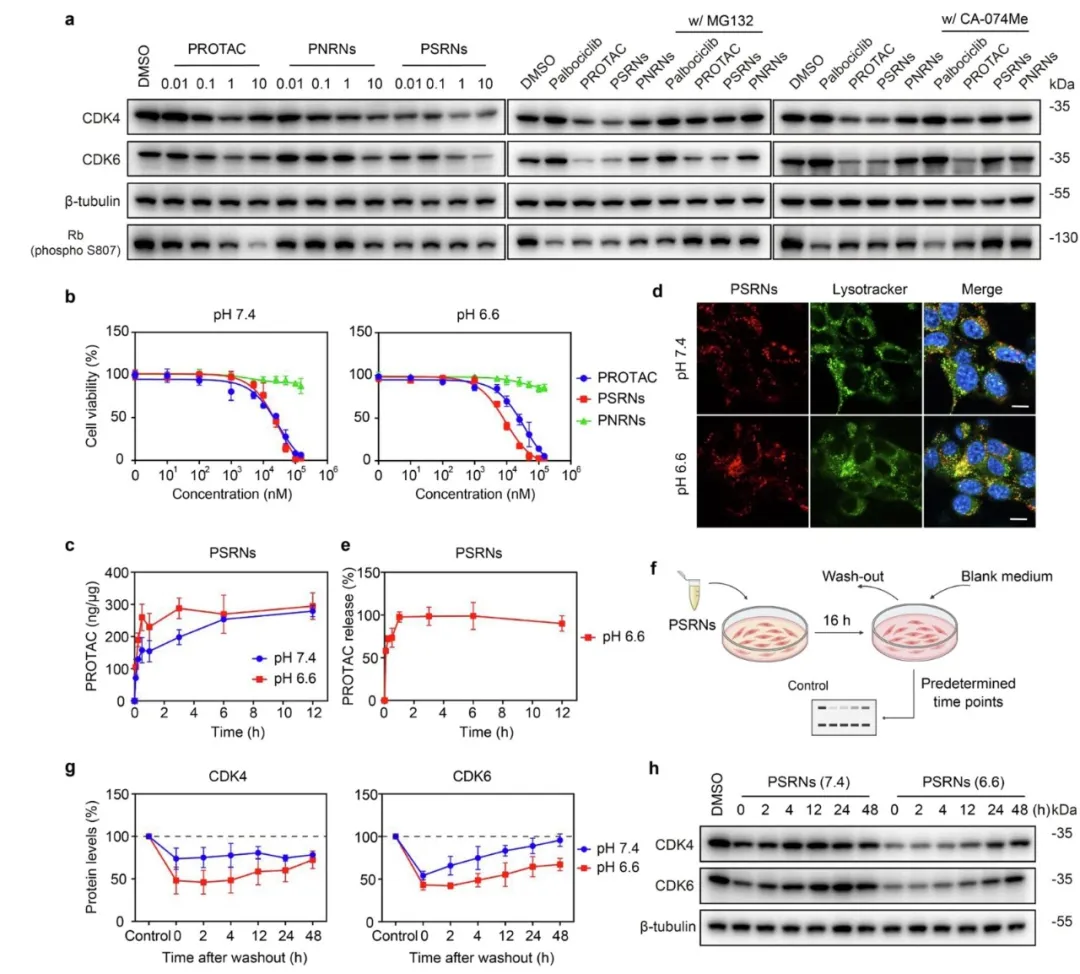
图3. 体外CDK4/6降解效能的提高
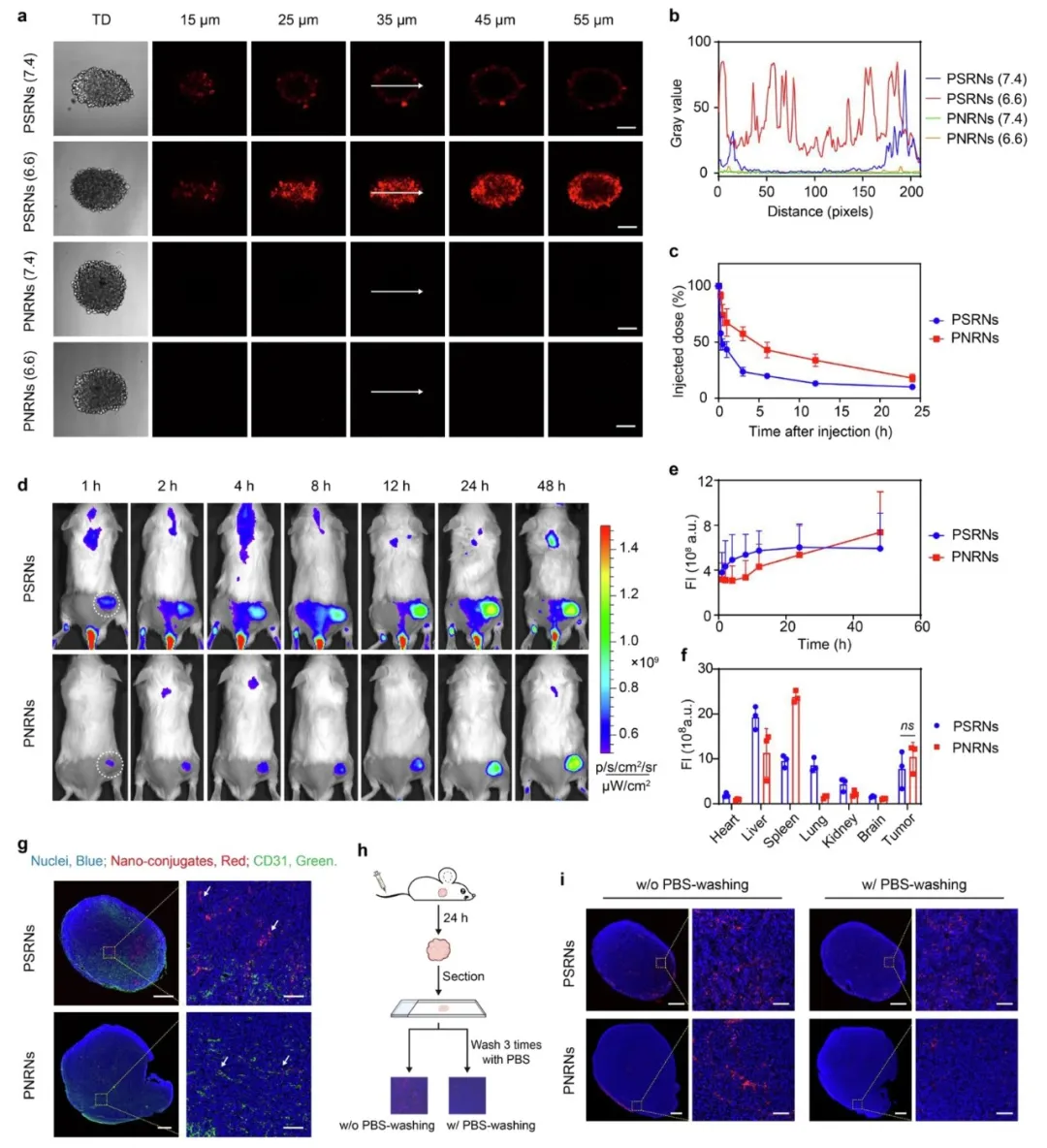
图4. 体内外肿瘤穿透和积累的增强
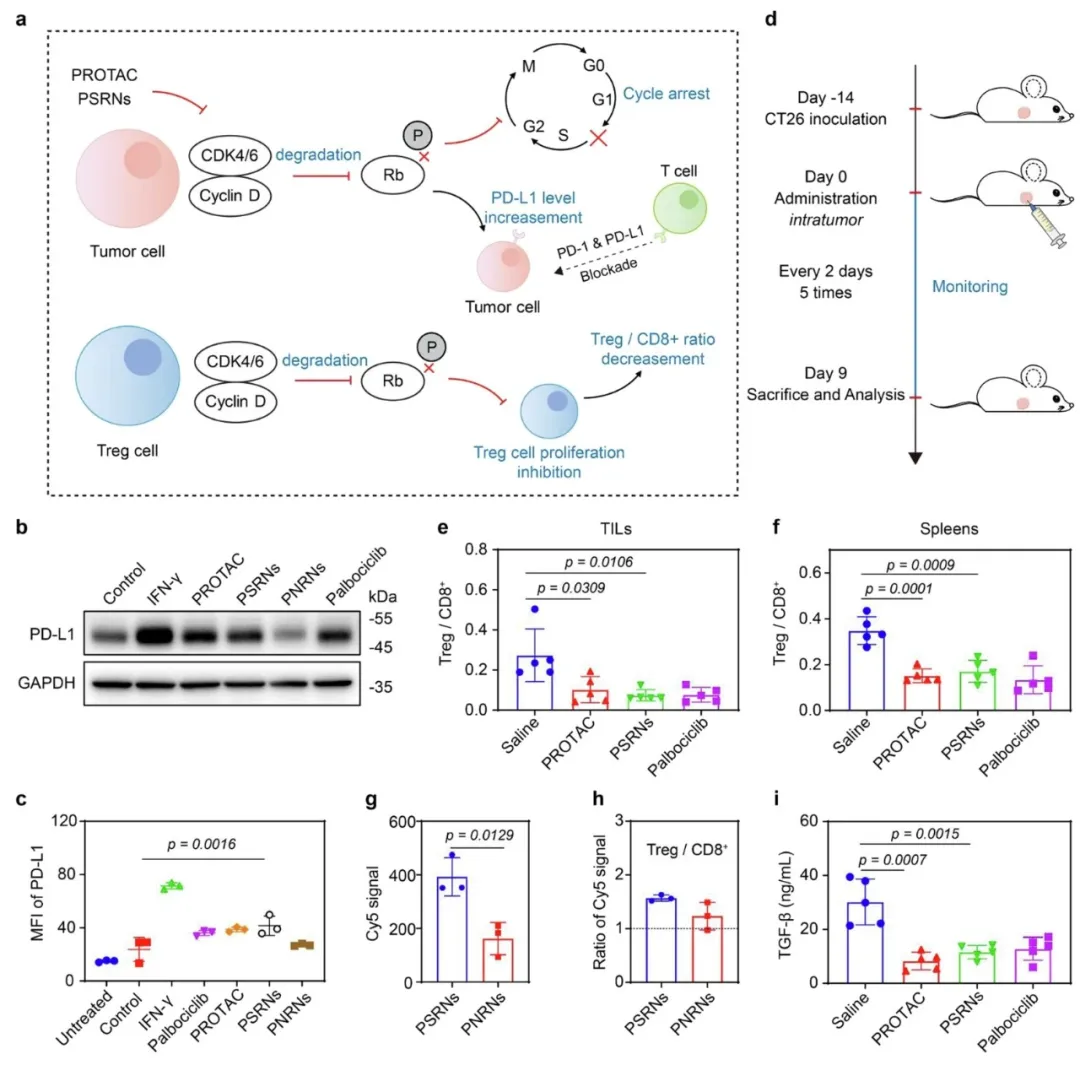
图5. PSRNs增强了CT26肿瘤对ICBs的敏感性
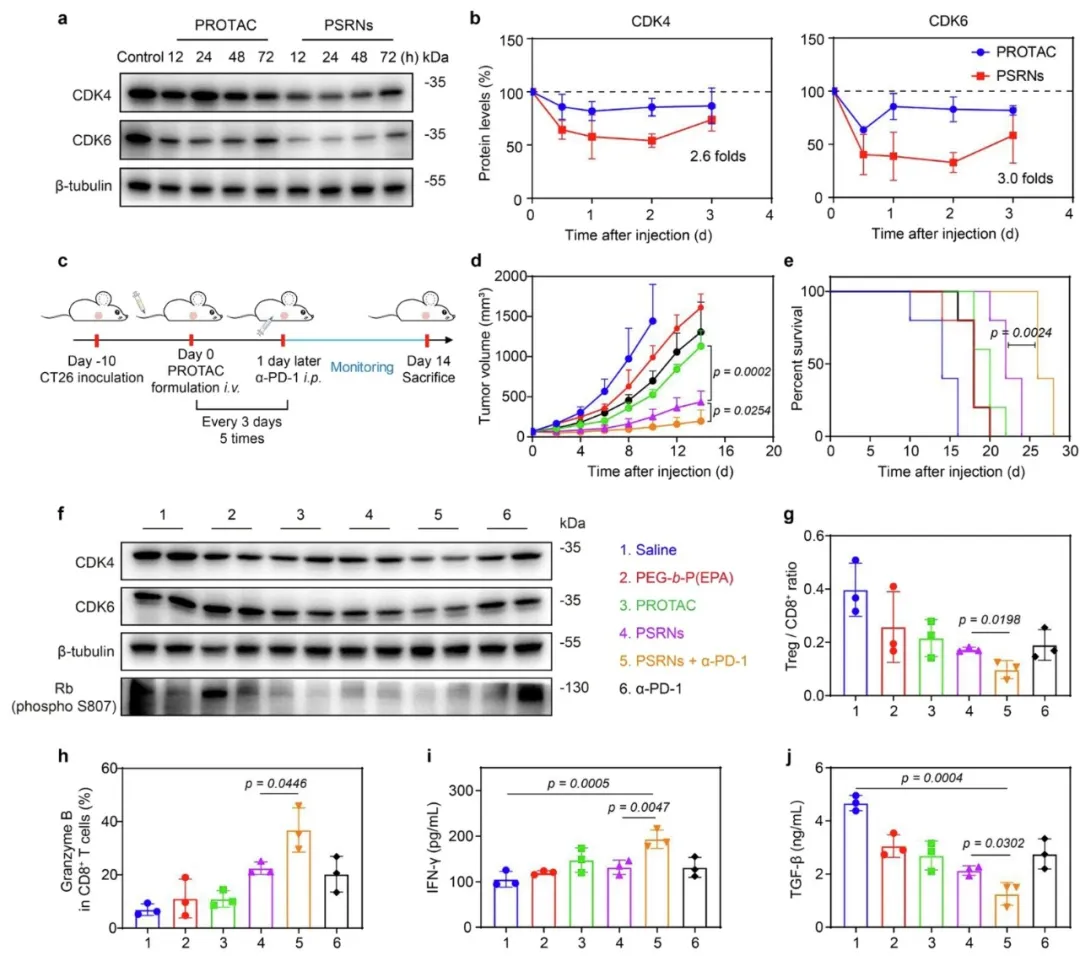
图6. PSRNs与免疫疗法联合应用的体内抗肿瘤效能
结论与讨论
本研究成功开发了一种pH/组织蛋白酶B双重响应的PROTAC纳米粒子(PSRNs),用于结直肠癌中CDK4/6的降解。PSRNs在体内外实验中显示出比自由PROTAC更高的CDK4/6降解效率和抗肿瘤效果,能够有效地在肿瘤微环境中响应并释放PROTAC,增强了肿瘤对免疫检查点阻断的敏感性。此外,PSRNs与免疫疗法的联合使用显著提高了治疗效果,为结直肠癌的治疗提供了新的策略。
未来研究需要进一步探索PSRNs在人体中的药代动力学、毒性和治疗效果。此外,还需要研究PSRNs对不同肿瘤类型的适用性,以及如何优化其设计以减少潜在的脱靶效应。而结合其他治疗手段如放疗和化疗,可能会进一步提高PSRNs的治疗效果,这些都需要在未来的研究中进行深入探讨。
















 {{item.name}}会员
{{item.name}}会员
