南京医科大学创新发现:铜代谢在创伤性脑损伤中线粒体自噬和神经保护中的作用
Highlights
1. TBI后脑内铜水平上升,并影响线粒体自噬加剧神经损伤。
2. BNIP3在线粒体自噬中起关键作用,提高其表达有助于保护神经细胞,改善脑损伤后的认知功能。
3. TRIM25通过影响NFKB信号通路来调控BNIP3,这可能是治疗脑损伤的新靶点。
近日,“Autophagy”(IF=14.6)上发表了一篇题为“Copper aggravated synaptic damage after traumatic brain injury by downregulating BNIP3-mediated mitophagy”的文章。这篇文章探讨了铜离子在创伤性脑损伤后突触损伤中的作用,特别是其对BNIP3介导的线粒体自噬的调控影响。

研究背景介绍
创伤性脑损伤(TBI)是导致儿童和青年死亡和残疾的主要原因之一,它会引起急性机械性脑组织损伤和随后的氧化应激、炎症反应等二次损伤。
线粒体自噬是一种选择性自噬过程,通过降解损伤的线粒体来维持线粒体稳态,对神经细胞的生存和减少神经功能障碍具有重要作用。
Bcl2/腺病毒E1B相互作用蛋白3(BNIP3)是一种具有非典型BH3结构域的BCL2家族蛋白,主要定位于线粒体外膜,它在介导线粒体自噬中发挥重要作用,尤其是在脑缺血后对少突胶质细胞和神经元的保护作用。
TRIM25是一种E3泛素连接酶,参与调控多种细胞过程,包括细胞周期、基因翻译、基因表达、抗原呈递和炎症发展。
研究思路分析
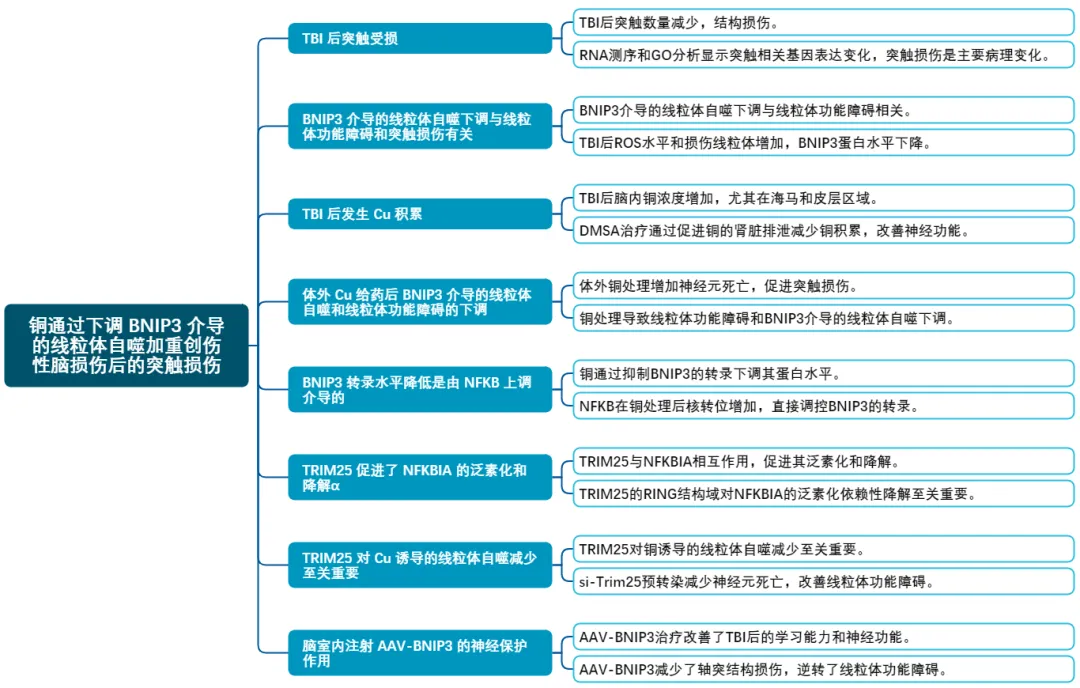
研究技术路线图
01突触损伤与线粒体功能障碍
①通过RNA测序技术比较了TBI小鼠组和假手术组之间的全局基因表达差异。结果发现,与假手术组相比,TBI组中有837个基因上调,1138个基因下调,GO分析显示,与突触相关的术语如“突触前膜”、“突触膜”、“突触后膜”和“突触组织”在TBI组中显著富集,表明突触损伤是闭合性脑损伤后的主要病理变化。此外,Reactome分析表明TBI后氧气的使用受到阻碍,这通常与线粒体损伤相关,因此研究聚焦在线粒体功能障碍的机制上。
②观察了TBI后不同时间点海马突触的状态,并发现突触数量逐渐减少,透射电镜可清晰检测到突触结构损伤。进一步检查了神经元细胞体中的活性氧(ROS)和线粒体水平,发现TBI后ROS水平、受损线粒体数量和细胞凋亡显著增加,表明线粒体介导的细胞凋亡与突触损伤密切相关。
③受损线粒体通过线粒体自噬进行溶酶体降解,线粒体自噬失衡可导致线粒体功能障碍,进一步研究发现,与TBI后14天相比,28天线粒体长度明显缩短,自噬体数量减少,这意味着线粒体功能障碍可能是线粒体自噬受损的结果。TBI后BNIP3蛋白水平下降,COX4/COX IV水平上升,其他线粒体自噬相关蛋白无变化,突出BNIP3在控制TBI后线粒体功能障碍中的重要作用。通过检查COX4与MAP1LC3B/LC3B和LAMP2的共定位评估线粒体自噬,发现TBI后两者共定位均减少。
02铜代谢紊乱与线粒体自噬
①研究发现,TBI后脑皮质和海马区的铜浓度增加,并在28天达到峰值。使用DMSA(一种促进铜通过肾脏排泄的药物)治疗可以显著降低海马区的铜浓度。DMSA治疗还减少了突触和线粒体的结构损伤,逆转了BNIP3蛋白水平的下降,促进了损伤线粒体的清除,保护了突触,并减少了神经元凋亡。在水迷宫实验中,DMSA处理的小鼠表现出比TBI组更好的学习能力。表明铜的积累损害了BNIP3介导的线粒体自噬,从而导致了神经功能障碍。
②构建了一个体外铜过载神经元模型,使用CuCl2来探索铜如何触发线粒体功能障碍的分子和细胞机制。研究发现,铜处理增加神经元死亡并促进了突触损伤。MitoTracker结果显示铜处理减少了线粒体面积、周长、形态因子和长宽比,表明线粒体受损。此外,铜处理后线粒体膜电位显著下降,表明线粒体功能障碍。③此外,研究发现铜处理下调了BNIP3介导的线粒体自噬,并且随着铜浓度的增加,损伤线粒体的清除和LC3B与COX4的共定位显著减少。强调了铜-BNIP3轴在TBI后神经恢复中的重要作用。
03分子机制与神经保护
①研究发现铜处理通过抑制BNIP3转录来下调其的表达,而非通过蛋白降解途径。进一步研究发现铜处理后NFKB在核中的含量随铜浓度增加而显著增加,且NFKB转移到核中。构建敲低和过表达质粒的实验表明,BNIP3的转录受NFKB的调控。此外,沉默NFKB(si-NFKB)可以逆转铜处理引起的BNIP3转录和蛋白水平的下降,减少细胞凋亡,并改善BNIP3介导的线粒体自噬。表明,NFKB在铜诱导的BNIP3下调和细胞凋亡中起着关键作用。
②研究发现铜处理能够促进核因子κB抑制因子α(NFKBIA)的磷酸化和降解,且这一过程涉及泛素-蛋白酶体途径。进一步研究发现TRIM25是与NFKBIA相互作用最丰富的蛋白。co-IP分析和共聚焦显微镜观察证实了NFKBIA与TRIM25在原代神经元和瞬时转染的HEK-293细胞中的相互作用。TRIM25的RING结构域对NFKBIA-TRIM25的相互作用至关重要,该结构域的缺失完全阻断了两者的相互作用。表明TRIM25特异性调控NFKBIA的泛素化依赖性降解。
③研究发现,在体内给予200 μmol/L铜处理后,预转染si-Trim25能够减少NFKBIA的泛素化和降解,并且减少NFKB的核转位,从而改善BNIP3介导的线粒体自噬。此外,si-Trim25预转染能够减少神经细胞死亡和线粒体功能障碍,提高BNIP3蛋白水平以及LC3B与COX4的共定位。表明TRIM25可能通过TRIM25-NFKBIA-NFKB-BNIP3轴影响铜处理后的线粒体自噬和神经功能。
④评估BNIP3介导的线粒体自噬对神经功能的保护作用,在水迷宫测试中,神经元中BNIP3的特异性促进的小鼠相比于对照组(AAV-NC)展现出更好的学习能力。通过透射电子显微镜观察,AAV-BNIP3处理减少了TBI后28天海马区轴突的结构损伤,并逆转了线粒体功能障碍。此外,与AAV-NC组相比,AAV-BNIP3增强了神经严重程度评分,表明BNIP3的药理学恢复可能通过促进线粒体自噬有效改善突触功能和神经康复。
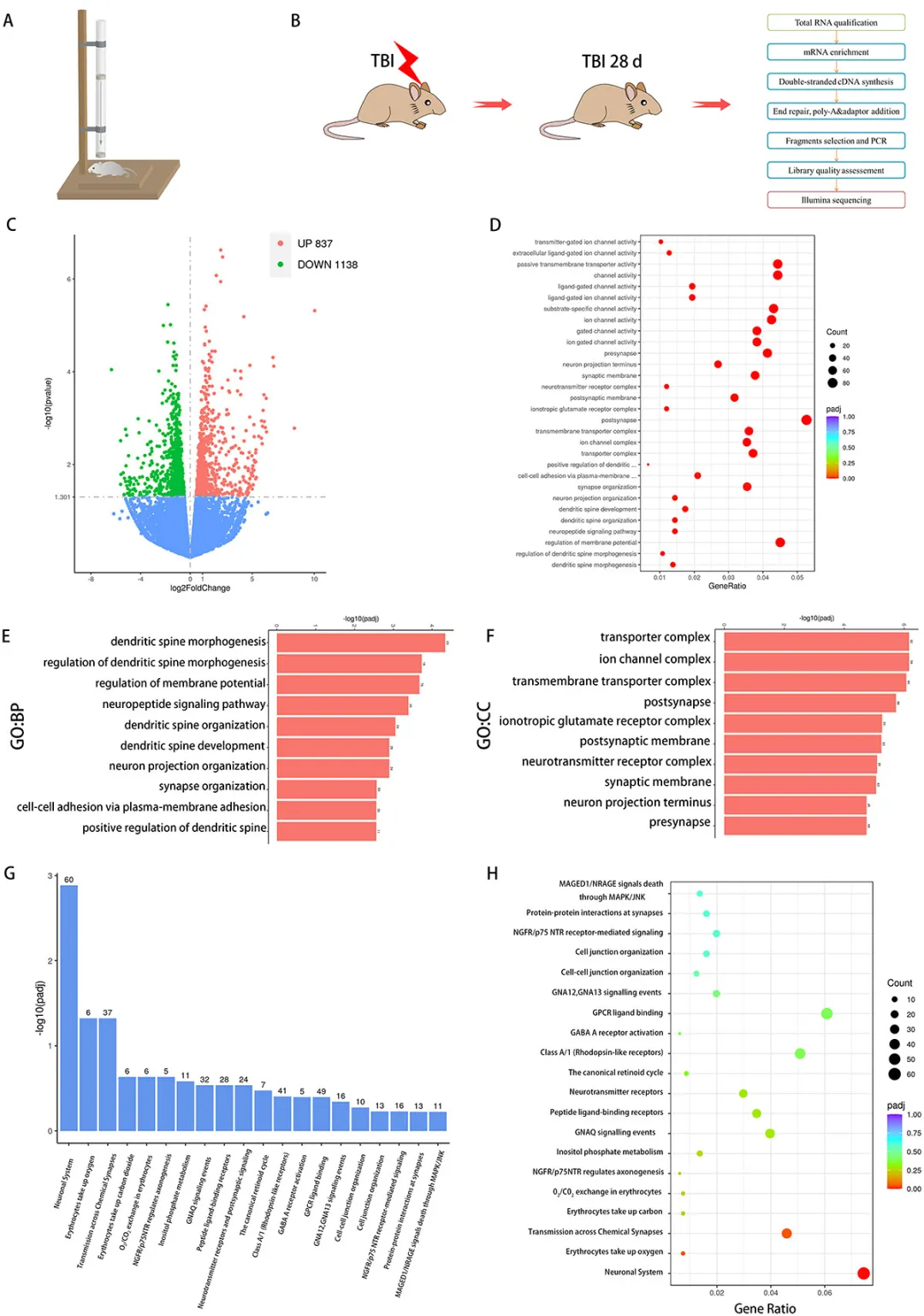
图1. TBI后突触受损
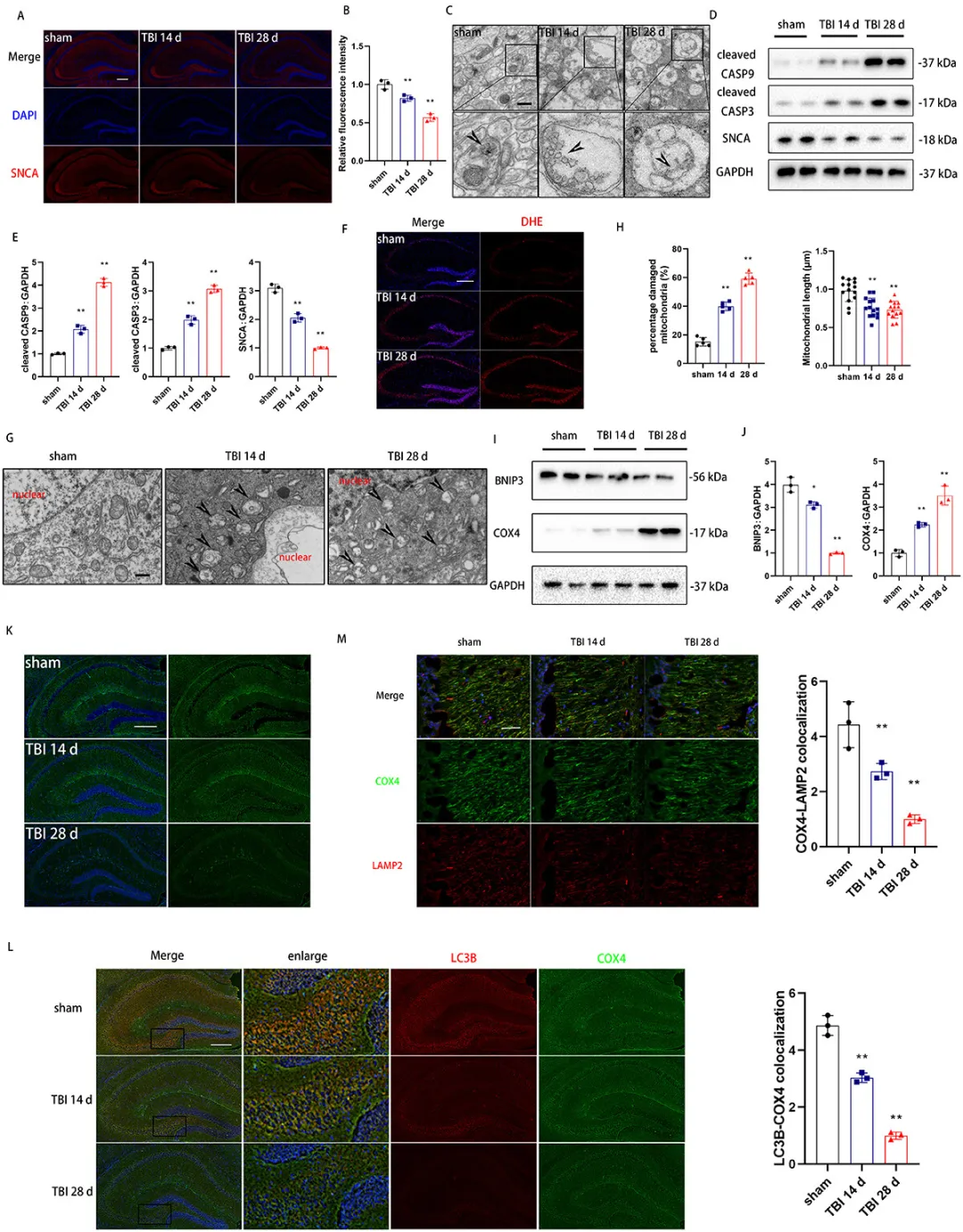
图2. BNIP3介导的线粒体自噬下调与线粒体功能障碍和突触损伤相关
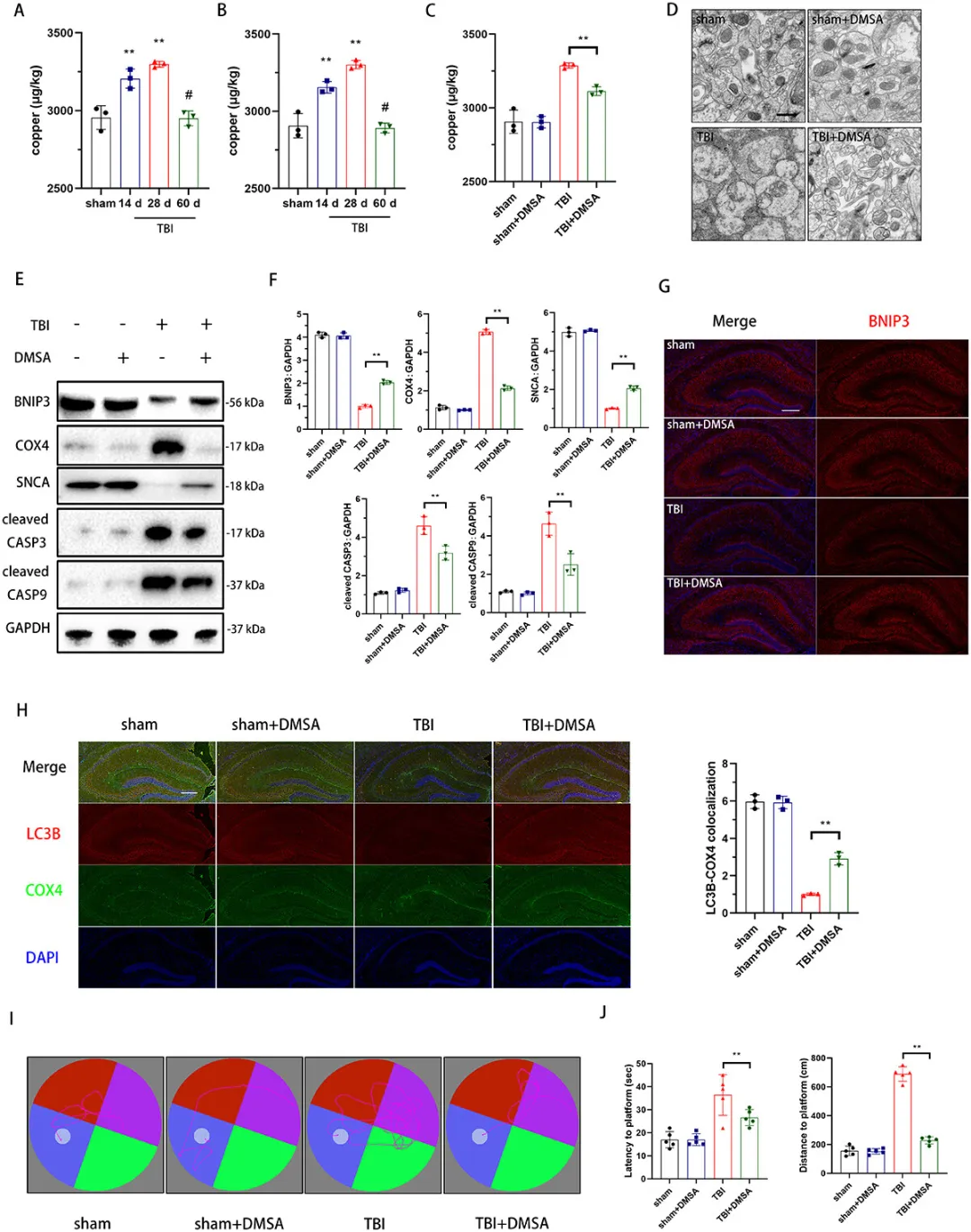
图3. TBI后铜积累
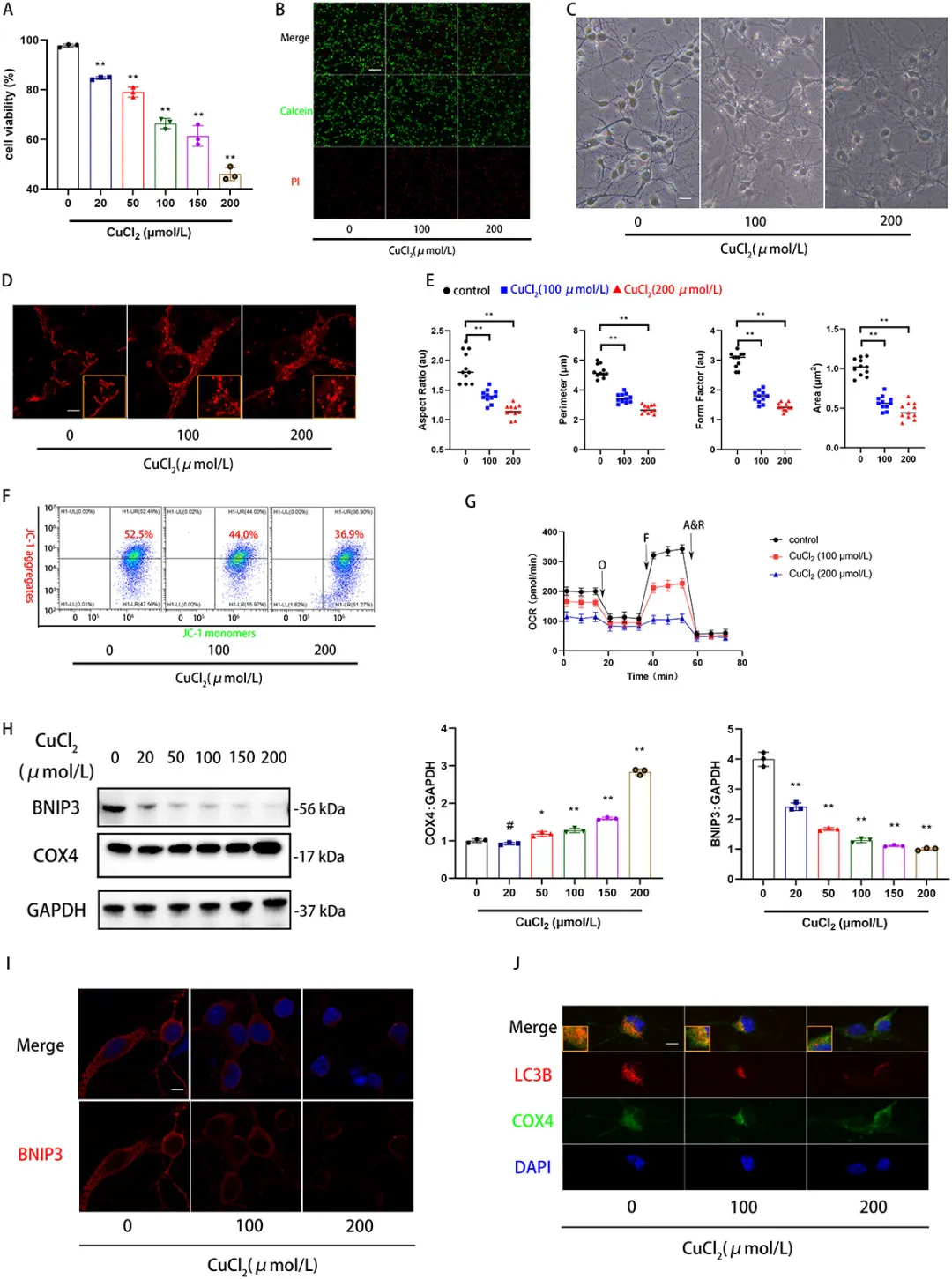
图4. 体外铜处理后BNIP3介导的线粒体自噬下调和线粒体功能障碍
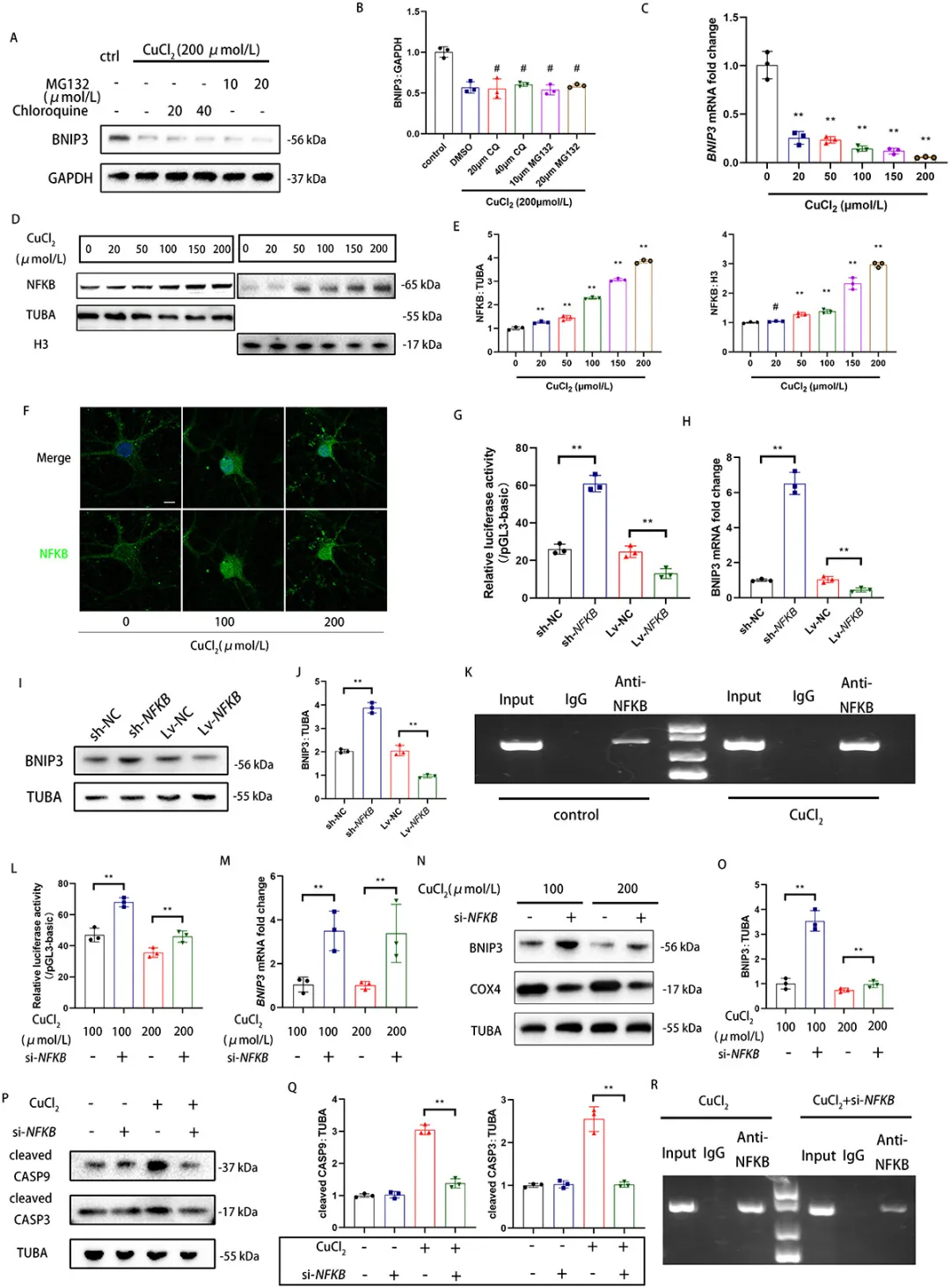
图5. BNIP3转录水平的降低是通过NFKB上调介导的
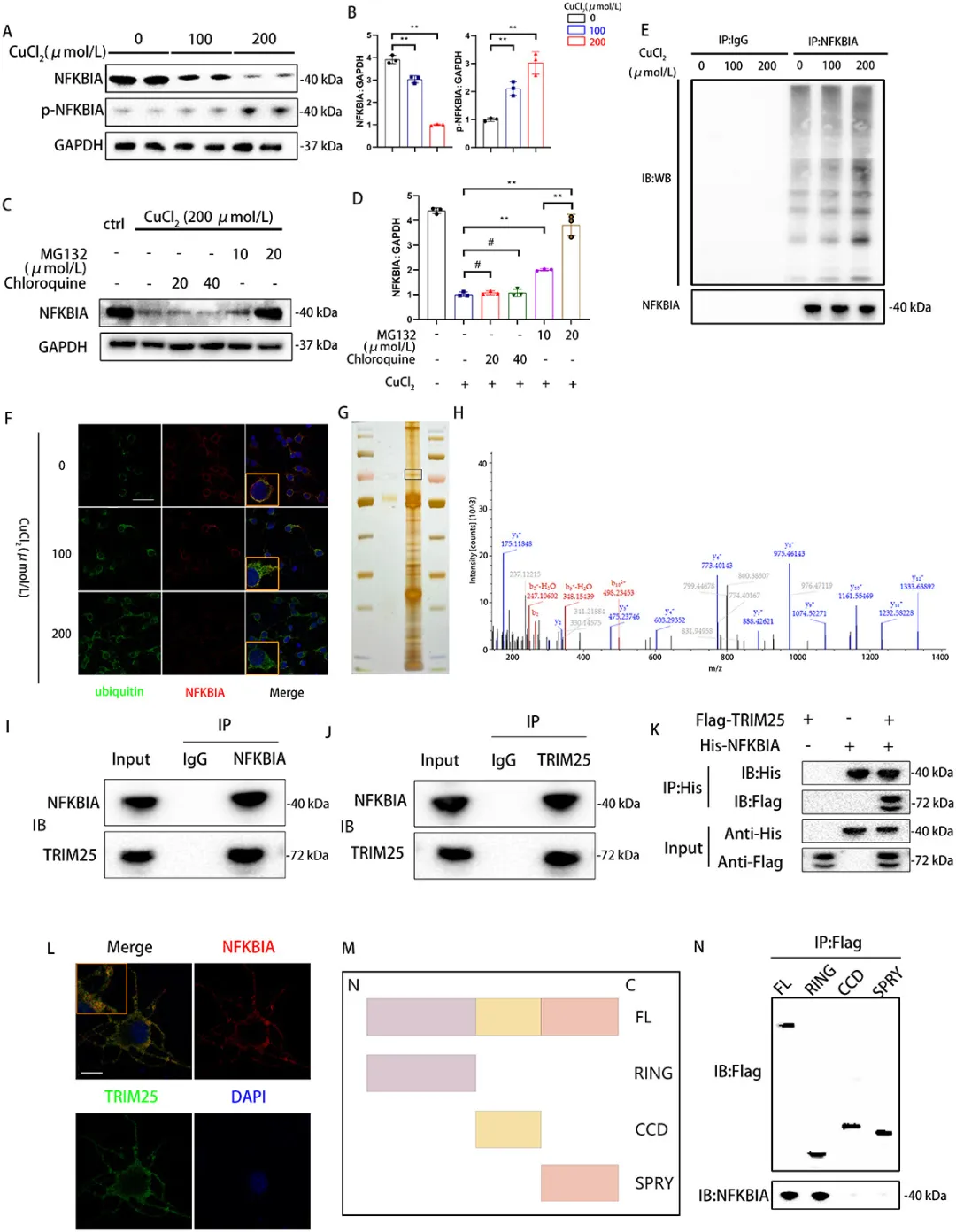
图6. TRIM25介导NFKBIA的泛素化降解
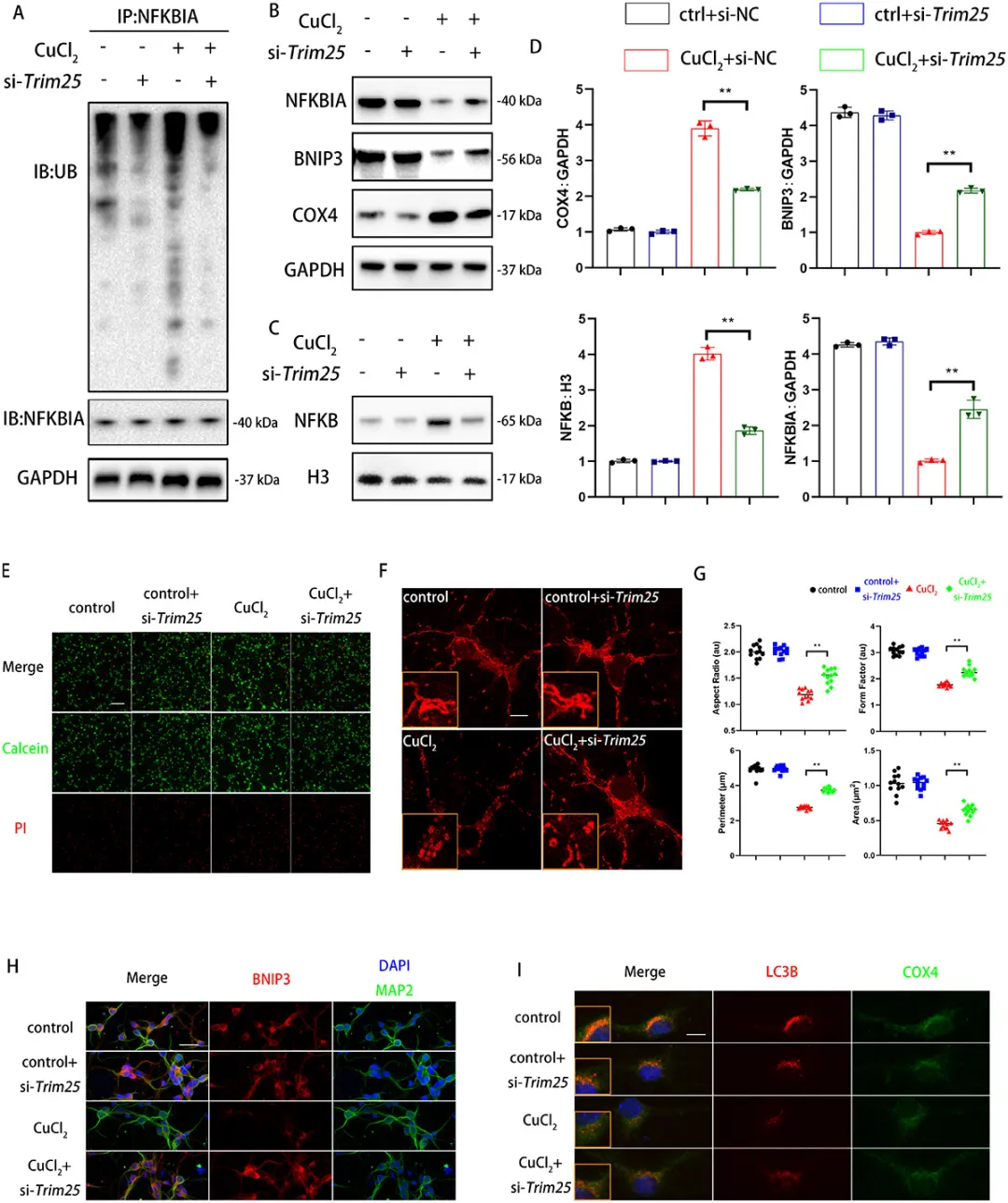
图7. TRIM25对铜诱导的线粒体自噬减少至关重要
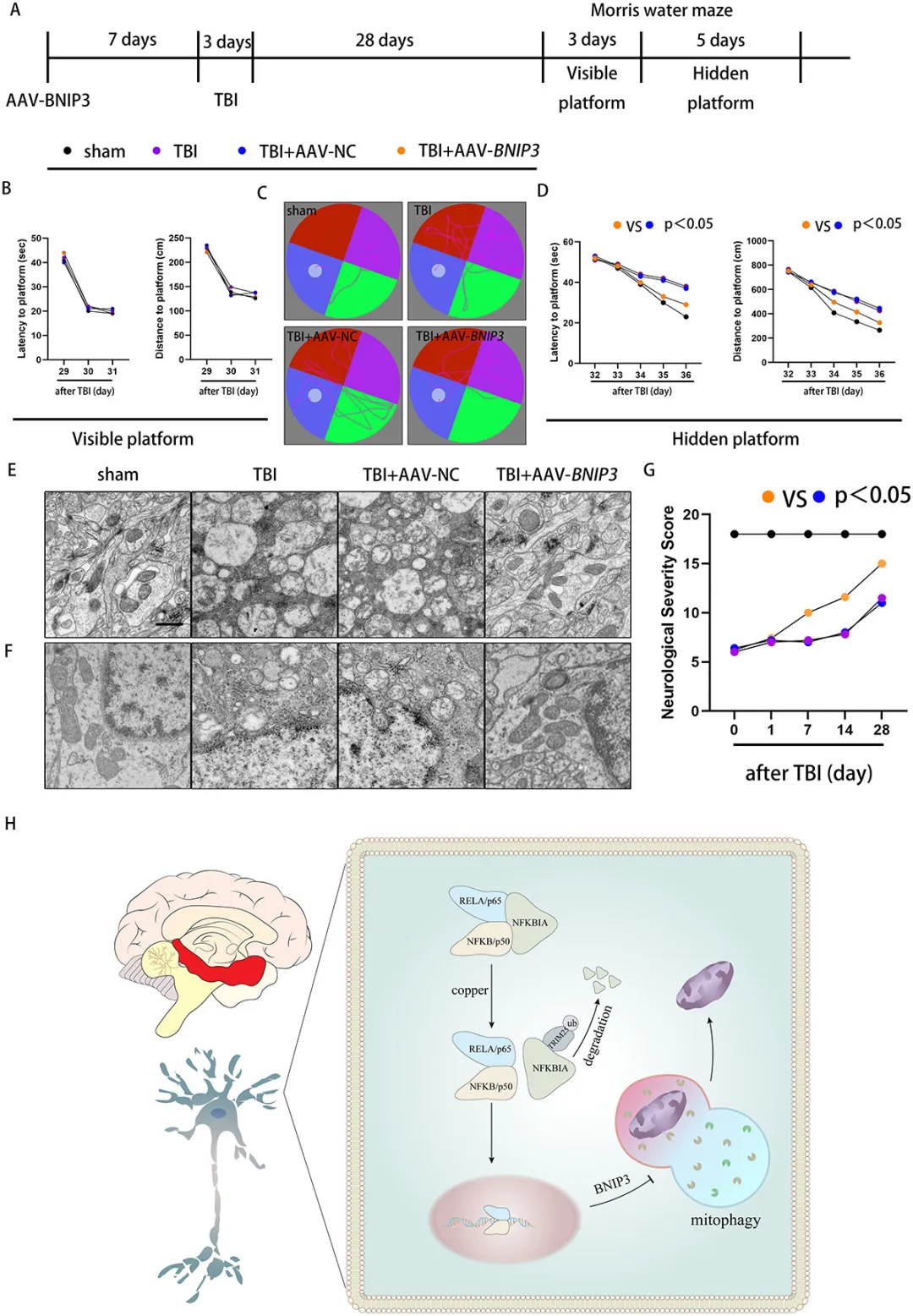
图8. 脑室内注射AAV-BNIP3的神经保护效果
结论与讨论
本研究发现,铜积累通过NFKB信号通路下调BNIP3表达,抑制线粒体自噬,加剧了创伤性脑损伤后的突触损伤和神经功能障碍。通过药物DMSA降低铜浓度或通过AAV病毒载体提高BNIP3表达,可以改善线粒体功能,减少神经元凋亡,并提高认知功能,表明靶向铜代谢和BNIP3介导的线粒体自噬可能是治疗创伤性脑损伤的潜在策略。
未来研究需要进一步探索铜代谢紊乱在开放性脑损伤中的作用,并评估AAV基因治疗在人类中的应用潜力和准确性。此外,研究还应开发更多针对线粒体自噬的药物,以预防和治疗创伤性脑损伤中的线粒体功能障碍和轴突损伤。
















 {{item.name}}会员
{{item.name}}会员
